早教吧作业答案频道 -->化学-->
有下列7种物质:①HF②H2O③NH3④CH4⑤SiO2⑥NaCl⑦CO2请根据要求回答:ⅠNH3分子的空间构型为;基态F原子的电子排布图为.ⅡCH4难溶于水的原因是.Ⅲ以上7种物质属于极性分子的是(
题目详情
有下列7种物质:①HF②H2O③NH3④CH4⑤SiO2⑥NaCl⑦CO2请根据要求回答:
ⅠNH3分子的空间构型为___;基态F原子的电子排布图为___.
ⅡCH4难溶于水的原因是___.
Ⅲ以上7种物质属于极性分子的是___(填数字序号)
Ⅳ②⑤⑥⑦四种物质的沸点由高到低的顺序是___(填数字序号).
Ⅴ测定HF的相对分子质量时,实验测得值一般高于理论值,主要原因是___.
ⅠNH3分子的空间构型为___;基态F原子的电子排布图为___.
ⅡCH4难溶于水的原因是___.
Ⅲ以上7种物质属于极性分子的是___(填数字序号)
Ⅳ②⑤⑥⑦四种物质的沸点由高到低的顺序是___(填数字序号).
Ⅴ测定HF的相对分子质量时,实验测得值一般高于理论值,主要原因是___.
▼优质解答
答案和解析
Ⅰ氨气分子中价层电子对个数=3+
×(5-3×1)=4且含有一个孤电子对,所以氨气分子为三角锥形结构;F原子核外有9个电子,分别位于1S、2S、2P轨道,其轨道表示式为: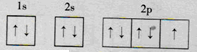 ,
,
故答案为:三角锥形; ;
;
ⅡCH4分子中有四个等同的C-H键,CH4是正四体的结构,为非极性分子,H2O中心原子O原子价层电子对为2+2=4,VSEPR模型为四面体,由于含有2对孤电子对,故为V型,是极性分子,根据结构相似相溶可知CH4难溶于水,
故答案为:甲烷为非极性溶质,水是极性溶剂;
Ⅲ①HF是直线形分子,分子结构对称,但正负电荷的中心不重合,属于极性分子;②H2O中心原子O原子价层电子对为2+2=4,VSEPR模型为四面体,由于含有2对孤电子对,故为V型,属于极性分子;③NH3中N原子形成3个δ键,有1个孤电子对,为sp3杂化,分子构型为三角锥形,空间结构不对称为极性分子;④CH4为正四面体结构,结构对称,正负电荷的中心重合,属于非极性分子;⑤SiO2属于原子晶体,无分子;⑥NaCl属于离子化合物,无分子;⑦CO2结构对称,正负电荷的中心重合,属于非极性分子;
故答案为:①②③;
Ⅳ⑤SiO2是原子晶体;⑥NaCl是离子晶体,②H2O、⑦CO2都是分子晶体,但②H2O分子间存在氢键,所以四种物质的熔沸点顺序为:⑤>⑥>②>⑦,
故答案为:⑤>⑥>②>⑦;
ⅤHF分子之间存在氢键,存在缔合(HF)n分子,故实验测得的相对分子质量一般高于理论值,故答案为:HF分子间存在氢键,易形成缔合分子.
| 1 |
| 2 |
 ,
,故答案为:三角锥形;
 ;
;ⅡCH4分子中有四个等同的C-H键,CH4是正四体的结构,为非极性分子,H2O中心原子O原子价层电子对为2+2=4,VSEPR模型为四面体,由于含有2对孤电子对,故为V型,是极性分子,根据结构相似相溶可知CH4难溶于水,
故答案为:甲烷为非极性溶质,水是极性溶剂;
Ⅲ①HF是直线形分子,分子结构对称,但正负电荷的中心不重合,属于极性分子;②H2O中心原子O原子价层电子对为2+2=4,VSEPR模型为四面体,由于含有2对孤电子对,故为V型,属于极性分子;③NH3中N原子形成3个δ键,有1个孤电子对,为sp3杂化,分子构型为三角锥形,空间结构不对称为极性分子;④CH4为正四面体结构,结构对称,正负电荷的中心重合,属于非极性分子;⑤SiO2属于原子晶体,无分子;⑥NaCl属于离子化合物,无分子;⑦CO2结构对称,正负电荷的中心重合,属于非极性分子;
故答案为:①②③;
Ⅳ⑤SiO2是原子晶体;⑥NaCl是离子晶体,②H2O、⑦CO2都是分子晶体,但②H2O分子间存在氢键,所以四种物质的熔沸点顺序为:⑤>⑥>②>⑦,
故答案为:⑤>⑥>②>⑦;
ⅤHF分子之间存在氢键,存在缔合(HF)n分子,故实验测得的相对分子质量一般高于理论值,故答案为:HF分子间存在氢键,易形成缔合分子.
看了 有下列7种物质:①HF②H2...的网友还看了以下:
下面是三年级某班本学期体检视力统计表.4.2以下4.3-4.64.7-4.95.0以上男生3791 2020-04-07 …
数学课上,探讨角平分线的作法时,李老师用直尺和圆规作角平分线,方法如下:作法:如图1,①在OA和O 2020-04-08 …
(2014•博野县模拟)如图,Rt△ABC中,∠C=90°,AC=3,BC=4.分别以AB、AC、 2020-05-13 …
如图,在平行四边形ABCD中,∠BAD=45°.分别以BC、CD为边向外作△BCF和△DCE,使B 2020-07-20 …
如图,C为射线AB上一点,AB=30,AC比BC的多5,P,Q两点分别从A,B两点同时出发.分别以 2020-07-24 …
如图中(1)、(2)、…(m)分别是边长均大于2的三角形、四边形、…、凸n边形.分别以它们的各顶点 2020-07-25 …
阅读材料,回答问题。材料一荀子说“人之所以异于禽兽者,以其能群也”,“人何以能群?曰:分(指差异性 2020-07-29 …
如图1,图2…、图m是边长均大于2的三角形、四边形、…、凸n边形.分别以它们的各顶点为圆心,以1为 2020-07-30 …
(2012•达州)数学课上,探讨角平分线的作法时,李老师用直尺和圆规作角平分线,方法如下:作法:如图 2020-11-06 …
观察复式统计表并回答问题.下面是三年级某班本学期体检视力统计表.4.2以下4.3~4.64.7~4. 2020-11-07 …