早教吧作业答案频道 -->化学-->
碳酸镁晶须是一种新型的吸波隐形材料中的增强材料.(1)合成该物质的步骤如下:步骤1:配制0.5mol•L-1MgSO4溶液和0.5mol•L-1NH4HCO3溶液.步骤2:用量筒量取500mLNH4HCO3溶液于1000mL三口烧瓶中
题目详情
碳酸镁晶须是一种新型的吸波隐形材料中的增强材料.
(1)合成该物质的步骤如下:
步骤1:配制0.5mol•L-1MgSO4溶液和0.5mol•L-1NH4HCO3溶液.
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三口烧瓶中,开启搅拌器.温度控制在50℃.
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5.
步骤4:放置1h后,过滤、洗涤.
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3•nH2O n=1~5).
回答下列问题:
①步骤2控制温度在50℃,较好的加热方法___;
②步骤3生成MgCO3•nH2O沉淀的离子方程式___;
③步骤4检验是否洗涤干净的方法是___;
(2)测定合成的MgCO3•nH2O中的n值.称量1.000 g碳酸镁晶须,放入如图所示的广口瓶中加入水滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,反应后期将温度升到30℃,最后的烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次.
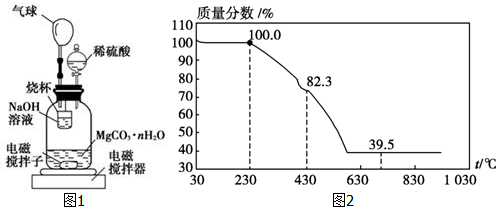
①图1中气球的作用是___.
②上述反应后期要升温到30℃,主要目的是___.
③用已知浓度的盐酸滴定烧杯中的溶液时应选用___为指示剂,若盛放盐酸的滴定管在滴定前有气泡未排尽,滴定后无气泡(其他操作均正确),则所测CO2的量会___(填“偏大”“偏小”“无影响”)
④设3次实验测得每1.000g碳酸镁晶须与稀硫酸反应产生的CO2平均值为a mol,则n值为___(用含a的表达式表示).
(3)称取100g上述晶须产品进行热重分析,热重曲线如图2.则该条件下合成的晶须中,n=___(选填1、2、3、4、5).
(1)合成该物质的步骤如下:
步骤1:配制0.5mol•L-1MgSO4溶液和0.5mol•L-1NH4HCO3溶液.
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三口烧瓶中,开启搅拌器.温度控制在50℃.
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5.
步骤4:放置1h后,过滤、洗涤.
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3•nH2O n=1~5).
回答下列问题:
①步骤2控制温度在50℃,较好的加热方法___;
②步骤3生成MgCO3•nH2O沉淀的离子方程式___;
③步骤4检验是否洗涤干净的方法是___;
(2)测定合成的MgCO3•nH2O中的n值.称量1.000 g碳酸镁晶须,放入如图所示的广口瓶中加入水滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,反应后期将温度升到30℃,最后的烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次.

①图1中气球的作用是___.
②上述反应后期要升温到30℃,主要目的是___.
③用已知浓度的盐酸滴定烧杯中的溶液时应选用___为指示剂,若盛放盐酸的滴定管在滴定前有气泡未排尽,滴定后无气泡(其他操作均正确),则所测CO2的量会___(填“偏大”“偏小”“无影响”)
④设3次实验测得每1.000g碳酸镁晶须与稀硫酸反应产生的CO2平均值为a mol,则n值为___(用含a的表达式表示).
(3)称取100g上述晶须产品进行热重分析,热重曲线如图2.则该条件下合成的晶须中,n=___(选填1、2、3、4、5).
▼优质解答
答案和解析
(1)①加热温度低于100°C需要水域加热控制温度,
故答案为:水浴加热;
②将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,用氨水调节溶液pH到9.5,反应生成碳酸镁结晶水合物,反应的化学方程式为Mg2++HCO3-+NH3•H2O+(n-1)H2O═MgCO3•nH2O+NH4+,
故答案为:Mg2++HCO3-+NH3•H2O+(n-1)H2O═MgCO3•nH2O+NH4+;
③步骤4检验沉淀已经洗涤干净的方法是取最后一次洗涤的滤出液,滴入盐酸酸化的BaCl2溶液,若无沉淀说明已洗涤干净,
故答案为:取最后一次洗涤的滤出液,滴入盐酸酸化的BaCl2溶液,若无沉淀说明已洗涤干净;
(2)①装置中气球可以缓冲压强并封闭装置,
故答案为:缓冲压强并封闭体系;
②反应后期将温度升到30℃,使生成的二氧化碳全部逸出后被氢氧化钠溶液吸收,减少测定产生的误差,
故答案为:使广口瓶内水中溶解的CO2充分逸出,并被NaOH充分吸收;
③用已知浓度的盐酸滴定烧杯中的溶液,主要是测定溶液没有反应的氢氧化钠,所以指示剂用酚酞,若盛放盐酸的滴定管在滴定前有气泡未排尽,滴定后无气泡,传导致读出的盐酸的体积偏大,所以测出的氢氧化钠的物质的量会偏大,从而会使测CO2的量会偏小,
故答案为:酚酞;偏小;
④实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,依据元素守恒可知,碳酸镁物质的量为amol,根据化学式可知,MgCO3•nH2O中碳酸镁晶体中碳酸镁和结晶水物质的量之比为1:n,得到1:n=a:
;得到n=
,
故答案为:
;
(3)MgCO3•nH2O n=1~5,分析图象400°C剩余质量为82.3g,为失去结晶水的质量,剩余质量为39.2g是碳酸镁分解失去二氧化碳的质量,得到100g×
=100-82.3,
n=1,
故答案为:1.
故答案为:水浴加热;
②将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,用氨水调节溶液pH到9.5,反应生成碳酸镁结晶水合物,反应的化学方程式为Mg2++HCO3-+NH3•H2O+(n-1)H2O═MgCO3•nH2O+NH4+,
故答案为:Mg2++HCO3-+NH3•H2O+(n-1)H2O═MgCO3•nH2O+NH4+;
③步骤4检验沉淀已经洗涤干净的方法是取最后一次洗涤的滤出液,滴入盐酸酸化的BaCl2溶液,若无沉淀说明已洗涤干净,
故答案为:取最后一次洗涤的滤出液,滴入盐酸酸化的BaCl2溶液,若无沉淀说明已洗涤干净;
(2)①装置中气球可以缓冲压强并封闭装置,
故答案为:缓冲压强并封闭体系;
②反应后期将温度升到30℃,使生成的二氧化碳全部逸出后被氢氧化钠溶液吸收,减少测定产生的误差,
故答案为:使广口瓶内水中溶解的CO2充分逸出,并被NaOH充分吸收;
③用已知浓度的盐酸滴定烧杯中的溶液,主要是测定溶液没有反应的氢氧化钠,所以指示剂用酚酞,若盛放盐酸的滴定管在滴定前有气泡未排尽,滴定后无气泡,传导致读出的盐酸的体积偏大,所以测出的氢氧化钠的物质的量会偏大,从而会使测CO2的量会偏小,
故答案为:酚酞;偏小;
④实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,依据元素守恒可知,碳酸镁物质的量为amol,根据化学式可知,MgCO3•nH2O中碳酸镁晶体中碳酸镁和结晶水物质的量之比为1:n,得到1:n=a:
| 1.000g-84ag |
| 18g/mol |
| (1-84a) |
| 18a |
故答案为:
| (1-84a) |
| 18a |
(3)MgCO3•nH2O n=1~5,分析图象400°C剩余质量为82.3g,为失去结晶水的质量,剩余质量为39.2g是碳酸镁分解失去二氧化碳的质量,得到100g×
| 18n |
| 18n+84 |
n=1,
故答案为:1.
看了碳酸镁晶须是一种新型的吸波隐形...的网友还看了以下:
如图所示,O为杠杆MN的支点,OM:ON=3:4,物块A和B分别挂在M、N两端,杠杆恰好平衡,已知 2020-05-13 …
某有机物中所含C、O、H元素的质量比是6:4:1.该有机物蒸汽对空气的相对密度为1、518.求该有 2020-05-15 …
抛物线y=ax2+bx+c的顶点为C(1,1),且过原点O,过抛物线上一点P(x,y)向直线y=4 2020-05-16 …
1.6g的可燃物在足量的氧气中燃烧,生成4.4g的二氧化碳和3.6g的水,则关于可燃物的下列判断, 2020-05-16 …
如图所示,物体自O点由静止开始作匀加速直线运动,A、B、C、D为其轨道上的四点,测得AB=2m,B 2020-07-31 …
某花铺摆放的一组花盆图案(O代表玫瑰花盆,△代表菊花花盆)(1)△:4个O:1个(2)△:8个O: 2020-08-01 …
已知抛物线y=ax2+bx+c(a≠0)顶点为C(1,1)且过原点O.过抛物线上一点P(x,y)向 2020-08-02 …
1章节因生病所以缺了这堂课,所以求大家简要的概括一下这一章节的内容:4.1物质在溶解过程中有能量变化 2020-11-05 …
o(∩∩)o...会么有一个物块在空气中称时重力为29.4牛,浸没在水里弹簧测力计读数为19.6牛, 2020-11-08 …
4分之一+8分之3-11分之5那37+(3/4-1/3)1/2-(1/4-1/8)4/5+7/10- 2020-12-17 …