早教吧作业答案频道 -->化学-->
在固定容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g)随温度升高,混合气体的颜色变深.回答下列问题:(1)反应的△H0(填“大于”“小于”);100℃时,体系
题目详情
在固定容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g)随温度升高,混合气体的颜色变深.回答下列问题:
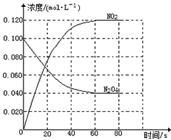
(1)反应的△H___0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为___.
反应的平衡常数K1=___.
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)降低,经10s又达到平衡.
①T___100℃(填“大于”“小于”),判断理由是___.
②100℃时达到平衡后,向容器中再充入0.20mol NO2气体,新平衡建立后,NO2的体积分数
___(填“增大”、“不变”或“减小”)
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___(填“正反应”或“逆反应”)方向移动,判断理由是___.

(1)反应的△H___0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为___.
反应的平衡常数K1=___.
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)降低,经10s又达到平衡.
①T___100℃(填“大于”“小于”),判断理由是___.
②100℃时达到平衡后,向容器中再充入0.20mol NO2气体,新平衡建立后,NO2的体积分数
___(填“增大”、“不变”或“减小”)
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___(填“正反应”或“逆反应”)方向移动,判断理由是___.
▼优质解答
答案和解析
(1)随温度的升高,混合气体的颜色变深,说明升高温度平衡正向移动,则正反应为吸热反应,即△H>0;
0~60s时段,N2O4浓度变化为:0.1mol/L-0.04mol/L=0.06mol/L,v(N2O4)=
=0.0010mol•L-1•s-1;
由图可知,平衡时c(NO2)=0.120mol•L-1、c(N2O4)=0.040mol•L-1,故K=
=0.36,
故答案为:大于;0.0010mol•L-1•s-1;0.36;
(2)①改变温度后,N2O4的浓度降低,平衡向正反应方向移动,由于正反应吸热反应,升高温度平衡正向移动,故T>100℃,
故答案为:大于;改变温度后,N2O4的浓度降低,平衡向正反应方向移动,正反应为吸热反应,故温度升高;
②100℃时达到平衡后,向容器中再充入0.20mol NO2气体,等效为在原平衡的基础上增大压强,平衡逆向移动,新平衡建立后,NO2的体积分数减小,
故答案为:减小;
(3)温度T时反应达平衡后,将反应容器的容积减少一半,压强增大,正反应是气体分子数增大的反应,增大压强平衡向逆反应方向移动,
故答案为:逆反应;正反应是气体分子数增大的反应,增大压强平衡向逆反应方向移动.
0~60s时段,N2O4浓度变化为:0.1mol/L-0.04mol/L=0.06mol/L,v(N2O4)=
| 0.06mol/L |
| 60s |
由图可知,平衡时c(NO2)=0.120mol•L-1、c(N2O4)=0.040mol•L-1,故K=
| 0.122 |
| 0.04 |
故答案为:大于;0.0010mol•L-1•s-1;0.36;
(2)①改变温度后,N2O4的浓度降低,平衡向正反应方向移动,由于正反应吸热反应,升高温度平衡正向移动,故T>100℃,
故答案为:大于;改变温度后,N2O4的浓度降低,平衡向正反应方向移动,正反应为吸热反应,故温度升高;
②100℃时达到平衡后,向容器中再充入0.20mol NO2气体,等效为在原平衡的基础上增大压强,平衡逆向移动,新平衡建立后,NO2的体积分数减小,
故答案为:减小;
(3)温度T时反应达平衡后,将反应容器的容积减少一半,压强增大,正反应是气体分子数增大的反应,增大压强平衡向逆反应方向移动,
故答案为:逆反应;正反应是气体分子数增大的反应,增大压强平衡向逆反应方向移动.
看了在固定容积为1.00L的容器中...的网友还看了以下:
(1)在标准状况下,200mL某气体的质量为1.142g,该气体的摩尔质量为(2)已知某种混盐中含 2020-05-02 …
某KCl、MgCl2、Mg(NO3)2形成的混合中,c(K+)=0.1mol/L,c(Mg2+)= 2020-05-13 …
计算25℃时下列溶液的pH:(1)1mLpH=2的H2SO4加水稀释至100mL;(2)0.01m 2020-05-17 …
已知C20混凝土的实验室配合比为1:2.52:2.22:0.62(水泥:砂:石:氺),每立方米混凝 2020-06-29 …
PH混=PH小+0.3和PH混=PH大-0.3怎么来的?再问多个问题25度时,PH=1的盐酸和PH 2020-07-08 …
在250ml某混合溶液中HNO3和硫酸的量浓度分别是0.2和0.1,加入1.92克铜粉,加热反应写 2020-07-08 …
2中0×250÷259h÷72h0-地925×4072÷中个9×245×2地0÷h中 2020-07-19 …
用Γ函数表示下列积分:(1)∫(0,+∞)e^[-(x^n]dx(n>0)(2)∫(0,1)[ln 2020-07-26 …
(1)等质量的CH4、C3H8、C2H4、C2H2四种烃完全燃烧,消耗氧气最多的是;(2)两种气态烃 2020-11-27 …
将对H2相对密度为3.6的N2与H2组成的混合气0.5mol通入一恒容密闭容器中,一定条件下发生反应 2021-01-09 …