早教吧作业答案频道 -->化学-->
过氧化钠常作漂白剂、杀菌剂、消毒剂.过氧化钠保存不当容易吸收空气中CO2而变质.(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入溶液,充分振荡
题目详情
过氧化钠常作漂白剂、杀菌剂、消毒剂.过氧化钠保存不当容易吸收空气中CO2而变质.
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入___溶液,充分振荡后有白色沉淀,证明Na2O2已经变质.
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数.
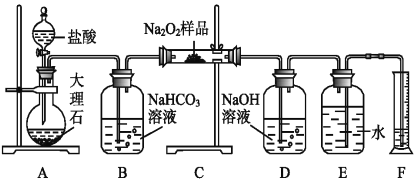
①A中发生反应离子方程式为___.
②将仪器连接好以后,必须进行的第一步操作是___.
③B装置出来的气体是否需要干燥___.(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式___,___.
⑤D中NaOH溶液的作用___.
⑥实验结束时,读取实验中生成气体的体积时,不合理的是___.
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为___.
⑧实验完成后E到F之间导管内残留水的体积会使测量结果___.(填“偏大”、“偏小”或“不影响”)
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入___溶液,充分振荡后有白色沉淀,证明Na2O2已经变质.
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数.

①A中发生反应离子方程式为___.
②将仪器连接好以后,必须进行的第一步操作是___.
③B装置出来的气体是否需要干燥___.(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式___,___.
⑤D中NaOH溶液的作用___.
⑥实验结束时,读取实验中生成气体的体积时,不合理的是___.
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为___.
⑧实验完成后E到F之间导管内残留水的体积会使测量结果___.(填“偏大”、“偏小”或“不影响”)
▼优质解答
答案和解析
(1)过氧化钠在空气中变质会最后生成碳酸钠固体,探究一包过氧化钠样品是否已经变质,可以利用碳酸根离子和钡离子结合生成碳酸钡白色沉淀证明Na2O2已经变质,取少量样品,溶解,加入CaCl2或BaCl2溶液,充分振荡后有白色沉淀,证明Na2O2已经变质,
故答案为:CaCl2或BaCl2溶液;
(2)装置图中A为生成二氧化碳的装置,B为洗气装置,吸收二氧化碳中混有的HCl,防止HCl与过氧化钠反应,C为二氧化碳与过氧化钠反应的装置,D为吸收多余的二氧化碳的装置,防止多余的二氧化碳进入量气装置,导致测得的氧气的体积偏大,E和F是测量生成氧气的体积的装置;
①A中发生反应是碳酸钙和盐酸反应生成二氧化碳、水和氯化钙,反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
②实验探究测定方法是测定二氧化碳和过氧化钠反应生成的氧气,装置中必须是气密性完好,将仪器连接好以后,必须进行的第一步操作是检查装置的气密性;
故答案为:检查装置的气密性;
③B装置出来的气体不需要干燥,二氧化碳、水蒸气和过氧化钠反应生成碳酸钠和氧气的反应,反应的化学方程式为:2CO2+2Na2O2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,过氧化钠反应生成氧气的物质的量定量关系相同对测定过氧化钠质量分数无影响,所以不需要干燥出去水蒸气,
故答案为:否;
④装置C中是二氧化碳、水蒸气和过氧化钠反应生成碳酸钠和氧气的反应,反应的化学方程式为:2CO2+2Na2O2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2CO2+2Na2O2=2Na2CO3+O2; 2Na2O2+2H2O=4NaOH+O2↑;
⑤D为吸收多余的二氧化碳的装置,防止多余的二氧化碳进入量气装置,导致测得的氧气的体积偏大,
故答案为:吸收未反应的CO2;
⑥a.直接读取气体体积,不冷却到室温,会使溶液体积增大,读出结果产生误差,故a不正确;
b.调整量筒内外液面高度使之相同,使装置内压强和外界压强相同,避免读取体积产生误差,故b正确;
c.视线与凹液面的最低点相平读取量筒中水的体积是正确的读取方法,故c正确;
故答案为:a;
⑦测定出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,物质的量=
,则样品中过氧化钠的质量分数为=
×100%=
%;
故答案为:
%;
⑧实验完成后E到F之间导管内残留水的体积会使测定氧气体积减小,导致测定过氧化钠质量分数测量结果偏小,故答案为:偏小.
故答案为:CaCl2或BaCl2溶液;
(2)装置图中A为生成二氧化碳的装置,B为洗气装置,吸收二氧化碳中混有的HCl,防止HCl与过氧化钠反应,C为二氧化碳与过氧化钠反应的装置,D为吸收多余的二氧化碳的装置,防止多余的二氧化碳进入量气装置,导致测得的氧气的体积偏大,E和F是测量生成氧气的体积的装置;
①A中发生反应是碳酸钙和盐酸反应生成二氧化碳、水和氯化钙,反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
②实验探究测定方法是测定二氧化碳和过氧化钠反应生成的氧气,装置中必须是气密性完好,将仪器连接好以后,必须进行的第一步操作是检查装置的气密性;
故答案为:检查装置的气密性;
③B装置出来的气体不需要干燥,二氧化碳、水蒸气和过氧化钠反应生成碳酸钠和氧气的反应,反应的化学方程式为:2CO2+2Na2O2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,过氧化钠反应生成氧气的物质的量定量关系相同对测定过氧化钠质量分数无影响,所以不需要干燥出去水蒸气,
故答案为:否;
④装置C中是二氧化碳、水蒸气和过氧化钠反应生成碳酸钠和氧气的反应,反应的化学方程式为:2CO2+2Na2O2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2CO2+2Na2O2=2Na2CO3+O2; 2Na2O2+2H2O=4NaOH+O2↑;
⑤D为吸收多余的二氧化碳的装置,防止多余的二氧化碳进入量气装置,导致测得的氧气的体积偏大,
故答案为:吸收未反应的CO2;
⑥a.直接读取气体体积,不冷却到室温,会使溶液体积增大,读出结果产生误差,故a不正确;
b.调整量筒内外液面高度使之相同,使装置内压强和外界压强相同,避免读取体积产生误差,故b正确;
c.视线与凹液面的最低点相平读取量筒中水的体积是正确的读取方法,故c正确;
故答案为:a;
⑦测定出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,物质的量=
| V×10-3L |
| 22.4L/mol |
| ||
| ag |
| 39V |
| 56a |
故答案为:
| 39V |
| 56a |
⑧实验完成后E到F之间导管内残留水的体积会使测定氧气体积减小,导致测定过氧化钠质量分数测量结果偏小,故答案为:偏小.
看了过氧化钠常作漂白剂、杀菌剂、消...的网友还看了以下:
高中化学选修4相关内容是否只有难溶物才存在溶解平衡?易溶物质存在溶解平衡吗?溶解方程式是吸热还是放 2020-05-13 …
某同学探究溶液的酸碱性对FeCl3水解平衡的影响,实验方案如下:配制50mL0.001mol/LF 2020-05-17 …
1.用图表示糖或高锰酸钾在水中的溶解过程.2.我关于其它溶解问题的研究.问1.用图表示糖或高锰酸钾 2020-07-05 …
为了探究“淀粉溶液遇碘(I2)的显色反应”,经查阅资料得知:常温下,淀粉溶液检验碘的反应灵敏度极高 2020-07-20 …
仔细阅读下面的探究实验信息,回答相关问题.Ⅰ.实验目的探究溶解过程中,溶液温度的变化情况.Ⅱ.查阅 2020-07-29 …
同学甲和乙在完成加热条件下Cu与过量H2SO4(浓)反应实验时,预测反应后溶液为蓝色,但实际反应后发 2020-11-28 …
某强酸溶液X中可能含有NH4+、Fe2+、Al3+、CO32-、SO42-、Cl-、NO3-中的若干 2020-12-04 …
PbSO4溶于较浓的盐酸,而BaSO4不溶?而且据说PbSO4溶于较浓的NaOH溶液PbSO4溶于较 2021-01-04 …
镁和铝都是比较活泼的金属,下列叙述正确的是()①镁易与热水反应,而铝难与热水反应②镁溶于碱溶液,而铝 2021-01-10 …
如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电能力的关系装置图.首先在水槽中加入200mL2m 2021-01-13 …