常温下,取浓度均为0.01mol•L-1的HA溶液和MOH溶液各20mL,分别用0.01mol•L-1NaOH溶液、0.01mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是(
常温下,取浓度均为0.01mol•L-1的HA溶液和MOH溶液各20mL,分别用0.01mol•L-1NaOH溶液、0.01mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )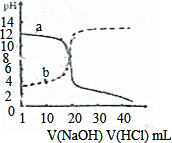
A. HA和MOH均为弱电解质
B. 曲线a中,滴加溶液到20mL时,c(Cl-)=c(M+)=c(OH-)=c(H+)
C. 曲线b中,滴加溶液到20mL时,c(Na+)>c(A-)>c(OH-)>c(H+)
D. 曲线b中,滴加溶液到10mL时,c(A-)+c(OH-)=c(H+)+c(HA)
已知向量a=(2,1),b=(x,y).(1)若x∈{-1,0,1,2},y∈{-1,0,1},求向 2020-03-30 …
求一数列.高2.a(n+1)=2an/2an+1已知a1=1a(n+1)=2an/2an+1求数列 2020-04-25 …
S=(1+1/1*2+(2+1/2*3)+(3+1/3*4)+...+(20+1/20*21)S= 2020-04-27 …
设函数f(x)=(2^x)/(1+2^x)-1/2,[x]表示不超过x的最大整数,则函数y=[f( 2020-04-27 …
设函数f(x)=(1+1/n)的n次方(n∈正整数,n大于1,x∈r)1,对于任意x,证明(f(2 2020-05-14 …
几道数学计算题(请写过程)第一题1/2+(1/3+2/3)+(1/4+2/4+3/4)+…+(1/ 2020-05-16 …
2^2-1^2=2*1+13^2-2^2=2*2+14^2-3^2=2*3+1……(n+1)^2- 2020-05-19 …
1.7/x²-1+8/x²-2x=37-9x/x^3-x²-x+12.3/x²+x-2=x/x-1 2020-07-18 …
(1)已知a+b=-c,则a(1/a+1/b)+b(1/a+1/c)+c(1/a+1/b)的值是多少 2020-10-31 …
计算一道数学题,(1+1/2)×(1+1/3)×(1+1/4)×(1+1/5)×(1+1/6)×(1 2020-11-30 …