早教吧作业答案频道 -->化学-->
C、Be、Cl、Fe等元素及其化合物有重要的应用.(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为(填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl2
题目详情
C、Be、Cl、Fe等元素及其化合物有重要的应用.
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为___(填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl2应与___(填MgCl2或AlCl3)化学性质更相似.
(2)上述四种元素的原子中,未成对电子数最多的元素是___.
(3)①试根据原子核外电子排布所遵循的原理解释Fe2+具有较的强还原性,易被氧化为Fe3+的原因___.
②当然Fe3+也有氧化性,在印刷行业中就用氯化铁溶液腐蚀铜板,写出离子方程式___.
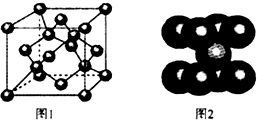
(4)一定条件下,C元素可形成多种晶体.图1是其中某种晶体的一个晶胞,该晶胞中含有___个C原子.
(5)图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol-1,该晶体的密度为a g•cm-3,NA为阿伏加德罗常数的值,则该晶胞的体积为___cm3.

(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为___(填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl2应与___(填MgCl2或AlCl3)化学性质更相似.
(2)上述四种元素的原子中,未成对电子数最多的元素是___.
(3)①试根据原子核外电子排布所遵循的原理解释Fe2+具有较的强还原性,易被氧化为Fe3+的原因___.
②当然Fe3+也有氧化性,在印刷行业中就用氯化铁溶液腐蚀铜板,写出离子方程式___.
(4)一定条件下,C元素可形成多种晶体.图1是其中某种晶体的一个晶胞,该晶胞中含有___个C原子.
(5)图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol-1,该晶体的密度为a g•cm-3,NA为阿伏加德罗常数的值,则该晶胞的体积为___cm3.
▼优质解答
答案和解析
(1)Be的电负性是1.5,Cl的电负性是3.0,△x=1.5<1.7,所以为共价化合物,铍元素和铝元素在周期表中的对角线的位置,根据对角线规则 可知,铍和铝的性质相似,所以BeCl2与 AlCl3的化学性质相似,
故答案为:共价;AlCl3;
(2)上述四种元素的原子中,C的未成对电子数为2,Be的未成对电子数为2,Cl的未成对电子数为1,Fe的未成对电子数为4,所以四种元素的原子中,未成对电子数最多的元素是Fe,
故答案为:Fe;
(3)①Fe2+的外围电子排布为3d6,Fe3+的外围电子排布为3d5,3d5是一种半充满结构,也是一种稳定结构,所以Fe2+具有较的强还原性,易被氧化为Fe3+,故答案为:Fe2+的外围电子排布为3d6,当失去一个电子后变成3d5的半充满结构的Fe3+,较稳定;
②用氯化铁溶液腐蚀铜板,铁离子与铜反应生成亚铁离子和铜离子,反应的离子方程式为2Fe3++Cu═2Fe2++Cu2+,
故答案为:2Fe3++Cu═2Fe2++Cu2+;
(4)根据均摊法可知,晶胞中含有C原子数为4+8×
+6×
=8,
故答案为:8;
(5)图2为金属铁某种晶体的晶胞结构,由晶胞的结构图可知,每个晶胞中含有的铁原子数为1+8×
=2,根据ρ=
可知,V=
=
,
故答案为:
.
故答案为:共价;AlCl3;
(2)上述四种元素的原子中,C的未成对电子数为2,Be的未成对电子数为2,Cl的未成对电子数为1,Fe的未成对电子数为4,所以四种元素的原子中,未成对电子数最多的元素是Fe,
故答案为:Fe;
(3)①Fe2+的外围电子排布为3d6,Fe3+的外围电子排布为3d5,3d5是一种半充满结构,也是一种稳定结构,所以Fe2+具有较的强还原性,易被氧化为Fe3+,故答案为:Fe2+的外围电子排布为3d6,当失去一个电子后变成3d5的半充满结构的Fe3+,较稳定;
②用氯化铁溶液腐蚀铜板,铁离子与铜反应生成亚铁离子和铜离子,反应的离子方程式为2Fe3++Cu═2Fe2++Cu2+,
故答案为:2Fe3++Cu═2Fe2++Cu2+;
(4)根据均摊法可知,晶胞中含有C原子数为4+8×
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:8;
(5)图2为金属铁某种晶体的晶胞结构,由晶胞的结构图可知,每个晶胞中含有的铁原子数为1+8×
| 1 |
| 8 |
| ||
| V |
| 2M |
| aNA |
| 112 |
| aNA |
故答案为:
| 112 |
| aNA |
看了 C、Be、Cl、Fe等元素及...的网友还看了以下:
偿还期在一年内或超过一年的一个营业周期内的企业债务称为( )。A.短期负债B.短期借款C.流动负债D 2020-05-21 …
进出口长期为负值的国家,对外投资必然会增加其国际资产,最终会成为债权 国。( ) 2020-05-30 …
单项选择题1.下列肯定会引起所有者权益总额怎家的情况是()A.资产与负债同增B.资产与负债同减C. 2020-06-20 …
设D={(x,y)|x2+y2≤R2,R>0},则二重积∬D(eλrcosθ−eλrsinθ)rd 2020-07-19 …
通电螺旋管旁的小磁针静止如图所示,判断正确的是()A.螺旋管a端为N极,电源C端为正极B.螺旋管a 2020-07-29 …
两个数相加,如果和比每个加数都小,那么这两个数是()A.异号B.同为正C.同为负D.0和负数 2020-07-30 …
通电螺旋管旁的小磁针静止如图所示,判断正确的是()A.螺旋管a端为N极,电源c端为正极B.螺旋管a端 2020-11-01 …
基期为负值,报告期为正值是,计算公式如何设置通用的增幅公式?同比,通常是和去年同期相比,今年称为报告 2020-11-27 …
高二物理电荷ABC三点在同一直线,依次排布.各点都有一个电荷,他们所带电荷相等,A.B为正电荷,C点 2021-01-05 …
第一题:如果两个数的积为负数,和为正数,则两个数()A均为正数B一正一负,且负数的绝对值大于正数的绝 2021-01-22 …