早教吧作业答案频道 -->化学-->
1915年诺贝尔物理学奖授予HenryBragg和LawrenceBragg,以表彰他们用X射线对晶体结构的分析所作的贡献.(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据
题目详情
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是___,Na、Mg、Al第一电离能I1从小到大的排列顺序是___.
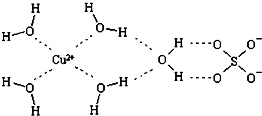
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示.
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是___.
②SO42-中S原子的杂化类型是___,与其互为等电子体的分子有___(任写一种).
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有___(填序号).
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式___;金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是___g/cm3(列出计算式).

(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示.
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是___.
②SO42-中S原子的杂化类型是___,与其互为等电子体的分子有___(任写一种).
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有___(填序号).
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式___;金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是___g/cm3(列出计算式).
▼优质解答
答案和解析
(1)离子半径Mg2++2-2+-;离子电荷数Na+=Cl-2-=Mg2+=Ca2+,离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl,
同周期从左到右第一电离能增大,但是第IIA与IIIA族、第VA与VIA族反常,则第一电离能I从小到大的排列顺序是Na、Al、Mg;
故答案为:MgO>CaO>NaCl>KCl;Na、Al、Mg;
(2)①因为水分子间存在氢键,氢键会使水分子成为缔合水分子,使得体积变小,所以用蒸汽密度法测得的H2O的相对分子质量比理论计算出来的相对分质量较大,
故答案为:水分子间有氢键发生缔合作用;
②SO42-中S的价电子对数=
=4,形成四条杂化轨道,S原子的杂化方式为sp3,具有相同原子数和价电子数的微粒互称为等电子体,所以与SO42-互为等电子体的微粒有SiCl4等;
故答案为:sp3;CCl4(SiCl4)等;
③)①[Cu(NH3)4]2+中Cu2+与NH3之间的化学键为配位键,N-H为极性共价键,
故答案为:AC;
④铜为29号元素,其原子外围电子排布式为3d104s1,根据均摊法计算出晶胞中铜原子数为8×
+6×
=4,Cu原子的半径为r pm,则晶胞的边长为2
r pm,晶胞的体积为(2
r×10-10)3cm3,所以铜的密度ρ=
=
g/cm3=
g/cm3,
故答案为:3d104s1;
.
同周期从左到右第一电离能增大,但是第IIA与IIIA族、第VA与VIA族反常,则第一电离能I从小到大的排列顺序是Na、Al、Mg;
故答案为:MgO>CaO>NaCl>KCl;Na、Al、Mg;
(2)①因为水分子间存在氢键,氢键会使水分子成为缔合水分子,使得体积变小,所以用蒸汽密度法测得的H2O的相对分子质量比理论计算出来的相对分质量较大,
故答案为:水分子间有氢键发生缔合作用;
②SO42-中S的价电子对数=
| 6+2 |
| 2 |
故答案为:sp3;CCl4(SiCl4)等;
③)①[Cu(NH3)4]2+中Cu2+与NH3之间的化学键为配位键,N-H为极性共价键,
故答案为:AC;
④铜为29号元素,其原子外围电子排布式为3d104s1,根据均摊法计算出晶胞中铜原子数为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 2 |
| 2 |
| m |
| V |
| ||
(2
|
| 4M | ||
NA(2
|
故答案为:3d104s1;
| 4M | ||
NA(2
|
看了 1915年诺贝尔物理学奖授予...的网友还看了以下:
下列格式中能用完全平方公式分解因式的是?A、(x+y)(y-x)-4xyB、a^2-2ab+4b^2 2020-03-31 …
关于反应K37ClO3+6H35Cl═KCl+3Cl2↑+3H2O的有关叙述中,正确的是()A.K 2020-05-20 …
●下列光盘格式中,能支持多次擦除重写数据的是(43)。(43) A.DVD-R B.CD-R C.D 2020-05-26 …
如图所示,歼击机的“稳定盘旋过载”指的是歼击机做水平盘旋时的加速度,这个参数越大,表明战机近距离格斗 2020-11-02 …
正方形网格中的交点,我们称之为格点.如图所示的网格图中,每个小正方形的边长都为1.现有格点A、B,那 2020-12-25 …
随着当今世界多极化趋势的发展,各国在世界格局中能够占据有利地位的决定性因素是()A.外交策略B.综合 2021-01-04 …
随着世界多极化趋势的发展,各国在世界格局中能够占据有利地位的决定性因素是()A.非集团政策B.外交策 2021-01-04 …
随着世界多极化趋势的发展,各国在世界格局中能够占据有利地位的决定性作用的是()A.非集团政策B.外交 2021-01-04 …
实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等。因而 2021-02-05 …
实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等.因而 2021-02-05 …