加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下性质稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工
加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下性质稳定,加热至 560 ℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
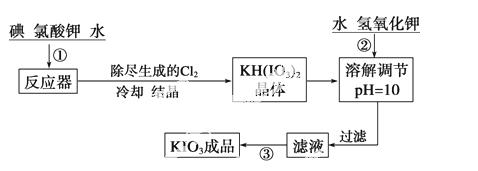
(1) 已知步骤 ① 反应器发生的反应中,单质碘和氯酸钾的物质的量之比为 6 ∶ 11 ,则反应器中发生反应的化学方程式为
_____________________________________________________________________ 。
(2) 步骤 ② 中调节 pH = 10 的目的是 _______________________________________ 。
参照碘酸钾的溶解度:
| 温度 / ℃ | 20 | 40 | 60 | 80 |
| KIO 3 g/100 g H 2 O | 8.08 | 12.6 | 18.3 | 24.8 |
操作 ③ 的方法是 _____________________________________________________ 。
(3) 检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应,然后用四氯化碳检验生成的碘单质时,甲应观察到的明显现象有 _______________________________________________________________________ 。
学生乙对纯净的 NaCl 进行了如下实验:取 1 g 纯净的 NaCl ,加 3 mL 水配成溶液,然后滴入 5 滴淀粉溶液和 1 mL 0.1 mol·L - 1 KI 溶液,振荡,溶液无变化,然后再滴入 1 滴 1 mol·L - 1 的 H 2 SO 4 ,振荡,一段时间后溶液变浅蓝色。请推测实验中产生蓝色现象的可能原因,用离子方程式表示
______________________________________________________________________ 。
(4) 学生丙查阅有关食品碘强化剂的资料后知道,碘酸钙也是一种允许使用的食品碘强化剂,它是一种白色结晶或结晶性粉末,难溶于水和乙醇。丙同学在氯化钙溶液中加入理论量的碘酸钾溶液,反应生成的沉淀经水洗后,室温下干燥得碘酸钙晶体,加热至 160 ~ 540 ℃变成无水物,此时固体质量为原晶体质量的 78.3% ,写出制备碘酸钙晶体的离子方程式: _________________________________________________ ;
检验沉淀已经洗涤干净的方法是 _________________________________________ 。

下列关于晶体结构和性质的叙述中,错误的是A.分子晶体中一定存在共价键B.原子晶体中一定存在共价键C 2020-04-09 …
下列关于三聚氰胺的性质中,属于化学性质的是()A.在高温下能分解成氰化物和氮气B.密度为1.573 2020-05-13 …
关于物质的变化和性质的1.二氧化碳在下列变化中只发生物理变化的是(C)A溶于江、河、湖水中 B被石 2020-05-16 …
下列有关物质性质的判断正确的是()A.熔点:SiO2<CO2B.沸点:H2O<H2SC.晶格能:C 2020-05-17 …
下列有关物质性质的应用正确的是A.浓硫酸铵溶液能使蛋白质聚沉,可用来消毒杀菌B.二氧化硅晶体具有高 2020-06-21 …
下列晶体性质的比较中,正确的是()A.熔点:金刚石>晶体硅>碳化硅B.熔点:SiI4>SiBr4> 2020-06-26 …
1.单质硅有硅和硅两种.晶体硅的结构与相似,物理性质有.晶体硅是良好的材料;硅是人类将能转换能的常 2020-07-06 …
各种晶体物质的熔沸点的比较原子晶体、离子晶体、分子晶体、金属晶体的物理和化学性质的比较 2020-07-06 …
一定温度下,取某物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半.给另 2020-07-08 …
准晶体可能具有下列性质,其中属于化学性质的是()A.密度低B.抗氧化性强C.导电性差D.耐磨损 2020-07-12 …