早教吧作业答案频道 -->化学-->
老师拿出一瓶没有瓶盖的氢氧化钠固体取出50g样品实验如图,请同学们进行分析:(如图所示)(1)计算50g样品中氢氧化钠的质量分数;(2)分析氢氧化钠变质的原因(3)若要提纯这瓶
题目详情
老师拿出一瓶没有瓶盖的氢氧化钠固体取出50g样品实验如图,请同学们进行分析:(如图所示)
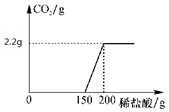
(1)计算50g样品中氢氧化钠的质量分数;
(2)分析氢氧化钠变质的原因___
(3)若要提纯这瓶氢氧化钠,可以采取的方法是___.

(1)计算50g样品中氢氧化钠的质量分数;
(2)分析氢氧化钠变质的原因___
(3)若要提纯这瓶氢氧化钠,可以采取的方法是___.
▼优质解答
答案和解析
(1)由图象可知,与碳酸钠反应的稀盐酸的质量为:200g-150g=50g;
设50g的稀盐酸中溶质的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 44
x 2.2g
=
解得:x=3.65g
稀盐酸中溶质的质量分数为:
×100%=7.3%
由图象可知,与氢氧化钠反应的稀盐酸的质量为150g,溶质的质量为:150g×7.3%=10.95g
设50g样品中氢氧化钠的质量为y
HCl+NaOH=NaCl+H2O
36.5 40
10.95g y
=
解得:y=12g
50g样品中氢氧化钠的质量分数是:
×100%=24%
(2)氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应生成了碳酸钠和水,反应的化学方程式是:CO2+2NaOH═Na2CO3+H2O;
(3)氢氧化钠变质后有生成的碳酸钠,碳酸钠能与氢氧化钙反应生成了碳酸钙沉淀和氢氧化钠,所以提纯这瓶氢氧化钠,可以采取的方法是:加入适量的氢氧化钙溶液,过滤.
故答为:(1)50g样品中氢氧化钠的质量分数是24%;(2)CO2+2NaOH═Na2CO3+H2O;(3)加入适量的氢氧化钙溶液,过滤.
设50g的稀盐酸中溶质的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 44
x 2.2g
| 73 |
| 44 |
| x |
| 2.2g |
稀盐酸中溶质的质量分数为:
| 3.65g |
| 50g |
由图象可知,与氢氧化钠反应的稀盐酸的质量为150g,溶质的质量为:150g×7.3%=10.95g
设50g样品中氢氧化钠的质量为y
HCl+NaOH=NaCl+H2O
36.5 40
10.95g y
| 36.5 |
| 40 |
| 10.95g |
| y |
50g样品中氢氧化钠的质量分数是:
| 12g |
| 50g |
(2)氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应生成了碳酸钠和水,反应的化学方程式是:CO2+2NaOH═Na2CO3+H2O;
(3)氢氧化钠变质后有生成的碳酸钠,碳酸钠能与氢氧化钙反应生成了碳酸钙沉淀和氢氧化钠,所以提纯这瓶氢氧化钠,可以采取的方法是:加入适量的氢氧化钙溶液,过滤.
故答为:(1)50g样品中氢氧化钠的质量分数是24%;(2)CO2+2NaOH═Na2CO3+H2O;(3)加入适量的氢氧化钙溶液,过滤.
看了 老师拿出一瓶没有瓶盖的氢氧化...的网友还看了以下:
仿写:你们的意志是那样的坚韧和刚强,你们品质是那样的崇高和伟大你们的意志是那样的坚韧和刚强,你们品 2020-06-21 …
“他们的品质是那样的纯洁和高尚,他们的意志是那样的坚韧和刚强,他们的气质是那样的淳朴和谦逊,他们的 2020-06-21 …
仿写句子:这样的题型怎么写呀?他们的品质是那样的清廉的高尚,他们的意志是那样的坚韧和刚强,他们的气 2020-06-21 …
下表是人的血浆、原尿、尿液的三个样品物质样品A样品B样品C葡萄糖00.10.1蛋白质0微量7.0尿 2020-06-22 …
下面是一个健康人的血浆.原尿.尿液的三个样品中主要物质质量物质样品A样品B样品C水969890葡萄 2020-06-22 …
写出下面句子运用的修辞手法他们的品质是那样的纯洁和高尚,他们的意志是那样的坚韧和刚强,他们的气质是 2020-06-23 …
1指出下列句子使用的修辞手法和表达方式(1)他们的品质是那样的纯洁与高尚,他们的意志是那样的坚韧和 2020-06-29 …
根据课文填空。他们的品质是那样的,他们的意志是那样的,他们的气质是那样的,他们的胸怀是那样的! 2020-12-06 …
指出“他们的品质是那样的纯洁和高尚,他们的意志是那样的坚韧和刚强,他们的气质是那样的淳朴和谦逊,他们 2020-12-21 …
为测定某石灰石样品中碳酸钙的含量,取10.0克样品于烧杯中再向其中加入稀盐酸50.0克,恰好完全反应 2021-02-06 …