早教吧作业答案频道 -->化学-->
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.(1)根据右侧能量变化示意图1;请写出NO2和CO反应的热化学方程式.(2)在固定体积的
题目详情
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
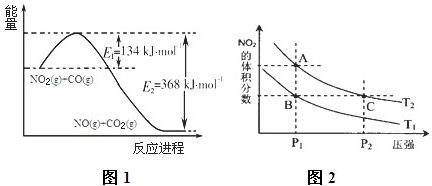
(1)根据右侧能量变化示意图1;请写出NO2和CO反应的热化学方程式___.
(2)在固定体积的密闭容器中,进行如下化学反应3A(s)+4B(g)⇌4C(g)△H>0
其平衡常数K与温度T的关系如下表:
①该反应的平衡常数表达式:K=___.
②试判断K1___K2(填写“>”,“=”或“<”).
③下列各项能说明该反应已达到平衡状态韵是___ (填字母).
a.容器内B.C的浓度之比为1:1
b.v(B)正=v(C)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)对反应N2O4(g)⇌2NO2(g)△H>0,在温度
分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是___.
a.A、C两点的反应速率:A>C b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在l L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的
,则N2的转化率a(N2)=___,以NH3表示该过程的反应速率v(NH3)=___.

(1)根据右侧能量变化示意图1;请写出NO2和CO反应的热化学方程式___.
(2)在固定体积的密闭容器中,进行如下化学反应3A(s)+4B(g)⇌4C(g)△H>0
其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1___K2(填写“>”,“=”或“<”).
③下列各项能说明该反应已达到平衡状态韵是___ (填字母).
a.容器内B.C的浓度之比为1:1
b.v(B)正=v(C)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)对反应N2O4(g)⇌2NO2(g)△H>0,在温度
分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是___.
a.A、C两点的反应速率:A>C b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在l L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的
| 7 |
| 8 |
▼优质解答
答案和解析
(1)该反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol,所以热化学方程式为NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1,
故答案为:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1;
(2)①3A(s)+4B(g)⇌4C(g)△H>0,平衡常数计算表达式k=
,故答案为:
;
②3A(s)+4B(g)⇌4C(g)△H>0为吸热反应,升高温度,平衡正向移动,平衡常数增大,所以K1<K2,故答案为:<;
③a.平衡时反应混合物中各组分的含量保持不变,但容器内BC的浓度之比不一定为为1:1,和起始量有关,所以不能作为平衡的标志,故a错误;
b.平衡时不同物质表示速率之比等于系数之比说明到达平衡,即v(B)正=v(C)逆,说明反应达到平衡,故b正确;
c.反应前后气体体积不变,若压强不变,不能说明反应达到平衡,故c错误;
容器内压强保持不变
d.反应前后气体的质量变化,容器的体积不变,所以密度该变,所以混合气体的密度保持不变,说明反应达到平衡状态,故d正确;
故选:bd;
(3)a.A、C两点都在等温线上,压强越大,反应速率越快,所以速率:C>A,故a错误;
b.A、C两点都在等温线上,平衡常数只与温度有关,所以化学平衡常数:A=C,故b错误;
c.A、C两点都在等温线上,C点压强更高,压强增大,平衡向气体体积减少的方向移动,即逆反应方向移动,N2O4的转化率降低,所以两点N2O4的转化率:A>C,故b正确;
d.该反应为吸热反应,升高温度平衡向正反应方向移动,NO2的体积分数增大,所以由状态B到状态A,可以用加热的方法,故d正确;
故选:cd;
(4)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的八分之七;设反应的氮气物质的量为x;
N2+3H2=2NH3
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol)1-x 3-3x 2x
(1-x)+(3-3x)+2x=(1+3)×
x=0.25mol
则N2的转化率a(N2)=25%;
以NH3表示该过程的反应速率v(NH3)=
=0.05mol/L•min,
故答案为:25%;0.05mol/L•min.
故答案为:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1;
(2)①3A(s)+4B(g)⇌4C(g)△H>0,平衡常数计算表达式k=
| c4(C) |
| c4(B) |
| c4(C) |
| c4(B) |
②3A(s)+4B(g)⇌4C(g)△H>0为吸热反应,升高温度,平衡正向移动,平衡常数增大,所以K1<K2,故答案为:<;
③a.平衡时反应混合物中各组分的含量保持不变,但容器内BC的浓度之比不一定为为1:1,和起始量有关,所以不能作为平衡的标志,故a错误;
b.平衡时不同物质表示速率之比等于系数之比说明到达平衡,即v(B)正=v(C)逆,说明反应达到平衡,故b正确;
c.反应前后气体体积不变,若压强不变,不能说明反应达到平衡,故c错误;
容器内压强保持不变
d.反应前后气体的质量变化,容器的体积不变,所以密度该变,所以混合气体的密度保持不变,说明反应达到平衡状态,故d正确;
故选:bd;
(3)a.A、C两点都在等温线上,压强越大,反应速率越快,所以速率:C>A,故a错误;
b.A、C两点都在等温线上,平衡常数只与温度有关,所以化学平衡常数:A=C,故b错误;
c.A、C两点都在等温线上,C点压强更高,压强增大,平衡向气体体积减少的方向移动,即逆反应方向移动,N2O4的转化率降低,所以两点N2O4的转化率:A>C,故b正确;
d.该反应为吸热反应,升高温度平衡向正反应方向移动,NO2的体积分数增大,所以由状态B到状态A,可以用加热的方法,故d正确;
故选:cd;
(4)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的八分之七;设反应的氮气物质的量为x;
N2+3H2=2NH3
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol)1-x 3-3x 2x
(1-x)+(3-3x)+2x=(1+3)×
| 7 |
| 8 |
则N2的转化率a(N2)=25%;
以NH3表示该过程的反应速率v(NH3)=
| ||
| 10min |
故答案为:25%;0.05mol/L•min.
看了 氮是地球上含量丰富的一种元素...的网友还看了以下:
化学推断题,1.淡黄色粉末A与CO2反应生成气体B和固体C2.气体B和X粉末,加热反应有黑色固体3 2020-05-20 …
锰酸钾加水过滤后可得到什么?其实原题是一道推断题,暗紫色粉末A加热生成固体物质和无色气体B,再将固 2020-06-14 …
将紫黑色固体A加热得到固体B和C,同时得到无色气体D,把带火星的木条伸入D中能重新燃烧,把C加入另 2020-07-13 …
某同学利用“验证牛顿第二定律”的实验器材,测量滑块和长木板之间的动摩擦因数..如图所示,带滑轮的长 2020-07-22 …
如图所示,长为L=1m的AB斜面倾角为θ=37°,将一劲度系数为k=60N/m的轻质弹簧的上端固定 2020-07-31 …
如图,轻弹簧一端固定在O1点,一端系一小球,小球穿在固定于竖直面内、圆心为O2的光滑圆环上,在O1上 2020-11-01 …
2.在显微镜低倍镜下观察时,所见视野内的图像是“上”和“6”,那么载玻片上实际写的字迹图形是()A. 2020-11-07 …
把一杯水和一杯花生油分别放在略低于它们熔点的低温环境中.在它们凝固的过程中,水从开始凝固,油从开始凝 2020-11-22 …
锰酸钾加水过滤后可得到什么?其实原题是一道推断题,暗紫色粉末A加热生成固体物质和无色气体B,再将固体 2020-11-25 …
(2014•余姚市模拟)设想在地球赤道沿地球半径方向插入并固定一根“通天杆”,在“通天杆”上固定A和 2020-12-17 …