早教吧作业答案频道 -->化学-->
已知重铬酸钾和浓盐酸在常温下反应可生成氯气,试回答下列问题:(1)请完成并配平如下化学方程式,再用双线桥表明电子转移的方向和数目:K2Cr2O7+HCl(浓)═KCl+CrCl3+Cl2↑+(2)浓
题目详情
已知重铬酸钾和浓盐酸在常温下反应可生成氯气,试回答下列问题:(1)请完成并配平如下化学方程式,再用双线桥表明电子转移的方向和数目:
K2Cr2O7+HCl(浓)═KCl+CrCl3+Cl2↑+______
(2)浓盐酸在上述反应中体现的性质有___.若反应中转移0.3mol电子,则氧化剂与还原剂的物质的量为___,产生的Cl2的体积(标准状况下)为___.
(3)某化学学习小组利用上述原理制备一定量氯气,并探究其性质.
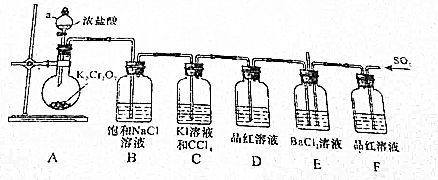
①仪器a的名称是___,B装置盛装饱和食盐水,其作用是___.
②反应开始一段时间后,C中的现象是___.
③实验一段时间后,观察到E的溶液中有白色沉淀,该白色沉淀的化学式为___,相关反应的离子方程式是___.
④反应结束后,分别取D、F中的溶液各少量于试管中加热,所产生的现象是:D中溶液:___,F中溶液:___
K2Cr2O7+HCl(浓)═KCl+CrCl3+Cl2↑+______
(2)浓盐酸在上述反应中体现的性质有___.若反应中转移0.3mol电子,则氧化剂与还原剂的物质的量为___,产生的Cl2的体积(标准状况下)为___.
(3)某化学学习小组利用上述原理制备一定量氯气,并探究其性质.
①仪器a的名称是___,B装置盛装饱和食盐水,其作用是___.
②反应开始一段时间后,C中的现象是___.
③实验一段时间后,观察到E的溶液中有白色沉淀,该白色沉淀的化学式为___,相关反应的离子方程式是___.
④反应结束后,分别取D、F中的溶液各少量于试管中加热,所产生的现象是:D中溶液:___,F中溶液:___

▼优质解答
答案和解析
(1)Cr元素化合价变化为:K2Cr2O7→CrCl3,化合价由+6→+3价,一个原子得3个电子,两个原子得6个电子;Cl元素的化合价变化为:HCl→Cl2,化合价由-1价→0价,一个原子失去一个电子,所以其最小公倍数为6,K2Cr2O7的计量数为1,作还原剂的 HCl的计量数为6,再根据原子守恒判断其它分子的计量数,根据元素守恒,生成物中的未知物为水.所以该方程式为:K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O,用双线桥表示为: ;
;
故答案为: ;
;
(2)反应中氯化氢中氯元素部分化合价升高,表现为还原性,部分化合价不变表现为酸性,依据方程式:K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O,生成3mol氯气,转移6mol电子,氧化剂物质的量为1mol,还原剂物质的量为6mol,则转移0.3mol电子,则氧化剂与还原剂的物质的量为1:6,生成氯气0.15mol,标况下体积V=22.4L/mol×0.15mol=3.36L;
故答案为:酸性和还原性;1:6;3.36L;
(3)①图中仪器a为分液漏斗;浓盐酸易挥发制备的氯气中含有氯化氢,氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,用饱和食盐水可以除去氯气中的氯化氢;
故答案为:分液漏斗;除去氯气中的氯化氢;
②氯气的氧化性强于碘,氯气与碘化钾反应生成单质碘,碘易溶于四氯化碳,四氯化碳密度大与水,与水互不相溶,所以看到现象:溶液分层,下层为紫红色;
故答案为:溶液分层,下层为紫红色;
③二氧化硫与氯气、水反应生成盐酸和硫酸,离子方程式:SO2+Cl2+2H2O═4H++2Cl-+SO42-;硫酸与氯化钡反应生成硫酸钡沉淀,离子方程式:SO42-+Ba2+=BaSO4↓;
故答案为:BaSO4;SO2+Cl2+2H2O═4H++2Cl-+SO42-;SO42-+Ba2+=BaSO4↓;
④二氧化硫能够与有色物质化合生成不稳定的无色物质,受热不稳定的无色物质分解生成有色物质,所以二氧化硫的漂白性具有可逆性,F中褪色的品红溶液加热恢复颜色;氯气与水反应生成的次氯酸具有强的氧化性,能够氧化有色物质生成稳定的无色物质,褪色的品红溶液加热不会恢复颜色;
故答案为:无明显现象;恢复颜色.
 ;
;故答案为:
 ;
;(2)反应中氯化氢中氯元素部分化合价升高,表现为还原性,部分化合价不变表现为酸性,依据方程式:K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O,生成3mol氯气,转移6mol电子,氧化剂物质的量为1mol,还原剂物质的量为6mol,则转移0.3mol电子,则氧化剂与还原剂的物质的量为1:6,生成氯气0.15mol,标况下体积V=22.4L/mol×0.15mol=3.36L;
故答案为:酸性和还原性;1:6;3.36L;
(3)①图中仪器a为分液漏斗;浓盐酸易挥发制备的氯气中含有氯化氢,氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,用饱和食盐水可以除去氯气中的氯化氢;
故答案为:分液漏斗;除去氯气中的氯化氢;
②氯气的氧化性强于碘,氯气与碘化钾反应生成单质碘,碘易溶于四氯化碳,四氯化碳密度大与水,与水互不相溶,所以看到现象:溶液分层,下层为紫红色;
故答案为:溶液分层,下层为紫红色;
③二氧化硫与氯气、水反应生成盐酸和硫酸,离子方程式:SO2+Cl2+2H2O═4H++2Cl-+SO42-;硫酸与氯化钡反应生成硫酸钡沉淀,离子方程式:SO42-+Ba2+=BaSO4↓;
故答案为:BaSO4;SO2+Cl2+2H2O═4H++2Cl-+SO42-;SO42-+Ba2+=BaSO4↓;
④二氧化硫能够与有色物质化合生成不稳定的无色物质,受热不稳定的无色物质分解生成有色物质,所以二氧化硫的漂白性具有可逆性,F中褪色的品红溶液加热恢复颜色;氯气与水反应生成的次氯酸具有强的氧化性,能够氧化有色物质生成稳定的无色物质,褪色的品红溶液加热不会恢复颜色;
故答案为:无明显现象;恢复颜色.
看了 已知重铬酸钾和浓盐酸在常温下...的网友还看了以下:
(1)铬酸根CrO42-呈黄色,重铬酸根Cr2O72-呈橙色.在水溶液中,铬酸根离子和重铬酸根离子 2020-04-12 …
1.镍铬合金比猛铜合金的电阻大,指的是A.镍铬合金比猛铜合金的长度长B.镍铬合金比猛铜合金的横截面 2020-06-20 …
铬(Ⅵ)的化合物是有毒物,已知Cr(Ⅲ)盐的毒性只有Cr(Ⅵ)盐的0.5%,所以将废水中Cr(Ⅵ) 2020-07-25 …
铬(Cr)属于重金属元素,含铬废水和废渣排放必须经过处理达到有关的安全标准.(1)铬原子核中质子数 2020-07-25 …
请回答下列生活中的化学问题:(1)铬酸洗液主要用来清理钢材,它是由浓硫酸和重铬酸钾(化学式K2Cr2 2020-11-21 …
(5分)水龙头中常镀铬。铬是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸 2020-11-25 …
水龙头中常镀铬.铬是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生 2020-11-25 …
水龙头中常镀铬,铬是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生 2020-11-25 …
2012年4月15日,央视《每周质量报告》对“非法厂商用皮革下脚料造药用胶囊”曝光,其制成的胶囊往往 2020-12-07 …
分析化学题用铬酸钾标准溶液测定1.000g试样中的铁.试问1.000L铬酸钾标准溶液中应含有多少克铬 2021-02-01 …