早教吧作业答案频道 -->化学-->
漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应.Ca(ClO)2+CO2+H2O═CaCO3
题目详情
漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应.Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH___ (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式___.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为___;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
(4)现有实验后的HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如图实验方案:
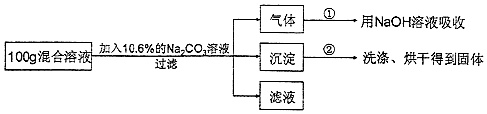
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=___.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH___ (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式___.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为___;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中, ___ | 有气体产生, 气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后试管中加少量 ___ | ___ |

【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=___.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
▼优质解答
答案和解析
(1)某瓶HClO溶液放置一段时间后,次氯酸分解生成了盐酸,溶液的酸性增强,pH减小.
故填:减小.
(2)漂白粉中的次氯酸钙和稀盐酸反应生成氯化钙和次氯酸,加入盐酸反应的化学方程式为:Ca(ClO)2+2HCl=CaCl2+2HClO.
故填:Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)【猜 想】
猜想1:该漂白粉未变质,成分不变,因此固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,一部分次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,全部的次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、CaCO3.
故填:CaCl2、Ca(ClO)2、CaCO3.
【实验探究】实验方案如下表所示:
(4)【实验数据】
(1)设和稀盐酸反应的碳酸钠质量为x,生成的氯化钠质量为y,和氯化钙反应的碳酸钠质量为m,反应生成的氯化钠质量为n,
Na2CO3+2HCl=2NaCl+H2O+CO2↑ Na2CO3+CaCl2=CaCO3↓+2NaCl
106 117 44 106 100 117
x y 4.4g m 10g n
=
=
,
=
=
,
x=10.6g,y=11.7g,m=10.6g,n=11.7g,
碳酸钠溶液的质量为:(10.6g+10.6g)÷10.6%=200g,因此m=200,
故填:200.
(2)经过滤后所得“滤液”中溶质的质量分数为:
×100%=8.2%,
答:过滤后所得“滤液”中溶质的质量分数为8.2%.
故填:减小.
(2)漂白粉中的次氯酸钙和稀盐酸反应生成氯化钙和次氯酸,加入盐酸反应的化学方程式为:Ca(ClO)2+2HCl=CaCl2+2HClO.
故填:Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)【猜 想】
猜想1:该漂白粉未变质,成分不变,因此固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,一部分次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,全部的次氯酸钙和空气中的水、二氧化碳反应生成了碳酸钙,因此固体成分为CaCl2、CaCO3.
故填:CaCl2、Ca(ClO)2、CaCO3.
【实验探究】实验方案如下表所示:
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的稀盐酸,塞上带导管的单孔塞,把导管插入另一盛有澄清石灰水的试管中 | 有气体产生, 气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后试管中加少量品红溶液 | 品红溶液褪色 |
(1)设和稀盐酸反应的碳酸钠质量为x,生成的氯化钠质量为y,和氯化钙反应的碳酸钠质量为m,反应生成的氯化钠质量为n,
Na2CO3+2HCl=2NaCl+H2O+CO2↑ Na2CO3+CaCl2=CaCO3↓+2NaCl
106 117 44 106 100 117
x y 4.4g m 10g n
| 106 |
| x |
| 117 |
| y |
| 44 |
| 4.4g |
| 106 |
| m |
| 100 |
| 10g |
| 117 |
| n |
x=10.6g,y=11.7g,m=10.6g,n=11.7g,
碳酸钠溶液的质量为:(10.6g+10.6g)÷10.6%=200g,因此m=200,
故填:200.
(2)经过滤后所得“滤液”中溶质的质量分数为:
| 11.7g+11.7g |
| 200g+100g-4.4g-10g |
答:过滤后所得“滤液”中溶质的质量分数为8.2%.
看了漂白粉的主要成分为次氯酸钙[C...的网友还看了以下:
我国处于社会主义初级阶段,制定一切方针政策都必须以这个国情为依据,这是因为A.社会主义初级阶段是能 2020-05-13 …
将一组数字按如图2方式排列,若(m,n)表示第m排从左到右第n个数,则(5,4)表示的数是____ 2020-05-15 …
孙中山在三民主义中提出通过改革土地制度,解脱劳动者的贫困,做到“家给人足”.三民主义中具体体现这一 2020-05-17 …
(1)已知一次函数y1=k1X+2在x=5时,y1=4;一次函数y2=k2X-6的图像经过点P(- 2020-05-22 …
已知圆C:x2+(y-3)2=9,过原点作圆C的弦OP,则OP的中点Q的轨迹方程为()A.(x-3 2020-06-04 …
有甲乙两船,甲船和漂流物同时由A地向B地行,乙船也同时从B地向A地行.甲船行3小时后与漂流物相距6 2020-06-20 …
2.一个静止的氢离子(H+)在电场中被加速而获得的速率为一静止的氧离子(O+2)在同一电场中且通过 2020-07-12 …
先主传的翻译以及一些题目曹公南征表,会表卒,子琮代立,遣使请降。先主屯樊,不知曹公卒至,至宛乃闻之, 2020-11-08 …
结合战后资本主义世界经济快速恢复和发展的史实,1.二战后的50年代末和60年代末,资本主义国家中发展 2020-12-12 …
在冬、夏主导风向正好相反的地区,为减少工业对城市的污染,工业区应布局在A.主导风向的下风地带B.主导 2021-01-13 …