早教吧作业答案频道 -->化学-->
钛铁矿的主要成分可表示为FeTiO3(Ti为+4价),某钛铁矿中含FeTiO3为76%.钛白粉在涂料、塑料、油墨、造纸等行业具有广泛的用途,钛白粉的主要成分为TiO2.利用该钛铁矿生产钛白粉及绿矾
题目详情
钛铁矿的主要成分可表示为FeTiO3(Ti为+4价),某钛铁矿中含FeTiO3为76%.钛白粉在涂料、塑料、油墨、造纸等行业具有广泛的用途,钛白粉的主要成分为TiO2.利用该钛铁矿生产钛白粉及绿矾的工艺流程如下:
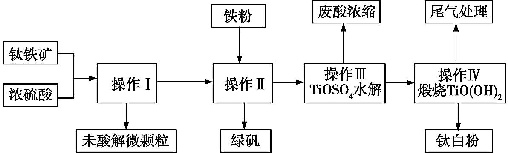
(1)若钛铁矿与浓硫酸反应时Ti 的转化率为92%,操作Ⅰ~Ⅳ中Ti的转化率均为96%,则1t该矿石可生产钛白粉(TiO2)___t (计算结果保留两位小数,下同),能否计算生成的绿矾(FeSO4•7H2O)的质量?___(能则写出计算结果,不能则说明理由).
(2)钛铁矿与硫酸的反应可表示为FeTiO3+H2SO4→TiOSO4+X+H2O(未配平).其中X的化学式为___.
(3)操作Ⅰ的名称是___,操作Ⅱ包括冷却结晶、___.操作Ⅱ中加入铁粉的目的是___ (用离子方程式表示).
(4)写出操作Ⅲ中TiOSO4水解的化学方程式:___.

(1)若钛铁矿与浓硫酸反应时Ti 的转化率为92%,操作Ⅰ~Ⅳ中Ti的转化率均为96%,则1t该矿石可生产钛白粉(TiO2)___t (计算结果保留两位小数,下同),能否计算生成的绿矾(FeSO4•7H2O)的质量?___(能则写出计算结果,不能则说明理由).
(2)钛铁矿与硫酸的反应可表示为FeTiO3+H2SO4→TiOSO4+X+H2O(未配平).其中X的化学式为___.
(3)操作Ⅰ的名称是___,操作Ⅱ包括冷却结晶、___.操作Ⅱ中加入铁粉的目的是___ (用离子方程式表示).
(4)写出操作Ⅲ中TiOSO4水解的化学方程式:___.
▼优质解答
答案和解析
钛铁矿与硫酸反应:FeTiO3+H2SO4→TiOSO4+FeSO4+H2O,然后过滤出未被酸溶解的物质,将所得到的滤液中加入铁粉可以得到了绿矾,将滤液控制在一定的条件,让TiOSO4水 TiOSO4+2H2O═TiO(OH)2↓+H2SO4,将过滤出的沉淀进行煅烧,可以得到钛白粉(TiO2).
(1)设得到二氧化钛的质量是m,则根据元素守恒得:
FeTiO3~TiO2
152 80
1t×76%×92%×96% m
m=0.31t,在制备钛白粉的过程中没有给出钛铁矿与硫酸的反应,在操作Ⅰ和操作Ⅱ中Fe的转化率也是未知的,故不能计算绿矾的产量;
故答案为:0.31;在制备钛白粉的过程中没有给出钛铁矿与硫酸的反应,在操作Ⅰ和操作Ⅱ中Fe的转化率也是未知的,故不能计算绿矾的产量;
(2)在FeTiO3中Ti为+4价故Fe为+2价,反应后铁元素的化合价没有发生改变,钛元素化合价也没有发生改变,其他元素的化合价都没发生改变,故此反应为非氧化还原反应,根据原子守恒可以得而X的化学式为FeSO4,
故答案为:FeSO4;
(3)在操作I从溶液中得到了没有与酸反应的颗粒状物质故所需的操作为过滤;在操作II加入铁粉后得到了绿矾,故应是从溶液中得到晶体的操作为结晶后过滤;在操作II加入铁粉的目的是为了防止在制备过程中钛铁矿+2价的铁生成+3价的铁使制备的绿矾中含有杂质,故应加入铁粉与可能生成的+3价的铁反应生成+2价的铁,
故答案为:过滤;过滤、洗涤、干燥;Fe+2Fe3+═3Fe2+;
(4)TiOSO4水解时SO42-结合水电离的H+,TiO2+结合水电离的OH-,故反应为TiOSO4+2H2O═TiO(OH)2↓+H2SO4,
故答案为:TiOSO4+2H2O═TiO(OH)2↓+H2SO4.
(1)设得到二氧化钛的质量是m,则根据元素守恒得:
FeTiO3~TiO2
152 80
1t×76%×92%×96% m
m=0.31t,在制备钛白粉的过程中没有给出钛铁矿与硫酸的反应,在操作Ⅰ和操作Ⅱ中Fe的转化率也是未知的,故不能计算绿矾的产量;
故答案为:0.31;在制备钛白粉的过程中没有给出钛铁矿与硫酸的反应,在操作Ⅰ和操作Ⅱ中Fe的转化率也是未知的,故不能计算绿矾的产量;
(2)在FeTiO3中Ti为+4价故Fe为+2价,反应后铁元素的化合价没有发生改变,钛元素化合价也没有发生改变,其他元素的化合价都没发生改变,故此反应为非氧化还原反应,根据原子守恒可以得而X的化学式为FeSO4,
故答案为:FeSO4;
(3)在操作I从溶液中得到了没有与酸反应的颗粒状物质故所需的操作为过滤;在操作II加入铁粉后得到了绿矾,故应是从溶液中得到晶体的操作为结晶后过滤;在操作II加入铁粉的目的是为了防止在制备过程中钛铁矿+2价的铁生成+3价的铁使制备的绿矾中含有杂质,故应加入铁粉与可能生成的+3价的铁反应生成+2价的铁,
故答案为:过滤;过滤、洗涤、干燥;Fe+2Fe3+═3Fe2+;
(4)TiOSO4水解时SO42-结合水电离的H+,TiO2+结合水电离的OH-,故反应为TiOSO4+2H2O═TiO(OH)2↓+H2SO4,
故答案为:TiOSO4+2H2O═TiO(OH)2↓+H2SO4.
看了钛铁矿的主要成分可表示为FeT...的网友还看了以下:
2道方程数学题,广深高速公路全长1262千米,一辆汽车从广州出发,以每小时80千米的速度开往深圳. 2020-05-13 …
课外阅读是提高学生素养的重要途径.某校为了解学生课外阅读情况,随机抽查了50名学生,统计他们平均每 2020-05-17 …
(2014•泉州)课外阅读是提高学生素养的重要途径.某校为了了解学生课外阅读情况,随机抽查了50名 2020-05-17 …
火车以.v的平均速度从A地到B地需要时间t,现火车以v0的初速度匀速由A出发,中途急刹车,停止后又 2020-06-12 …
simulink中的s函数我用simulink搭建了一个模块,用到了s函数,用来实现以下功能:对于 2020-07-23 …
判断题1,已知工作效率是a,时间是t,工作总量是c=axt.当a=5.8,t=7时,c=39.判断 2020-07-26 …
帮忙求个递推公式,从兔子繁殖问题衍生而来.m(0)=1,m(1)=1,m(2)=1,m(3)=2, 2020-08-01 …
课外阅读是提高学生素养的重要途径.某校为了了解学生课外阅读情况,随机抽查了50名学生,统计他们平均每 2020-11-14 …
一个物体速度=时间的开平方,也就是说t=1,v=根号1,t=2,v=根号2依此类推t=7是v=根号7 2020-12-28 …
y=2x-3+根号4x-13求值域函数y=(2x-3)+根号下(4x-13)y=2x-3+√(4x- 2021-02-18 …