早教吧作业答案频道 -->化学-->
氨是重要的化工原料,用途广泛.(1)N的基态原子中,有个运动状态不同的未成对电子;(2)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布式是;(3)NH3、N2H4、NH4+、
题目详情
氨是重要的化工原料,用途广泛.
(1)N的基态原子中,有___个运动状态不同的未成对电子;
(2)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布式是___;
(3)NH3、N2H4、NH4+、N2H62+四种微粒中,同种微粒间能形成氢键的有___
(4)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO-构成)溶液吸收对氨合成催化剂(铁粉)有毒害的CO气体.
①醋酸二氨合铜所含的元素中,第一电离能最大的是___.(填元素符号)
②醋酸二氨合铜所含元素的单质,所属的晶体类型有___(填序号).
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态29Cu原子未成对电子数目相同的元素有___种(不含Cu).
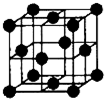
④铜单质为面心立方晶体,其晶胞如图.如果Cu的原子半径为a cm,阿伏加德常数的值为NA,则此种Cu单质的密度表达式为___g/cm3.(相对原子质量Cu:64)

(1)N的基态原子中,有___个运动状态不同的未成对电子;
(2)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布式是___;
(3)NH3、N2H4、NH4+、N2H62+四种微粒中,同种微粒间能形成氢键的有___
(4)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO-构成)溶液吸收对氨合成催化剂(铁粉)有毒害的CO气体.
①醋酸二氨合铜所含的元素中,第一电离能最大的是___.(填元素符号)
②醋酸二氨合铜所含元素的单质,所属的晶体类型有___(填序号).
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态29Cu原子未成对电子数目相同的元素有___种(不含Cu).
④铜单质为面心立方晶体,其晶胞如图.如果Cu的原子半径为a cm,阿伏加德常数的值为NA,则此种Cu单质的密度表达式为___g/cm3.(相对原子质量Cu:64)
▼优质解答
答案和解析
(1)氮原子能量最低排布是: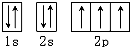 ,有3个运动状态不同的未成对电子,故答案为:3;
,有3个运动状态不同的未成对电子,故答案为:3;
(2)某元素原子的电子数为22,该元素基态原子的电子排布式为:1s22s22p63s23p63d24s2,价电子排布式为:3d24s2;
故答案为:3d24s2;
(3)氢键的形成原因是孤电子对与原子核之间的引力,这就要求另一个条件为原子核要小,所以一般为O,N,F原子,像NH3有一对孤电子对,N2H4有两对孤电子对.所以NH3,N2H4等能形成氢键,故答案为:NH3,N2H4;
(4)①非金属性越强,第一电离能越大,同周期随原子序数增大,元素第一电离能呈增大趋势,氮元素原子2p能级为半满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能由小到大的顺序为:Cu故答案为:N;
②醋酸二氨合铜所含元素的单质有Cu、氢气、氮气、氧气、金刚石、石墨等,铜属于金属晶体,金刚石属于原子晶体,氧气和氢气属于分子晶体;
故答案为:b、c、d;
③Cu的外围电子排布为3d104s1,只有1个未成对电子,第4周期元素中,其它基态原子含有1个单电子的外围电子排布为4s1、3d14s2、4s24p1、4s24p5,分别为K、Sc、Ga、Br,共有4种元素;
故答案为:4;
④晶胞中Cu原子数目为8×
+6×
=4,晶胞质量为4×
g,处于面对角线上的原子相邻,Cu的原子半径为a cm,则晶胞棱长为4a cm×
=2
a cm,则晶体密度为:
=
g/cm3,
故答案为:
.
 ,有3个运动状态不同的未成对电子,故答案为:3;
,有3个运动状态不同的未成对电子,故答案为:3;(2)某元素原子的电子数为22,该元素基态原子的电子排布式为:1s22s22p63s23p63d24s2,价电子排布式为:3d24s2;
故答案为:3d24s2;
(3)氢键的形成原因是孤电子对与原子核之间的引力,这就要求另一个条件为原子核要小,所以一般为O,N,F原子,像NH3有一对孤电子对,N2H4有两对孤电子对.所以NH3,N2H4等能形成氢键,故答案为:NH3,N2H4;
(4)①非金属性越强,第一电离能越大,同周期随原子序数增大,元素第一电离能呈增大趋势,氮元素原子2p能级为半满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能由小到大的顺序为:Cu
②醋酸二氨合铜所含元素的单质有Cu、氢气、氮气、氧气、金刚石、石墨等,铜属于金属晶体,金刚石属于原子晶体,氧气和氢气属于分子晶体;
故答案为:b、c、d;
③Cu的外围电子排布为3d104s1,只有1个未成对电子,第4周期元素中,其它基态原子含有1个单电子的外围电子排布为4s1、3d14s2、4s24p1、4s24p5,分别为K、Sc、Ga、Br,共有4种元素;
故答案为:4;
④晶胞中Cu原子数目为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 65 |
| NA |
| ||
| 2 |
| 2 |
4×
| ||
(2
|
8
| ||
| a3×NA |
故答案为:
8
| ||
| a3×NA |
看了氨是重要的化工原料,用途广泛....的网友还看了以下:
关于英语的常识英文的动词过去式ED结尾的发音规则,还有动词的进行式末尾字母双写规则,此外请给我解释 2020-04-11 …
请教一个被动式句子的用法Hisheadhasnotbeencuthair.似乎被动式的主语和谓语要 2020-04-26 …
英语中哪些动词没有被动式?如题除了come,seem,还有哪些词语没有被动式的?多给一点! 2020-04-26 …
没有运动和行为就没有动物的灵活的生活方式的选择,下列关于动物的运动和行为说法错误的是()A.动物的 2020-05-16 …
claim后通常跟动词的什么形式claim后有动词的固定形式吗 2020-06-14 …
有关圆周运动的所有公式的详细推导过程公式我知道点就是不太清楚有些公式怎么来的教课书和参考书上写的不 2020-07-18 …
求以下成语各3个.1.描写人物外貌的2.描写人物神态的3.表示爱国的4.表示爱学习的5.表示某种精 2020-07-24 …
AABC式的成语5个.ABAB式5个,成语中含有意思相近的字5个,含有褒义的成语5个,含有动物的5 2020-07-24 …
我有道数学题不会,来帮我啊~可能对你们来说,十分简单,是5年级口算上的~A.B两数的和是34.1, 2020-07-31 …
[自我归纳]★动词-ing形式的被动式的构成形式:①一般式:beingdone表示一个正在进行或与 2020-08-01 …