早教吧作业答案频道 -->化学-->
400℃时,某密闭容器中有X,Y,Z三种气体,从反应开始到达到平衡时各物质浓度的变化如图甲所示(假定反应向正反应方向进行).图乙为相应时刻仅改变反应体系中某一条件后正、逆反应
题目详情
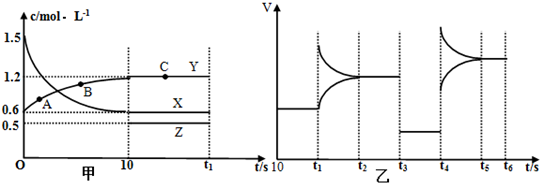
400℃时,某密闭容器中有X,Y,Z三种气体,从反应开始到达到平衡时各物质浓度的变化如图甲所示(假定反应向正反应方向进行).图乙为相应时刻仅改变反应体系中某一条件后正、逆反应速率随时间变化的情况.
(1)反应开始至平衡时v(X)=___;A,B,C三点的逆反应速率由小到大的顺序为___
(2)若t3时改变的条件是降低压强,则Z物质的起始浓度是___;400℃时该反应的平衡常数为___
(3)t4时改变的条件是___,若该反应具有自发性,则此时平衡向___移动(选填“正反应方向”或“逆反应方向”).
(4)在图乙中绘制出t6时向容器中加入一定量X后建立新平衡的过程中(压强保持不变)正、逆反应速率的变化曲线并注明速率类型.
(1)反应开始至平衡时v(X)=___;A,B,C三点的逆反应速率由小到大的顺序为___
(2)若t3时改变的条件是降低压强,则Z物质的起始浓度是___;400℃时该反应的平衡常数为___
(3)t4时改变的条件是___,若该反应具有自发性,则此时平衡向___移动(选填“正反应方向”或“逆反应方向”).
(4)在图乙中绘制出t6时向容器中加入一定量X后建立新平衡的过程中(压强保持不变)正、逆反应速率的变化曲线并注明速率类型.

▼优质解答
答案和解析
(1)根据图象可知,10min时反应达到平衡,X的浓度从1.5mol/L降为0.6mol/L,所以v(X)=
=
=0.09mol/(L•min),根据图可知,反应中X的浓度随反应的进行在减小,Y的浓度在增大,所以Y为生成物,A、B、C三点的Y的浓度逐渐增大,所以A、B、C三点的逆反应速率也逐渐增大,即反应速率A<B<C,
故答案为:0.09mol/(L•min);A<B<C;
(2)若t3时改变的条件是降低压强,根据图乙可知,平衡不移动,说明该反应前后气体体积不变,根据图甲可知,X为反应物,Y为生成物,X、Y的浓度变化量之比为3:2,所以Z只能生成物,且反应方程式为3X⇌2Y+Z,利用三段式可知,
3X⇌2Y+Z
起始(mol/L) 1.5 0.6 0.8
转化(mol/L) 0.9 0.6 0.3
平衡(mol/L) 0.6 1.2 0.5
所以Z物质的起始浓度是0.8mol/L,K=
=1.39,
故答案为:1.1mol/L;1.39;
(3)t4时改变条件时,正逆反应速率都增大,说明t4时改变条件是升高温度,由于该反应熵不变,所以根据反应自发进行的条件,该反应正反应为放热反应,所以升高温度平衡逆向移动,
故答案为:升高温度;逆反应方向;
(4)在t6时向容器中加入一定量X后建立新平衡的过程中(压强保持不变),体积增大,根据反应3X⇌Y+2Z可知,反应物浓度增大,正反应速率增大,生成物浓度减小,逆反应速率 减小,但建立新平衡与原平衡为等效平衡,平衡不移动,最终平衡时的速率与原来的相等地,所以图象为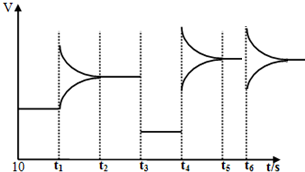 ,
,
故答案为: ;
;
| △c |
| △t |
| 1.5mol/L-0.6mol/L |
| 10min |
故答案为:0.09mol/(L•min);A<B<C;
(2)若t3时改变的条件是降低压强,根据图乙可知,平衡不移动,说明该反应前后气体体积不变,根据图甲可知,X为反应物,Y为生成物,X、Y的浓度变化量之比为3:2,所以Z只能生成物,且反应方程式为3X⇌2Y+Z,利用三段式可知,
3X⇌2Y+Z
起始(mol/L) 1.5 0.6 0.8
转化(mol/L) 0.9 0.6 0.3
平衡(mol/L) 0.6 1.2 0.5
所以Z物质的起始浓度是0.8mol/L,K=
| 1.2×0.52 |
| 0.63 |
故答案为:1.1mol/L;1.39;
(3)t4时改变条件时,正逆反应速率都增大,说明t4时改变条件是升高温度,由于该反应熵不变,所以根据反应自发进行的条件,该反应正反应为放热反应,所以升高温度平衡逆向移动,
故答案为:升高温度;逆反应方向;
(4)在t6时向容器中加入一定量X后建立新平衡的过程中(压强保持不变),体积增大,根据反应3X⇌Y+2Z可知,反应物浓度增大,正反应速率增大,生成物浓度减小,逆反应速率 减小,但建立新平衡与原平衡为等效平衡,平衡不移动,最终平衡时的速率与原来的相等地,所以图象为
 ,
,故答案为:
 ;
;
看了400℃时,某密闭容器中有X,...的网友还看了以下:
过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量 2020-04-06 …
下列说法正确的是()A.所有反应物的键能之和小于所有生成物的键能之和的反应为放热反应B.所有反应物 2020-04-08 …
来评论我的故事寓言故事:从前有一只青蛙.经典故事:从前在井里有一只青蛙.古代故事:从前在小茅屋里有 2020-05-14 …
下列是某同学设计的制取Fe2(SO4)3溶液的四种方案,从反应原理和产物纯度两个角度考虑,最佳方案 2020-05-14 …
安全知识,判断题,3道1.开车门A.在下车开门时,从反光镜内发现后面没有车,才可以下车.B.在下车 2020-05-20 …
从珠算的发明到“银河”系列、“天河一号”再到“天河二号”的研制成功,证实了①认识具有反复性、无限性 2020-07-15 …
从甲苯出发,按下面流程可以合成苯甲酸苯甲酯和水杨酸():(1)写出反应①的反应条件:.(2)写出C 2020-07-29 …
等价关系中的传递性和对称性,为什么不能推出反身性?由等价关系的传递性:若a=>b,b=>a,则a= 2020-08-01 …
隔绝空气,用过量的镁在加热的条件下与TiCl4反应制得金属钛后,如何从反应后的固体中分离出纯净的金属 2020-11-21 …
给"()"里的词造句.1.善于"打破沙锅问到底的人'',却从中(有所)发现,(有所)创造,(有所)成 2021-01-31 …