早教吧作业答案频道 -->化学-->
绿矾(FeSO4•7H2O相对分子质量为278))在医药和染料生产中有广泛应用.下面是以铁屑(含少量锡等杂质)生产绿矾的一种方法:已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开
题目详情
绿矾(FeSO4•7H2O相对分子质量为278))在医药和染料生产中有广泛应用.下面是以铁屑(含少量锡等杂质)生产绿矾的一种方法:
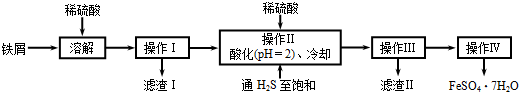
已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
(1)操作Ⅱ在溶液中用硫酸酸化至pH=2的目的是___.通入硫化氢至饱和的目的是:①除去操作Ⅰ所得溶液中含有的Sn2+等杂质离子;②___.
(2)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②___.
(3)测定绿矾产品中Fe2+含量的方法是:
a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液放于锥形瓶中;
c.用硫酸酸化的0.0100mol•L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O)
①滴定终点的判断依据是___.
②上述样品中FeSO4•7H2O的质量分数为___.

已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
(1)操作Ⅱ在溶液中用硫酸酸化至pH=2的目的是___.通入硫化氢至饱和的目的是:①除去操作Ⅰ所得溶液中含有的Sn2+等杂质离子;②___.
(2)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②___.
(3)测定绿矾产品中Fe2+含量的方法是:
a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液放于锥形瓶中;
c.用硫酸酸化的0.0100mol•L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O)
①滴定终点的判断依据是___.
②上述样品中FeSO4•7H2O的质量分数为___.
▼优质解答
答案和解析
(1)操作Ⅱ在溶液中用硫酸酸化至pH=2的目的是,在溶液PH=2时,Sn2+完全沉淀,亚铁离子不沉淀,通入硫化氢至饱和的目的是:硫化氢具有强还原性,可以防止亚铁离子被氧化,
故答案为:除去溶液中的Sn2+离子,亚铁离子不沉淀,防止Fe2+被氧化;
(2)冰水温度低,物质溶解度减小,可以洗去沉淀表面的杂质离子,避免绿矾溶解带来的损失,
故答案为:降低洗涤过程中FeSO4•7H2O的损耗;
(3)①高锰酸钾溶液具有强氧化性能氧化橡胶管,不能用简式滴定管,用酸式滴定管,故答案为:酸式滴定管;
②滴定实验达到终点时,滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
③a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL,则
5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
5 1
n(Fe2+) 0.01000mol/L×0.0200L
计算得到;n(Fe2+)=0.001mol;
则250mL溶液中含Fe2+=0.001mol×
=0.01mol;
FeSO4•7H2O物质的量为0.01mol,质量=0.01mol×278g/mol=2.78g;
质量分数=
×100%=97.54%,
故答案为:97.54%.
故答案为:除去溶液中的Sn2+离子,亚铁离子不沉淀,防止Fe2+被氧化;
(2)冰水温度低,物质溶解度减小,可以洗去沉淀表面的杂质离子,避免绿矾溶解带来的损失,
故答案为:降低洗涤过程中FeSO4•7H2O的损耗;
(3)①高锰酸钾溶液具有强氧化性能氧化橡胶管,不能用简式滴定管,用酸式滴定管,故答案为:酸式滴定管;
②滴定实验达到终点时,滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
③a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL,则
5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
5 1
n(Fe2+) 0.01000mol/L×0.0200L
计算得到;n(Fe2+)=0.001mol;
则250mL溶液中含Fe2+=0.001mol×
| 250 |
| 25 |
FeSO4•7H2O物质的量为0.01mol,质量=0.01mol×278g/mol=2.78g;
质量分数=
| 2.78g |
| 2.85g |
故答案为:97.54%.
看了绿矾(FeSO4•7H2O相对...的网友还看了以下:
直通线和双绞线做法小第有点疑惑.看到有人说"网线有2种做发标准568B:橙白--1,橙--2,绿白 2020-04-27 …
科学家大隅良典因在细胞自噬机制研究中取得成就而获得2016年诺贝尔生理学或医学奖.能参与细胞自噬作 2020-05-14 …
2016年10月3日科学家大隅良典在细胞自噬机制研究中取得成就,从而获得诺贝尔生理学或医学奖,下列 2020-05-14 …
中国饮食文化讲究“色香味”,叶绿素易溶于有机溶剂,不易溶于水,对人体无毒无害,可以作为食用色素添加 2020-05-16 …
[1]20克硫酸溶液与足量的绿化钡溶液充分反应,将所生成的沉淀洗涤干燥后称量,质量为6.9试求:( 2020-06-03 …
铁作导线插入盐水中通电产生物质是什么本人做此实验时,负极有气泡,正极无,产物为绿色不溶物及绿色可溶物 2020-11-11 …
黄色溶液中慢慢加入浅绿色的溶液时颜色会变成什么色来源:稀盐酸除铁锈时,先反应生成黄色的铁离子,过度除 2020-11-24 …
向Fe(NO3)2溶液中加入少量稀盐酸,可能出现的现象是()A.溶液由黄色变为浅绿色B.溶液由浅绿色 2020-11-24 …
(右图14•普陀区图模)甲、乙、丙是三种不含相同离子6可溶性强电解质.它们所含6离子如表所示,若取等 2020-11-30 …
标准溶液的配制,如果是0.5%的溴甲酚绿乙醇溶液那么要怎么配溴甲酚绿和乙醇呢甲基红混合 2021-02-05 …