早教吧作业答案频道 -->化学-->
甲醇是重要的化工原料,在制造燃料电池、农药、医药、塑料、合成纤维及有机化工产品中有着广泛的应用.甲醇也是重要的燃料,可掺入汽油作替代燃料使用,如甲醇已经作为F1赛车的燃
题目详情
甲醇是重要的化工原料,在制造燃料电池、农药、医药、塑料、合成纤维及有机化工产品中有着广泛的应用.甲醇也是重要的燃料,可掺入汽油作替代燃料使用,如甲醇已经作为F1赛车的燃料添加剂.
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)⇌CH3OH(g)
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为___.
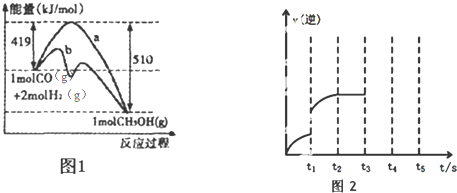
②对于反应Ⅰ,图1表示能量的变化;在“图1”中,曲线___(填:“a”或“b”)表示使用了催化剂;根据图1写出反应Ⅰ的热化学反应方程式___.
③图2表示在恒容密闭容器中,反应Ⅰ的逆反应速率随时间变化的关系.在t1时刻改变某条件,使v逆速率出现了如图所示的变化,改变的条件可能是___.(填字母)
A.充入He气 B.升高温度 C.加催化剂
若t3时刻再在容器中加入一定量的H2,t4-t5时刻达到平衡,请在图中画出v逆的变化示意图.
(2)对于反应Ⅱ,在一定温度下,若将6a mol H2和2amol CO2放入2L的密闭容器中,充分反应后测得CO2的转化率为50%,则该反应的平衡常数为___(用a表示).
若此时再向该容器中投入a mol CO2、3amol H2、amol CH3OH(g)和amol H2O(g),判断平衡移动的方向是___(“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO2的物质的量浓度___(填“增大”、“不变”或“减小”).
(3)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化.
①阳极电极反应式为___.
②除去甲醇的离子方程式为___.

(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)⇌CH3OH(g)
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为___.
②对于反应Ⅰ,图1表示能量的变化;在“图1”中,曲线___(填:“a”或“b”)表示使用了催化剂;根据图1写出反应Ⅰ的热化学反应方程式___.
③图2表示在恒容密闭容器中,反应Ⅰ的逆反应速率随时间变化的关系.在t1时刻改变某条件,使v逆速率出现了如图所示的变化,改变的条件可能是___.(填字母)
A.充入He气 B.升高温度 C.加催化剂
若t3时刻再在容器中加入一定量的H2,t4-t5时刻达到平衡,请在图中画出v逆的变化示意图.
(2)对于反应Ⅱ,在一定温度下,若将6a mol H2和2amol CO2放入2L的密闭容器中,充分反应后测得CO2的转化率为50%,则该反应的平衡常数为___(用a表示).
若此时再向该容器中投入a mol CO2、3amol H2、amol CH3OH(g)和amol H2O(g),判断平衡移动的方向是___(“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO2的物质的量浓度___(填“增大”、“不变”或“减小”).
(3)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化.
①阳极电极反应式为___.
②除去甲醇的离子方程式为___.
▼优质解答
答案和解析
(1)①反应Ⅰ中生成物只有一种,而反应Ⅱ中还有水生成,反应I符合“原子经济性”的原则即原子利用率为100%,故答案为:反应I符合“原子经济性”的原则即原子利用率为100%;
②根据图象1可知,曲线b的活化能低于曲线a的活化能,所以曲线b表示使用了催化剂.从图象上可看出生成物能量低于反应物能量,是放热反应,△H=419-510=-91kJ/mol,热化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H=-91KJ/mol,故答案为:b;CO(g)+2H2(g)⇌CH3OH(g)△H=-91KJ/mol;
③从图2曲线上可以看出,t1时刻并没有达到平衡状态,t1时刻逆反应速率瞬间增大,可使反应速率增大的因素有加压、升温、加催化剂等,若t3时刻再在容器中加入一定量的H2,t4-t5时刻达到平衡,图象如图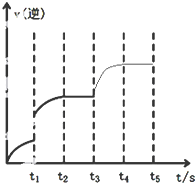 ,
,
故答案为:B; ;
;
(2)CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
起始量(mol) 2a 6a 0 0
转化量(mol) a 3a a a
平衡量(mol) a 3a a a
体积为2L,平衡常数:K
=
.
若此时再向该容器中投入a mol CO2、3amol H2、amol CH3OH(g)和amol H2O(g),因为体积不变,相当于加压,平衡正向移动,各物质浓度都增加,
故答案为:
;增大;
(3)原电池中阳极失电子,由题可知,Co2+在阳极失去电子,阳极电极反应式为Co2+-e-=Co3+,Co3+做氧化剂,能把水中的甲醇氧化成CO2,反应的离子方程式为6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,故答案为:Co2+-e-=Co3+;6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.
②根据图象1可知,曲线b的活化能低于曲线a的活化能,所以曲线b表示使用了催化剂.从图象上可看出生成物能量低于反应物能量,是放热反应,△H=419-510=-91kJ/mol,热化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H=-91KJ/mol,故答案为:b;CO(g)+2H2(g)⇌CH3OH(g)△H=-91KJ/mol;
③从图2曲线上可以看出,t1时刻并没有达到平衡状态,t1时刻逆反应速率瞬间增大,可使反应速率增大的因素有加压、升温、加催化剂等,若t3时刻再在容器中加入一定量的H2,t4-t5时刻达到平衡,图象如图
 ,
,故答案为:B;
 ;
;(2)CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
起始量(mol) 2a 6a 0 0
转化量(mol) a 3a a a
平衡量(mol) a 3a a a
体积为2L,平衡常数:K
| ||||
|
| 4 |
| 27a2 |
若此时再向该容器中投入a mol CO2、3amol H2、amol CH3OH(g)和amol H2O(g),因为体积不变,相当于加压,平衡正向移动,各物质浓度都增加,
故答案为:
| 4 |
| 27a2 |
(3)原电池中阳极失电子,由题可知,Co2+在阳极失去电子,阳极电极反应式为Co2+-e-=Co3+,Co3+做氧化剂,能把水中的甲醇氧化成CO2,反应的离子方程式为6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,故答案为:Co2+-e-=Co3+;6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.
看了甲醇是重要的化工原料,在制造燃...的网友还看了以下:
贷款服务机构更换的,受托机构应当及时通知借款人,并在()工作日内向银监会报告,报送新签署的 2020-05-26 …
企业对考核不能胜任岗位要求的员工,应当及时 按照规定的权限和程序解除劳动合同。 2020-05-27 …
根据国务院《信访条例》,县级以上人民政府信访工作机构发现有关行政机关有( )情形之一的,应当及时 2020-05-27 …
英语翻译NO1-7货仓部份区域钢板割换工程及仓盖修理,机仓风机2台修理工程,部份泵浦电机修理工程, 2020-06-03 …
石油加工工程2考试题,望专家解答!一,填空1.热加工过程遵循()反应机理,催化裂化遵循()反应机理 2020-06-14 …
为下面的报道拟一条标题。(不超过15个字)本报讯:央行将拟定保证金融稳健运行的各项应对预案,建立完 2020-06-16 …
一下工程需要在180天完成,需要工程机械:挖机、平地机、推土机以及压路机的需求量序号项目名称单位工程 2020-11-02 …
英语翻译就是下面这些话机译的不要1变电站装配及送电测试及调试;工程竣工验收及进度请款作业;2XXX项 2020-11-21 …
英语翻译浅谈网络信息安全及对策随着计算机及信息网络技术的飞速发展,计算机已普遍应用到日常工作、生活的 2020-12-09 …
在日常政治生活中,作为政府机关应进一步完善工作机制,自觉接受人大及其常委会的监督指导。这一监督属于[ 2020-12-21 …