早教吧作业答案频道 -->化学-->
硫及其化合物在生产及生活中有着广泛的应用.(1)硫能形成分子组成不同的多种单质,其中一种分子组成为S8,它与KOH溶液反应时可得到两种钾盐,其中一种为K2SO3,写出该反应的离子方
题目详情
硫及其化合物在生产及生活中有着广泛的应用.
(1)硫能形成分子组成不同的多种单质,其中一种分子组成为S8,它与KOH溶液反应时可得到两种钾盐,其中一种为K2SO3,写出该反应的离子方程式:___.
(2)H2S是一种可燃性气体,与O2反应时可转化为单质S或者SO2,标准状况下将2.24L H2S与2.24L O2混合于一容积恒定的密闭容器中并引燃,则生成S的物质的量是___mol,待温度恢复到原温度时,容器中气体密度是原来的___倍.
(3)向MnSO4溶液中加入无色的过二硫酸钾(K2S2O8)可发生反应:(&SrCU可发生反应:2Mn2++5S2O82-+8H2O═2MnO4-+10SO42-+16H+,若反应过程中转移5mol电子,则生成MnO4-的物质的量为___.
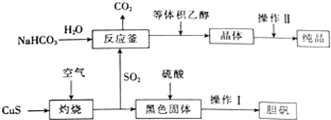
(4)焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂,工业上制备Na2S2O5的方法有多种,其中的一种生产工艺流程如图所示.
①操作Ⅱ包括过滤、洗涤和干燥,干搡时需要在还原性气体或惰性气体氛围下进行干燥,其原因是___.
②写出反应釜中反应的化学方程式:___.
③在0.01mol•L-1的CuSO4溶液中加入等体积0.03mol•L-1Na2S溶液,有黑色CuS沉淀生成,反应后溶液中c(Cu2+)=___.[已知:Ksp(CuS)=6.3×10-36].

(1)硫能形成分子组成不同的多种单质,其中一种分子组成为S8,它与KOH溶液反应时可得到两种钾盐,其中一种为K2SO3,写出该反应的离子方程式:___.
(2)H2S是一种可燃性气体,与O2反应时可转化为单质S或者SO2,标准状况下将2.24L H2S与2.24L O2混合于一容积恒定的密闭容器中并引燃,则生成S的物质的量是___mol,待温度恢复到原温度时,容器中气体密度是原来的___倍.
(3)向MnSO4溶液中加入无色的过二硫酸钾(K2S2O8)可发生反应:(&SrCU可发生反应:2Mn2++5S2O82-+8H2O═2MnO4-+10SO42-+16H+,若反应过程中转移5mol电子,则生成MnO4-的物质的量为___.
(4)焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂,工业上制备Na2S2O5的方法有多种,其中的一种生产工艺流程如图所示.
①操作Ⅱ包括过滤、洗涤和干燥,干搡时需要在还原性气体或惰性气体氛围下进行干燥,其原因是___.
②写出反应釜中反应的化学方程式:___.
③在0.01mol•L-1的CuSO4溶液中加入等体积0.03mol•L-1Na2S溶液,有黑色CuS沉淀生成,反应后溶液中c(Cu2+)=___.[已知:Ksp(CuS)=6.3×10-36].
▼优质解答
答案和解析
(1)依据题意可知单质硫与氢氧化钠发生歧化反应生成硫化钠和亚硫酸钠和水,方程式:3S8+48NaOH=16Na2S+8Na2SO3,离子方程式:3S8+48OH-=24H2O+16S2-+8SO32-,故答案为:3S8+48OH-=24H2O+16S2-+8SO32-;
(2)标准状况下将2.24L H2S与2.24L O2 物质的量都是0.1mol,硫化氢与氧气反应先生成硫单质,硫单质再与氧气反应生成二氧化硫,则:
2H2S+O2(少量)
2S+2H2O,
2 1 2
0.1 0.05 0.1
S+O2
SO2,
1 1 1
0.05 0.05 0.05
所以生成硫的物质的量为0.1mol-0.05mol=0.05mol;
反应后气体为二氧化硫,相对分子质量为64,反应前气体为硫化氢与氧气11混合,平均相对分子质量为
=33
依据相同条件下气体密度之比等于摩尔质量质量等于相对分子质量之比,则待温度恢复到原温度时,容器中气体密度是原来的
倍;
故答案为:0.05mol;
.
(3)由反应可知生成MnO4-,Mn元素化合价由+2价升高为+7价,共升高5价,O元素化合价由-1价降低为-2价,2个O共降低2价,故反应过程中转移5mol电子,则生成MnO4-的物质的量为
=1mol,
故答案为:1mol;
(4)①干燥时需要在还原性气候或惰性气体氛围下,其原因Na2S2O5晶体在空气中被氧化生成Na2SO4,
故答案为:Na2S2O5晶体在空气中被氧化生成Na2SO4;
②反应釜反应方程式为2NaHCO3+2SO2=Na2S2O5+2CO2+H2O,
故答案为:2NaHCO3+2SO2=Na2S2O5+2CO2+H2O;
③反应后溶液中c(S2-)=0.01mol/L,又知Ksp(CuS)=6.3×10-36,故c(Cu2+)=
=6.3×10-34
故答案为:6.3×10-34
(2)标准状况下将2.24L H2S与2.24L O2 物质的量都是0.1mol,硫化氢与氧气反应先生成硫单质,硫单质再与氧气反应生成二氧化硫,则:
2H2S+O2(少量)
| ||
2 1 2
0.1 0.05 0.1
S+O2
| ||
1 1 1
0.05 0.05 0.05
所以生成硫的物质的量为0.1mol-0.05mol=0.05mol;
反应后气体为二氧化硫,相对分子质量为64,反应前气体为硫化氢与氧气11混合,平均相对分子质量为
| 34+32 |
| 2 |
依据相同条件下气体密度之比等于摩尔质量质量等于相对分子质量之比,则待温度恢复到原温度时,容器中气体密度是原来的
| 64 |
| 33 |
故答案为:0.05mol;
| 64 |
| 33 |
(3)由反应可知生成MnO4-,Mn元素化合价由+2价升高为+7价,共升高5价,O元素化合价由-1价降低为-2价,2个O共降低2价,故反应过程中转移5mol电子,则生成MnO4-的物质的量为
| 5 |
| 5 |
故答案为:1mol;
(4)①干燥时需要在还原性气候或惰性气体氛围下,其原因Na2S2O5晶体在空气中被氧化生成Na2SO4,
故答案为:Na2S2O5晶体在空气中被氧化生成Na2SO4;
②反应釜反应方程式为2NaHCO3+2SO2=Na2S2O5+2CO2+H2O,
故答案为:2NaHCO3+2SO2=Na2S2O5+2CO2+H2O;
③反应后溶液中c(S2-)=0.01mol/L,又知Ksp(CuS)=6.3×10-36,故c(Cu2+)=
| 6.3×10-36 |
| 0.01 |
故答案为:6.3×10-34
看了硫及其化合物在生产及生活中有着...的网友还看了以下:
某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能,写出相应的离子方程 2020-04-11 …
在反应中,反应物的过量与否,在什么情况下会引起方程式也就是生成物的变化?我想知道,在题中给出一种反 2020-04-11 …
如果反应物不只一种,增加其中一种反应物的浓度,其他反应物的转化率会增大,...如果反应物不只一种, 2020-04-25 …
初中化学中学到的基本反应类型有四种,下列有关这四种反应的说法正确的是()A.化合反应是有一种物质生 2020-05-13 …
一个反应已达平衡,现向其中加入一种反应物,反应向正反应方向移动,但是这种反应物的转化效率却降低了, 2020-06-04 …
图中每个方框表示一种反应物或一种生成的物质(水均已略去)已知A中含有钾离子E通常情况下是一种无色无 2020-06-11 …
1.当同时改变几个影响平衡的条件时,勒夏特列原理对每个条件来说仍适用,但实际移动方向是多个条件综合 2020-06-26 …
核反应堆的工作原理是利用中子轰击重核发生的裂变反应.在众多的裂变反应中,有一种反应方程为23592 2020-07-01 …
某校宣传栏后3m处与宣传栏平行的地方种了一排树,每隔2m中一颗,共种了6棵续:小明站在距宣传栏前2 2020-07-11 …
在恒温恒压的条件下,对于气体反应体系,充入其中一种气体反应物,反应速率怎样变化一种反应物浓度减小, 2020-07-13 …