早教吧作业答案频道 -->化学-->
(1)写出电解饱和食盐水的离子方程式(2)用如图所示装置电解500mL2mol•L-1食盐水可制取一种消毒液,在通电过程中不断搅拌溶液(使阳极产物全部溶解在溶液中)溶液的pH(填写字母
题目详情
(1)写出电解饱和食盐水的离子方程式___
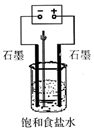
(2)用如图所示装置电解500mL2mol•L-1食盐水可制取一种消毒液,在通电过程中不断搅拌溶液(使阳极产物全部溶解在溶液中)溶液的pH___(填写字母)
A.逐渐增大;
B.逐渐减小;
C.保持不变
当阳极有氧气生成时,停止通电最终所得溶液中的溶质主要成分是___;
假设电解过程中阳极产物无逸出,溶液加水至500mL,消毒液的浓度是___mol•L-1
(3)向上述制取的消毒液中通入CO2气体,可以增强消毒效果,写出反应的离子方程式___.
(2)用如图所示装置电解500mL2mol•L-1食盐水可制取一种消毒液,在通电过程中不断搅拌溶液(使阳极产物全部溶解在溶液中)溶液的pH___(填写字母)
A.逐渐增大;
B.逐渐减小;
C.保持不变
当阳极有氧气生成时,停止通电最终所得溶液中的溶质主要成分是___;
假设电解过程中阳极产物无逸出,溶液加水至500mL,消毒液的浓度是___mol•L-1
(3)向上述制取的消毒液中通入CO2气体,可以增强消毒效果,写出反应的离子方程式___.

▼优质解答
答案和解析
(1)电解饱和食盐水,溶液中的氯离子在阳极失电子生成氯气,氢离子在阴极得到电子生成氢气,阴极附近氢氧根离子浓度增大生成氢氧化钠,反应的离子方程式:2Cl-+2H2O
2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;
(2)因为电解饱和食盐水的离子方程式2Cl-+2H2O
2OH-+H2↑+Cl2↑,所以溶液的pH逐渐增大;
因为阳极产物全部溶解在溶液中,说明生成的氯气与氢氧根反应生成NaClO和NaCl,又阳极有氧气生成时,即氯离子放电完全,则溶液中的溶质主要成分是NaClO;
根据氯原子守恒,则NaClO的物质的量为0.500L×2mol•L-1=1mol,所以c=
=
=2mol•L-1;
故答案为:A;NaClO; 2;
(3)因为碳酸酸性比次氯酸强,所以向上述制取的消毒液中通入CO2气体发生的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32-;故答案为:2ClO-+CO2+H2O=2HClO+CO32-.
| ||
| ||
(2)因为电解饱和食盐水的离子方程式2Cl-+2H2O
| ||
因为阳极产物全部溶解在溶液中,说明生成的氯气与氢氧根反应生成NaClO和NaCl,又阳极有氧气生成时,即氯离子放电完全,则溶液中的溶质主要成分是NaClO;
根据氯原子守恒,则NaClO的物质的量为0.500L×2mol•L-1=1mol,所以c=
| n |
| V |
| 1mol |
| 0.5L |
故答案为:A;NaClO; 2;
(3)因为碳酸酸性比次氯酸强,所以向上述制取的消毒液中通入CO2气体发生的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32-;故答案为:2ClO-+CO2+H2O=2HClO+CO32-.
看了 (1)写出电解饱和食盐水的离...的网友还看了以下:
(1)写出电解饱和食盐水的离子方程式(2)用如图所示装置电解500mL2mol•L-1食盐水可制取 2020-05-14 …
按要求用课文中的原句默写填空。(1)当别人不了解甚至误解自己时,孔子在《论语》中认为应当采取的正确 2020-05-17 …
认识并填写图中鲫鱼各部分的结构([]内填写图中数字).(1)填写名称:1、2、4.(2)鲫鱼的鳍中 2020-07-01 …
文中有不少四字短语:津津有味、气愤填胸、栩栩如生、索然无味、无病呻吟、自作多情、不能自已、一知半解 2020-07-03 …
如图是成熟蘑菇形态示意图,请据图回答、(括号内填写标号,横线上填写文字)(1)填写图中标号代表的名 2020-07-06 …
观察图形,解答问题:(1)按下表已填写的形式填写表中的空格:(2)请用你发现的规律求出图④中的数y 2020-07-16 …
观察图形,解答问题:(1)按下表已填写的形式填写表中的空格:图①图②图③三个角上三个数的积1×(- 2020-07-20 …
如图是人的性别决定图解(甲、乙为正常婚配的夫妇),发现后回答有关问题:(1)图解中甲为,乙为.(填身 2020-11-02 …
如图是人的性别决定图解(甲、乙为正常婚配夫妇)分析后回答有关问题(1)图解中甲为性,乙为性.(2)填 2020-11-02 …
(2012•益阳)观察图形,解答问题:(1)按下表已填写的形式填写表中的空格:图①图②图③三个角上三 2020-11-12 …