早教吧作业答案频道 -->化学-->
某学习小组在实验室以食盐为原料模拟氯碱工业.步骤有①粗盐的提纯、②电解饱和食盐水.具体流程如下:第一步:粗盐(含)的提纯.请回答:(1)试剂丙的化学式为,目
题目详情
某学习小组在实验室以食盐为原料模拟氯碱工业.步骤有①粗盐的提纯、②电解饱和食盐水.具体流程如下:
第一步:粗盐(含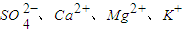 )的提纯.
)的提纯.
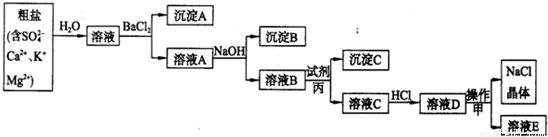
请回答:
(1)试剂丙的化学式为______,目的是除去溶液B中的______ (写离子符号).
(2)用离子方程式表示溶液C中加入HCl后发生的化学反应:______.
(3)溶液E中含有的离子是______(写离子符号).
第二步:用提纯后的食盐晶体制备化工产品烧碱和产品甲.
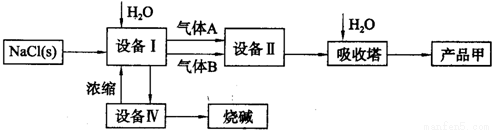
请回答:
(4)设备II内火焰的颜色是______.其化学反应为______ 2HCl
第一步:粗盐(含
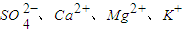 )的提纯.
)的提纯.
请回答:
(1)试剂丙的化学式为______,目的是除去溶液B中的______ (写离子符号).
(2)用离子方程式表示溶液C中加入HCl后发生的化学反应:______.
(3)溶液E中含有的离子是______(写离子符号).
第二步:用提纯后的食盐晶体制备化工产品烧碱和产品甲.

请回答:
(4)设备II内火焰的颜色是______.其化学反应为______ 2HCl
▼优质解答
答案和解析
分析:
(1)欲除去溶液I中的Mg2+、Ca2+、SO42-,则用氢氧化镁除掉Mg2+,用氯化钡除掉SO42-,用碳酸钠除掉Ca2+与多余的Ba2+,根据流程图可知试剂丙为碳酸钠;其作用为除掉掉Ca2+与多余的Ba2+;(2)根据溶液C中的成分为碳酸钠、氢氧化钠、氯化钠、氯化钾来分析;(3)根据溶液D中的成分为:氯化钠、氯化钾和过量的盐酸,操作甲为降温结晶来分析;(4)根据电解饱和食盐水得到氢氧化钠、氢气、氯气,氢气在氯气中燃烧火焰呈苍白色;(5)根据2NaCl+2H2O2NaOH+Cl2↑+H2↑来计算,若要恢复浓度,则通入氯化氢即可,其质量等于氢气和氯气的质量之和;(6)根据溶液中的镁离子能和碱反应生成沉淀.
(1)欲除去溶液I中的Mg2+、Ca2+、SO42-,则用氢氧化镁除掉Mg2+,用氯化钡除掉SO42-,用碳酸钠除掉Ca2+与多余的Ba2+,根据流程图可知试剂丙为碳酸钠;其作用为除掉掉Ca2+与多余的Ba2+,故答案为:Na2CO3;Ca2+、Ba2+;(2)溶液C中的成分为碳酸钠、氢氧化钠、氯化钠、氯化钾,能与盐酸反应的有碳酸钠、氢氧化钠,离子方程式为:CO32-+2H+═H2O+CO2↑,H++OH-=H2O,故答案为:CO32-+2H+═H2O+CO2↑,H++OH-=H2O;(3)根据溶液D中的成分为:氯化钠、氯化钾和过量的盐酸,操作甲为降温结晶,溶液E中含有氯化钠、氯化钾和过量的盐酸,含有的离子有:Na+、K+、H+、OH-、Cl-,故答案为:Na+、K+、H+、OH-、Cl-.(4)根据电解饱和食盐水得到氢氧化钠、氢气、氯气,氢气在氯气中燃烧火焰呈苍白色,故答案为:苍白色;H2+Cl22HCl;(5)溶液的pH值为13,c(OH-)=0.1mol/L,n(NaOH)=cV=0.1mol/L×0.1L=0.01mol 2NaCl+2H2O2NaOH+Cl2↑+H2↑ 2 1 1 0.01mol n(Cl2) n(H2) n(Cl2)=0.005mol n(H2)=0.005mol阴极产生的氢气的体积n(氢气)=0.005mol×22.4L/mol=0.112L=112mL, m(Cl2)+m(H2)=0.005mol×71g/mol+0.005mol×2g/mol=0.365g,所以若恢复原溶液的成分和浓度,需要加入氯化氢,其质量为:0.365g;故答案为:112;氯化氢;0.365;(6)电解食盐水产生氢氧化钠:2NaCl+2H2O2NaOH+H2↑+Cl2↑,氢氧化钠能和镁离子反应生成沉淀:2OH-+Mg2+=Mg(OH)2↓,故答案为:溶液中出现白色沉淀;2Cl-+2H2O2OH-+H2↑+Cl2↑;2OH-+Mg2+=Mg(OH)2↓.
点评:
本题主要考查了粗盐的提纯、电解饱和食盐水,涉及到物质的除杂和提纯,化学计算等,难度中等,试题综合性较大.
分析:
(1)欲除去溶液I中的Mg2+、Ca2+、SO42-,则用氢氧化镁除掉Mg2+,用氯化钡除掉SO42-,用碳酸钠除掉Ca2+与多余的Ba2+,根据流程图可知试剂丙为碳酸钠;其作用为除掉掉Ca2+与多余的Ba2+;(2)根据溶液C中的成分为碳酸钠、氢氧化钠、氯化钠、氯化钾来分析;(3)根据溶液D中的成分为:氯化钠、氯化钾和过量的盐酸,操作甲为降温结晶来分析;(4)根据电解饱和食盐水得到氢氧化钠、氢气、氯气,氢气在氯气中燃烧火焰呈苍白色;(5)根据2NaCl+2H2O2NaOH+Cl2↑+H2↑来计算,若要恢复浓度,则通入氯化氢即可,其质量等于氢气和氯气的质量之和;(6)根据溶液中的镁离子能和碱反应生成沉淀.
(1)欲除去溶液I中的Mg2+、Ca2+、SO42-,则用氢氧化镁除掉Mg2+,用氯化钡除掉SO42-,用碳酸钠除掉Ca2+与多余的Ba2+,根据流程图可知试剂丙为碳酸钠;其作用为除掉掉Ca2+与多余的Ba2+,故答案为:Na2CO3;Ca2+、Ba2+;(2)溶液C中的成分为碳酸钠、氢氧化钠、氯化钠、氯化钾,能与盐酸反应的有碳酸钠、氢氧化钠,离子方程式为:CO32-+2H+═H2O+CO2↑,H++OH-=H2O,故答案为:CO32-+2H+═H2O+CO2↑,H++OH-=H2O;(3)根据溶液D中的成分为:氯化钠、氯化钾和过量的盐酸,操作甲为降温结晶,溶液E中含有氯化钠、氯化钾和过量的盐酸,含有的离子有:Na+、K+、H+、OH-、Cl-,故答案为:Na+、K+、H+、OH-、Cl-.(4)根据电解饱和食盐水得到氢氧化钠、氢气、氯气,氢气在氯气中燃烧火焰呈苍白色,故答案为:苍白色;H2+Cl22HCl;(5)溶液的pH值为13,c(OH-)=0.1mol/L,n(NaOH)=cV=0.1mol/L×0.1L=0.01mol 2NaCl+2H2O2NaOH+Cl2↑+H2↑ 2 1 1 0.01mol n(Cl2) n(H2) n(Cl2)=0.005mol n(H2)=0.005mol阴极产生的氢气的体积n(氢气)=0.005mol×22.4L/mol=0.112L=112mL, m(Cl2)+m(H2)=0.005mol×71g/mol+0.005mol×2g/mol=0.365g,所以若恢复原溶液的成分和浓度,需要加入氯化氢,其质量为:0.365g;故答案为:112;氯化氢;0.365;(6)电解食盐水产生氢氧化钠:2NaCl+2H2O2NaOH+H2↑+Cl2↑,氢氧化钠能和镁离子反应生成沉淀:2OH-+Mg2+=Mg(OH)2↓,故答案为:溶液中出现白色沉淀;2Cl-+2H2O2OH-+H2↑+Cl2↑;2OH-+Mg2+=Mg(OH)2↓.
点评:
本题主要考查了粗盐的提纯、电解饱和食盐水,涉及到物质的除杂和提纯,化学计算等,难度中等,试题综合性较大.
看了 某学习小组在实验室以食盐为原...的网友还看了以下:
某组室共有6人,请假人数有2人,病假1人2天,年休1人3天,求这个组室这周的出勤率. 2020-06-07 …
某寝室四位同学各有一张贺年卡并且送给寝室中的其中一位同学且每人得到了一张有多少种送法?某寝室四位同 2020-07-04 …
某组织培养实验室的愈伤组织被真菌严重污染,为查找污染原因设计了4个实验,实验条件除图示外其他均相同 2020-07-13 …
某组织培养实验室的愈伤组织被真菌严重污染,为查找污染原因设计了四个实验,实验条件除图示外其他均相同 2020-07-15 …
某科室共有11人,如果“该科室所有的人都是四川人”“该科室所有的人都不是四川人”和“该科室有的人不 2020-07-20 …
某科室共11人如果“该科室所有的人都是四川人”“该科室所有的人都不是四川人”中有一句是假话,则下列必 2020-11-21 …
某科室有科员8人,要从中选出2名小组长,请问可有多少种选择? 2020-11-21 …
某研究性学习小组设计用如下方法测定某居室空气中甲醛(HCHO)的含量.Ⅰ.测定原理:4MnO4-+5 2020-12-23 …
某研究性学习小组设计用如下方法测定某居室空气中甲醛(HCHO)的含量.Ⅰ.测定原理:4MnO4-+5 2020-12-23 …
在电学探究实验课中,某组同学在实验室利用如图甲所示的电路图连接好电路,并用于测定定值电阻R0,电源的 2020-12-31 …