早教吧作业答案频道 -->化学-->
NH4Al(SO4)2、NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:(1)常温时,0.1mol•L-1NH4Al(SO4)2溶液的PH=3.①溶液的Kw=(填数值),由水电离的c(H+)=mol•L-1②溶
题目详情
NH4Al(SO4)2、NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下
列问题:
(1)常温时,0.1mol•L-1NH4Al(SO4)2溶液的PH=3.
①溶液的Kw=___(填数值),由水电离的c(H+)=___mol•L-1
②溶液中c(NH4+)+c(NH3•H2O)___c (Al3+)+c( Al(OH)3)(填“>”“=”“<.”):
2c(SO42-)-c(NH4+)-3c (Al3+)=___ mol•L-1(填数值).
(2)80℃时,0.1mol•L-1NH4Al(SO4)2溶液的pH小于3,分析导致pH随温度变化的原因是___.
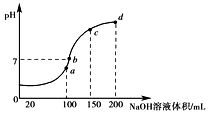
(3)常温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示.
①图中a、b、c、d四个点中水的电离程度最小的是___.
②向NH4HSO4溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为___.
③NH4HSO4溶液中各离子浓度由大到小的排列顺序是___.
列问题:

(1)常温时,0.1mol•L-1NH4Al(SO4)2溶液的PH=3.
①溶液的Kw=___(填数值),由水电离的c(H+)=___mol•L-1
②溶液中c(NH4+)+c(NH3•H2O)___c (Al3+)+c( Al(OH)3)(填“>”“=”“<.”):
2c(SO42-)-c(NH4+)-3c (Al3+)=___ mol•L-1(填数值).
(2)80℃时,0.1mol•L-1NH4Al(SO4)2溶液的pH小于3,分析导致pH随温度变化的原因是___.
(3)常温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示.
①图中a、b、c、d四个点中水的电离程度最小的是___.
②向NH4HSO4溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为___.
③NH4HSO4溶液中各离子浓度由大到小的排列顺序是___.
▼优质解答
答案和解析
(1)①常温时,水的离子积常数为l.0×l0-14;0.1mol•L-1NH4Al(SO4)2溶液的PH=3是因为铵根离子和铝离子的水解,所以由水电离的c(H+)=l.0×l0-3mol/L,
故答案为:l.0×l0-14;l.0×l0-3;
②据物料守恒,NH4Al(SO4)2中N原子与Al原子个数比为1:1,所以c(NH4+)+c(NH3•H2O)=c (Al3+)+c( Al(OH)3);根据电荷守恒得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol•L-1-10-11mol•L-1=10-3-10-11mol•L-1,
故答案为:=;10-3-10-11;
(2)NH4Al(SO4)2水解,升高温度其水解程度增大,pH减小,故答案为:NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
(3)①a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离,所以d点水的电离程度最小,故答案为:d;
②向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液100mL时,仅发生氢离子和氢氧根离子的中和反应,离子方程式为H++OH-=H2O,
故答案为:H++OH-=H2O;
③NH4HSO4的电离方程式为NH4HSO4=NH4++H++SO42-,还有水的微弱电离,铵根离子因微弱水解导致浓度略有减小,所以离子浓度由大到小的顺序为c(H+)>c(SO42-)>c(NH4+)>c(OH-),故答案为:c(H+)>c(SO42-)>c(NH4+)>c(OH-).
故答案为:l.0×l0-14;l.0×l0-3;
②据物料守恒,NH4Al(SO4)2中N原子与Al原子个数比为1:1,所以c(NH4+)+c(NH3•H2O)=c (Al3+)+c( Al(OH)3);根据电荷守恒得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol•L-1-10-11mol•L-1=10-3-10-11mol•L-1,
故答案为:=;10-3-10-11;
(2)NH4Al(SO4)2水解,升高温度其水解程度增大,pH减小,故答案为:NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
(3)①a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离,所以d点水的电离程度最小,故答案为:d;
②向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液100mL时,仅发生氢离子和氢氧根离子的中和反应,离子方程式为H++OH-=H2O,
故答案为:H++OH-=H2O;
③NH4HSO4的电离方程式为NH4HSO4=NH4++H++SO42-,还有水的微弱电离,铵根离子因微弱水解导致浓度略有减小,所以离子浓度由大到小的顺序为c(H+)>c(SO42-)>c(NH4+)>c(OH-),故答案为:c(H+)>c(SO42-)>c(NH4+)>c(OH-).
看了NH4Al(SO4)2、NH4...的网友还看了以下:
鲁迅《中国人失掉自信力了吗》1.副词.如“总’句子1:赏析:句子2:赏析:句子3:赏析:1.副词. 2020-06-04 …
正常情况多,人体胃液的pH在1.2~3.0之间.当人体内胃酸分泌过多时,会出现吐酸水、恶心、胃痛等 2020-06-22 …
某城市爱心医院共有医生152人.选出男医生的11分之1和5个女医生组成一支医疗队奔赴四川汶川地震灾 2020-06-25 …
头痛医头,脚痛医脚体现了具体分析的辩证法思想 2020-06-27 …
头痛医头,脚痛医脚体现了具体分析的辩证法思想.内容如题, 2020-06-27 …
麻烦了,帮帮忙预防医学的1简述职业性损害的一级预防措施2防止信息偏倚的措施6.某医师用甲、乙两疗法 2020-07-10 …
材料分析陈晓兰,女,55岁,原上海一家医院的理疗科医生.近年来,陈晓兰一直从事医疗器械行业打假,被 2020-07-14 …
某市对A、B两类医院进行改造。根据预算,共需资金1575万元。改造1所A类医院和2所B类医院共需资 2020-08-04 …
一道逻辑推理题有三位见习医生,他们在同一家医院中担任住院医生.(1)一星期中只有一天三位见习医生同 2020-08-04 …
甲医院用药品A、B的患者分别有50人100人,各治愈了35人69人.乙医院用药品A、B的患者分别有 2020-08-04 …