早教吧作业答案频道 -->化学-->
铵明矾[(NH4)xAly(SO4)m•nH2O]为无色、透明晶体.工业常用于制造颜料、媒染剂、净水剂等.制取铵明矾的工艺流程图如下:(1)25℃时,将0.2mol•L-1的氨水与0.1mol•L-1的H2SO4溶液等体积混
题目详情
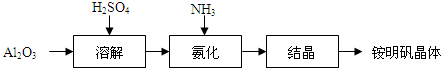
铵明矾[(NH4)xAly(SO4)m•nH2O]为无色、透明晶体.工业常用于制造颜料、媒染剂、净水剂等.制取铵明矾的工艺流程图如下:
(1)25℃时,将0.2mol•L-1的氨水与0.1mol•L-1的H2SO4溶液等体积混合,所得溶液的pH=5,则该温度下氨水的电离常数Kb≈___.(忽略混合时溶液体积的变化)
(2)铵明矾的化学式可通过下列实验测定:准确称取4.53g铵明矾配成溶液,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色沉淀4.66g.另取4.53g铵明矾,配制成250.00mL溶液.准确量取25.00mL 溶液,调节溶液pH约为3.5,加入30.00mL 0.0500mol•L-1乙二胺四乙酸二钠(Na2H2Y)标准溶液,加热至沸,使Al3+与Na2H2Y的反应迅速定量进行;待反应完成后调节溶液为5~6,加入二甲酚橙指示剂,再用0.0500mol•L-1 Zn2+滴定液返滴定过量的Na2H2Y,至滴定终点消耗Zn2+滴定液10.00mL.反应的离子方程式为:Al3++H2Y2-═AlY-+2H+,Zn2++H2Y2-═ZnY2-+2H+
①若返滴定时,滴定管在使用前未用Zn2+滴定液润洗,测得的Al3+含量将___(填“偏高”、或“偏低”或“不变”);
②调节溶液pH约为3.5的目的是___;
③通过计算确定铵明矾的化学式(写出计算过程).

(1)25℃时,将0.2mol•L-1的氨水与0.1mol•L-1的H2SO4溶液等体积混合,所得溶液的pH=5,则该温度下氨水的电离常数Kb≈___.(忽略混合时溶液体积的变化)
(2)铵明矾的化学式可通过下列实验测定:准确称取4.53g铵明矾配成溶液,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色沉淀4.66g.另取4.53g铵明矾,配制成250.00mL溶液.准确量取25.00mL 溶液,调节溶液pH约为3.5,加入30.00mL 0.0500mol•L-1乙二胺四乙酸二钠(Na2H2Y)标准溶液,加热至沸,使Al3+与Na2H2Y的反应迅速定量进行;待反应完成后调节溶液为5~6,加入二甲酚橙指示剂,再用0.0500mol•L-1 Zn2+滴定液返滴定过量的Na2H2Y,至滴定终点消耗Zn2+滴定液10.00mL.反应的离子方程式为:Al3++H2Y2-═AlY-+2H+,Zn2++H2Y2-═ZnY2-+2H+
①若返滴定时,滴定管在使用前未用Zn2+滴定液润洗,测得的Al3+含量将___(填“偏高”、或“偏低”或“不变”);
②调节溶液pH约为3.5的目的是___;
③通过计算确定铵明矾的化学式(写出计算过程).
▼优质解答
答案和解析
(1)将0.2mol•L-1的氨水与0.1mol•L-1的H2SO4溶液等体积混合,二者恰好反应生成硫酸铵,生成硫酸铵的浓度为:0.05mol/L,铵根离子水解生成一水合氨和氢离子,水解反应方程式为:NH4++H2O⇌NH3•H2O+H+,所得溶液的pH=5,则c(H+)=10-5,c(NH3•H2O)=c(H+)=10-5,c(OH-)=
=1×10-9,c(NH4+)=0.1-10-5,K=
=
=1×10-5,故答案为:1×10-5;
(2)①若返滴定时,滴定管在使用前未用Zn2+滴定液润洗,导致锌离子浓度偏低,所用体积偏大,据此计算出未和铝离子反应的乙二胺四乙酸二钠溶液偏多,和铝离子反应的乙二胺四乙酸二钠偏少,由此计算的铝离子浓度偏低;故答案为:偏低;
②本实验是用乙二胺四乙酸二钠滴定铝离子,调节pH为3.5,酸性条件下抑制了铝离子的水解,保证所有铝离子和乙二胺四乙酸二钠反应,故答案为:抑制Al3+水解;
③n(铵明矾)=4.53g÷453g/mol=0.01mol,n(SO42-)=n(BaSO4)=4.66g÷233g/mol=0.02mol,
n(Al3+)=250mL÷25mL×0.0500mol/L×(30.00-10.00)×10-3L=0.01mol,
由电荷守恒知:n(NH4+)=2n(SO42-)-3n(Al3+)=0.02mol×2-0.01mol×3=0.01mol
n(H2O)=(4.53-0.02×96-0.01×27-0.01×18)g÷18g/mol=0.12mol,
所以n(Al3+):n(NH4+):n(SO42-):n(H2O)=0.01mol:0.01mol:0.02mol:0.12mol=1:1:2:12,
铵明矾的化学式为:NH4Al(SO4)2•12H2O,
答:铵明矾的化学式为NH4Al(SO4)2•12H2O.
| 1×10-14 |
| 10-5 |
| c(NH4+)•c(OH-) |
| c(NH3•H2O) |
| (0.1-10-5)×10-9 |
| 10-5 |
(2)①若返滴定时,滴定管在使用前未用Zn2+滴定液润洗,导致锌离子浓度偏低,所用体积偏大,据此计算出未和铝离子反应的乙二胺四乙酸二钠溶液偏多,和铝离子反应的乙二胺四乙酸二钠偏少,由此计算的铝离子浓度偏低;故答案为:偏低;
②本实验是用乙二胺四乙酸二钠滴定铝离子,调节pH为3.5,酸性条件下抑制了铝离子的水解,保证所有铝离子和乙二胺四乙酸二钠反应,故答案为:抑制Al3+水解;
③n(铵明矾)=4.53g÷453g/mol=0.01mol,n(SO42-)=n(BaSO4)=4.66g÷233g/mol=0.02mol,
n(Al3+)=250mL÷25mL×0.0500mol/L×(30.00-10.00)×10-3L=0.01mol,
由电荷守恒知:n(NH4+)=2n(SO42-)-3n(Al3+)=0.02mol×2-0.01mol×3=0.01mol
n(H2O)=(4.53-0.02×96-0.01×27-0.01×18)g÷18g/mol=0.12mol,
所以n(Al3+):n(NH4+):n(SO42-):n(H2O)=0.01mol:0.01mol:0.02mol:0.12mol=1:1:2:12,
铵明矾的化学式为:NH4Al(SO4)2•12H2O,
答:铵明矾的化学式为NH4Al(SO4)2•12H2O.
看了铵明矾[(NH4)xAly(S...的网友还看了以下:
一定条件下将m体积的一氧化氮和n体积的氧气同时通入倒立于水中且充满水的容器内,充分反应后,容器内残 2020-05-14 …
一气球质量为M,下系一个质量为m的物体,此时气球以加速度a匀加速上升.则还…………一气球质量为M, 2020-05-16 …
一个公司共有N名员工,下设一些部门,要采用等比例分层抽样的方法从全体员工中抽取样本容量为n的样本, 2020-06-08 …
如图中a、b和c构成了化合物m.下列叙述正确的是()A.若c为腺嘌呤,则m一定是腺嘌呤脱氧核苷酸B 2020-07-04 …
如图所示,质量不同的两物体通过轻绳相连,M>m,滑轮光滑且质量不计,轻绳的伸长不计,空气阻力不计. 2020-07-15 …
如图,在光滑的水平面上,叠放着两个质量分别为m、M的物体(m<M),用一水平恒力作用在m物体上,两物 2020-11-02 …
芳香化合物A是一种基本化工原料,可以制备有机化工中间体M.各物质之间的转化关系如下:已知:请回答下列 2020-11-04 …
某分部分项工程计划单价6元/m,当月计划完成工程量lom,当月实际完成工程量16m,实际单价5元/m 2020-11-07 …
如图所示,小物体P放在直角斜劈M上,M下端连接一竖直弹簧,并紧贴竖直光滑墙壁;开始时,P、M静止,M 2020-11-25 …
已知有如下平衡体系:3A(g)+B(g)2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和 2020-12-22 …