早教吧作业答案频道 -->化学-->
C和Si元素在化学中占有极其重要的地位:(1)写出Si的基态原子核外电子排布式.从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为.(2)CO2分子的空间构型为,中
题目详情
C和Si元素在化学中占有极其重要的地位:
(1)写出Si的基态原子核外电子排布式___.从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为___.
(2)CO2分子的空间构型为___,中心原子的杂化方式为___,和CO2 互为等电子体的氧化物是___.
(3)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键.___
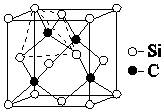
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为___,在SiC中,每个C原子周围最近的C原子数目为___,若晶胞的边长为a pm,则金刚砂的密度为___.

(1)写出Si的基态原子核外电子排布式___.从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为___.
(2)CO2分子的空间构型为___,中心原子的杂化方式为___,和CO2 互为等电子体的氧化物是___.
(3)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键.___
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为___,在SiC中,每个C原子周围最近的C原子数目为___,若晶胞的边长为a pm,则金刚砂的密度为___.
▼优质解答
答案和解析
(1)Si是14号元素,Si原子核外共14个电子,按照能量最低原则电子先填入能量最低的1s轨道,填满后再依次填入能量较高的轨道;其电子排布式为:1s22s22p63s23p2;从电负性的角度分析,O和C位于同一周期,非金属性O强于C;C和Si为与同一主族,C的非金属性强于Si,故由强到弱为O>C>Si,
故答案为:1s22s22p63s23p2; O>C>Si;
(2)CO2分子为直线形结构,可知碳原子采取sp杂化方式,原子数目相等、价电子总数也相等的微粒互为等电子体,和CO2 互为等电子体的氧化物是N2O,
故答案为:直线形;sp;N2O;
(3)CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键,是因Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键,故答案为:Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键;
(4)金刚砂(SiC)的硬度为9.5,属于原子晶体;每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,所以每个碳原子周围最近的碳原子数目为3×4=12;该晶胞中C原子个数=8×
+6×
=4,Si原子个数为4,晶胞边长=a×10-10cm,体积V=(a×10-10cm)3,ρ=
=
g•cm3=
g•cm3;
故答案为:原子晶体;12;
.
故答案为:1s22s22p63s23p2; O>C>Si;
(2)CO2分子为直线形结构,可知碳原子采取sp杂化方式,原子数目相等、价电子总数也相等的微粒互为等电子体,和CO2 互为等电子体的氧化物是N2O,
故答案为:直线形;sp;N2O;
(3)CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键,是因Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键,故答案为:Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键;
(4)金刚砂(SiC)的硬度为9.5,属于原子晶体;每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,所以每个碳原子周围最近的碳原子数目为3×4=12;该晶胞中C原子个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| V |
| ||
| (a×10 -10)3 |
| 1.6×10 32 |
| N A |
故答案为:原子晶体;12;
| 1.6×10 32 |
| N A |
看了C和Si元素在化学中占有极其重...的网友还看了以下:
基因型为AaBbCc的个体,测交后代的类型及比例是:Aabbcc占21%,AaBbCc占4%,Aa 2020-04-07 …
某植物种群中基因型AA的个体占20%,基因型aa的个体占50%.倘若人为舍弃隐性性状类型仅保留显性 2020-06-30 …
如果在一个种群中,基因型AA的比例占25%,基因型Aa的比例占50%,基因型aa的比例占25%.已 2020-07-25 …
下列对不同时期原子结构模型的提出时间排列正确的是()①电子分层排布模型;②“葡萄干布丁”模型;③量 2020-07-29 …
固体、液体和气体是自然界中的物质最常见的三种状态.如图所示是这三种状态物质的分子结构排列模型.其中 2020-07-30 …
某植物种群中基因型为AA的个体数占20%,基因型aa的个体数占50%.(1)这个种群中基因A、a的频 2020-11-04 …
(1)我国土地利用类型中,耕地占,林地占16.6%,草地占32.6%,而沙漠、石头、山地永久积雪和冰 2020-11-21 …
C和Si元素在化学中占有极其重要的地位:(1)写出Si的基态原子核外电子排布式.从电负性角度分析,C 2020-12-07 …
在人的ABO血型系统中,血液可分为四种类型:A型、B型、型和型.血液占体重的.一般来说.输血时应以为 2020-12-24 …
某植物种群,AA基因型个体占30%,aa基因型个体占20%,据此回答下面的问题.(1)该植物的A、a 2021-01-04 …