早教吧作业答案频道 -->化学-->
B、C、N、O、Si、S是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在(1)Si位于元素周期表第周期族;基态硼原子的电子排布式为;C、N、Si元素原子的第一电离
题目详情
B、C、N、O、Si、S是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在
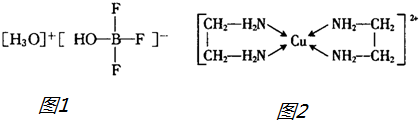
(1)Si位于元素周期表第___周期___族;基态硼原子的电子排布式为___;C、N、Si元素原子的第一电离能由大到小的顺序为___.
(2)BF3与一定量的水可形成如图1晶体R.晶体R中各种微粒间的作用力包含___(填字母).
a.离子键 b.共阶键 c.范德华力 d.金属键
(3)乙二胺(H2N-CH2-CH2-NH2)与CuCl2溶液可形成配离子(结构如图2).乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是___.
(4)在25℃、101kpa下,NO2(g)与SO2(g)反应生成SO3(g)和NO(g),已知每生成1g SO3(g)放出热量0.52kJ,该反应的热化学方程式是___.
(5)硼砂(Na2B4O7•10H2O)可用作清洁剂或杀虫剂,易溶于水.在酸性溶液中会生成H3BO3,该反应的离子方程式为___.
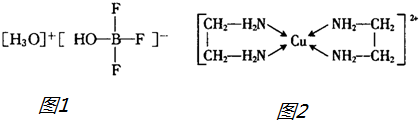
(1)Si位于元素周期表第___周期___族;基态硼原子的电子排布式为___;C、N、Si元素原子的第一电离能由大到小的顺序为___.
(2)BF3与一定量的水可形成如图1晶体R.晶体R中各种微粒间的作用力包含___(填字母).
a.离子键 b.共阶键 c.范德华力 d.金属键
(3)乙二胺(H2N-CH2-CH2-NH2)与CuCl2溶液可形成配离子(结构如图2).乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是___.
(4)在25℃、101kpa下,NO2(g)与SO2(g)反应生成SO3(g)和NO(g),已知每生成1g SO3(g)放出热量0.52kJ,该反应的热化学方程式是___.
(5)硼砂(Na2B4O7•10H2O)可用作清洁剂或杀虫剂,易溶于水.在酸性溶液中会生成H3BO3,该反应的离子方程式为___.
▼优质解答
答案和解析
(1)硅是14号元素,位于第三周期,第ⅣA族,硼原子核外有5个电子,其核外电子排布式为:1s22s22p1,同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素,所以C、N、si三种元素的第一电离能由大到小的顺序为:N>C>Si,
故答案为:三;ⅣA;1s22s22p1;N>C>Si;
(2)晶体R中各种微粒间的作用力涉及离子键、共价键、配位键,故答案为:ab;
(3)乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高,故答案为:乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
(4)由反应方程式可知:NO2(g)+SO2(g)=SO3(g)+NO(g),1g SO3(g)放出热量0.52kJ,所以80g三氧化硫放出的热量为:80×0.52kJ=41.6KJ,所以热化学方程式为:NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-41.6KJ/mol,故答案为:NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-41.6KJ/mol;(5)硼砂的化学式为Na2B4O7•10H2O,用H2SO4调pH2~3,硼砂中的Na2B4O7在酸溶液中生成H3BO3 ,反应的离子方程式为:B4O72-+2H++5H2O=4H3BO3,
故答案为:B4O72-+2H++5H2O=4H3BO3.
故答案为:三;ⅣA;1s22s22p1;N>C>Si;
(2)晶体R中各种微粒间的作用力涉及离子键、共价键、配位键,故答案为:ab;
(3)乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高,故答案为:乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
(4)由反应方程式可知:NO2(g)+SO2(g)=SO3(g)+NO(g),1g SO3(g)放出热量0.52kJ,所以80g三氧化硫放出的热量为:80×0.52kJ=41.6KJ,所以热化学方程式为:NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-41.6KJ/mol,故答案为:NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-41.6KJ/mol;(5)硼砂的化学式为Na2B4O7•10H2O,用H2SO4调pH2~3,硼砂中的Na2B4O7在酸溶液中生成H3BO3 ,反应的离子方程式为:B4O72-+2H++5H2O=4H3BO3,
故答案为:B4O72-+2H++5H2O=4H3BO3.
看了B、C、N、O、Si、S是几种...的网友还看了以下:
初一的用方程解应用题,王大伯承包了25亩土地,今年春季改种茄子和西红柿两种大棚蔬菜,用去了4400 2020-04-27 …
初一入门英语翻译句子(每空一词)我不相信那些短袜仅售2元I()believethose()()() 2020-06-11 …
王大伯承包了25亩土地,今年春季改种西红柿与茄子两种大棚蔬菜,用去了44000元,其中种茄子每亩用 2020-06-11 …
每千克价分别为2元,3元,2元4角,4元桔子,苹果,香蕉,柿子四种水果共买了83千克,每千克价分别 2020-06-18 …
高一化学原子结构神末的核外电子数相等的原子一定是()同种元素同种原子质量数相同同位素说法错误()一 2020-07-17 …
下列说法不正确的是()①质子数相同的粒子一定是同一种元素②质子数相同且电子数也相同的两种粒子不可能 2020-07-21 …
如表是元素周期表的一部分,有关说法中正确的是()ⅠAⅡAⅢAⅣAⅤAⅥAVⅡA二abc三defgh 2020-07-23 …
卤族元素包括F、Cl、Br、I等.(1)图1曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 2020-07-29 …
卤族元素包括F、Cl、Br、I等.(1)图1中曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的 2020-07-29 …
下表是元素周期表的一部分,有关说法正确的是[]A.a、b、e、f四种元素的原子半径:e>f>b>aB 2020-11-26 …