早教吧作业答案频道 -->化学-->
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.它易溶于水,难溶于乙醇,加热、遇酸均易分解.工业上常用亚硫酸
题目详情
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.它易溶于水,难溶于乙醇,加热、遇酸均易分解.工业上常用亚硫酸钠法、硫化碱法等制备.
某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图1:
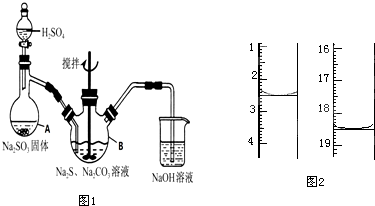
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸.
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体.
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3•5H2O.
④再经过滤、洗涤、干燥,得到所需的产品.
(1)写出仪器A的名称___,步骤④中洗涤时,为了减少产物的损失用的试剂可以是___;
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因___;
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式___;
(4)最后得到的产品中可能含有Na2SO4杂质.请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论___;
(5)测定产品纯度准确称取1.00g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L-1碘的标准溶液滴定.反应原理为2S2O32-+I2═S4O62-+2I-.滴定终点的现象为:___,
滴定起始和终点的液面位置如图2:则消耗碘的标准溶液体积为___ mL,产品的纯度为___.
某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图1:

实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸.
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体.
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3•5H2O.
④再经过滤、洗涤、干燥,得到所需的产品.
(1)写出仪器A的名称___,步骤④中洗涤时,为了减少产物的损失用的试剂可以是___;
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因___;
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式___;
(4)最后得到的产品中可能含有Na2SO4杂质.请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论___;
(5)测定产品纯度准确称取1.00g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L-1碘的标准溶液滴定.反应原理为2S2O32-+I2═S4O62-+2I-.滴定终点的现象为:___,
滴定起始和终点的液面位置如图2:则消耗碘的标准溶液体积为___ mL,产品的纯度为___.
▼优质解答
答案和解析
(1)根据仪器A的结构特点知A的名称为蒸馏烧瓶;产品易溶于水,难溶于乙醇,步骤 ④中洗涤时,为了减少产物的损失用的试剂可以是乙醇;
故答案为:蒸馏烧瓶;乙醇;
(2)Na2S2O3在酸性条件下会生成S和二氧化硫,所以产率会下降,其反应的离子方程式为:S2O32-+2H+=S↓+H2O+SO2↑;
故答案为:S2O32-+2H+=S↓+SO2↑+H2O;
(3)三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式为:4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3;
故答案为:4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3;
(4)检测产品中是否存在Na2SO4的实验方案为:取少量产品溶于足量稀盐酸、静置、取上层清液滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
故答案为:取少量产品溶于足量稀盐酸、静置、取上层清液滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
(5)淀粉遇碘变蓝色,其它物质遇碘不变蓝色,所以滴定终点现象是:滴入最后一滴标准液时,溶液由无色变为蓝色,且半分钟内不再褪色;
消耗碘的标准溶液体积=(18.50-2.50)mL=16.00mL,n(I2)=0.100 0mol•L-1×0.0016L=1.6×10-4mol,根据2S2O32-+I2═S4O62-+2I-可知知n(Na2S2O3•5H2O)=3.2×10-4mol,m(Na2S2O3•5H2O)=0.7936g,产品的纯度为,其纯度=
×100%=79.36%;
故答案为:滴入最后一滴标准液时,溶液由无色变为蓝色,且半分钟内不再褪色;16.00;79.36%.
故答案为:蒸馏烧瓶;乙醇;
(2)Na2S2O3在酸性条件下会生成S和二氧化硫,所以产率会下降,其反应的离子方程式为:S2O32-+2H+=S↓+H2O+SO2↑;
故答案为:S2O32-+2H+=S↓+SO2↑+H2O;
(3)三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式为:4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3;
故答案为:4SO2+2Na2S+Na2CO3=CO2+3Na2S2O3;
(4)检测产品中是否存在Na2SO4的实验方案为:取少量产品溶于足量稀盐酸、静置、取上层清液滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
故答案为:取少量产品溶于足量稀盐酸、静置、取上层清液滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质;
(5)淀粉遇碘变蓝色,其它物质遇碘不变蓝色,所以滴定终点现象是:滴入最后一滴标准液时,溶液由无色变为蓝色,且半分钟内不再褪色;
消耗碘的标准溶液体积=(18.50-2.50)mL=16.00mL,n(I2)=0.100 0mol•L-1×0.0016L=1.6×10-4mol,根据2S2O32-+I2═S4O62-+2I-可知知n(Na2S2O3•5H2O)=3.2×10-4mol,m(Na2S2O3•5H2O)=0.7936g,产品的纯度为,其纯度=
| 0.7936g |
| 1.00g |
故答案为:滴入最后一滴标准液时,溶液由无色变为蓝色,且半分钟内不再褪色;16.00;79.36%.
看了硫代硫酸钠(Na2S2O3•5...的网友还看了以下:
数学题:一卷纸毛重547kg,直径为76cm,纸芯为3kg,纸芯直径为10cm,本卷纸分两次生产完 2020-04-07 …
甲、乙二人分编号分别为001,002,003,…,998,999的999张纸牌,凡编号的三个数码都 2020-05-17 …
甲、乙二人分编号分别为001,002,003,…,998,999的999张纸牌,凡编号的三个数码都 2020-06-14 …
物理兴趣小组在探究纸锥下落的速度与哪些因素有关的实验时,分别做了重量相同的三个不同的纸锥,如图所示 2020-07-05 …
⑧在一张比例尺是10:1的图纸上,量某零件图纸上的长是8厘米,它实际长度是()厘米.⑨如果甲数的3 2020-07-29 …
将420块同样的巧克力装在甲乙两个纸箱中,如果先装满甲纸箱,那么剩余的巧克力装乙纸箱的1/2,如果先 2020-11-10 …
(15分)硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂 2020-11-23 …
硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于 2020-11-23 …
甲、乙二人分编号分别为001,002,003,…,998,999的999张纸牌,凡编号的三个数码都不 2020-12-02 …
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定型剂,也可用于 2020-12-06 …