早教吧作业答案频道 -->化学-->
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大
题目详情
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E,F和C位于同一主族,F处于第一个长周期.
(1)F原子基态的外围核外电子排布式为___;
(2)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为___;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为___;
(4)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH.CH3COONO2(PAN)等二次污染物.
①下列说法正确的是___
A.N2O为直线型分子
B.C、N、O的第一电离能依次增大
C.CH2═CHCHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
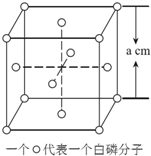
(5)白磷(P4)的晶体属于分子晶体,其晶胞结构如图(小圆圈表示白磷分子).己知晶胞的边长为a cm,阿伏加德罗常数为NA mol-l,则该晶胞中含有的P原子的个数为___,该晶体的密度为___ g•cm-3(用含NA、a的式子表示)

(1)F原子基态的外围核外电子排布式为___;
(2)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为___;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为___;
(4)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH.CH3COONO2(PAN)等二次污染物.
①下列说法正确的是___
A.N2O为直线型分子
B.C、N、O的第一电离能依次增大
C.CH2═CHCHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
(5)白磷(P4)的晶体属于分子晶体,其晶胞结构如图(小圆圈表示白磷分子).己知晶胞的边长为a cm,阿伏加德罗常数为NA mol-l,则该晶胞中含有的P原子的个数为___,该晶体的密度为___ g•cm-3(用含NA、a的式子表示)
▼优质解答
答案和解析
原子序数依次增大的A、B、C、D、E、F六种元素,A的基态原于有3个不同的能级,各能级中的电子数相等,则A是C元素;C的基态原子2p能级上的未成对电子数与A原子的相同,C原子序数大于A,则C为O元素;
B原子序数大于A而小于C,则B是N元素;
E和C位于同一主族,且E原子序数小于25,则C是S元素;
D为它所在周期中原子半径最大的主族元素,原子序数小于S,则D是Na元素;
F的原子序数为29,为Cu元素;
(1)F是Cu元素,其原子核外有29个电子,根据构造原理知Cu元素基态原子的核外电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1,
故答案为:1s22s22p63s23p63d104s1或[Ar]3d104s1;
(2)由C、N、O形成的离子OCN-与CO2互为等电子体,根据二氧化碳结构式知OCN-的结构简式为[N=C=O]-;
故答案为:[N=C=O]-;
(3)在元素C与S所形成的常见化合物CS2中,二硫化碳分子中中心原子价层电子对个数是2且不含孤电子对,所以C原子采用sp杂化;
故答案为:sp;
(4)①A.N2O与CO2是等电子体,二者结构相似,则N2O为直线型分子,故A正确;
B.同一周期元素的第一电离能随着原子序数的增大而呈增大趋势,由于氮原子2p轨道是半满稳定结构,第一电离能高于同周期相邻元素的,所以其第一电离能大小顺序是:N>O>C,故B错误;
C.CH2=CH-CHO分子中每个碳原子均形成三个σ键,没有孤对电子,杂化轨道数目为3,均采用sp2杂化,故C正确;
D.HCOOH分子间能形成氢键,CH3OCH3不能形成分子间氢键,所以相同压强下,HCOOH沸点比CH3OCH3高,故D错误.
故选:AC;
(5)根据均摊法可知,晶胞中P4分子数目为8×
+6×
=4,则晶胞中P原子数目为4×4=16,晶胞质量为16×
g,晶胞体积为(a cm)3,则晶胞密度为
=
g•cm-3;
故答案为:16;
.
B原子序数大于A而小于C,则B是N元素;
E和C位于同一主族,且E原子序数小于25,则C是S元素;
D为它所在周期中原子半径最大的主族元素,原子序数小于S,则D是Na元素;
F的原子序数为29,为Cu元素;
(1)F是Cu元素,其原子核外有29个电子,根据构造原理知Cu元素基态原子的核外电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1,
故答案为:1s22s22p63s23p63d104s1或[Ar]3d104s1;
(2)由C、N、O形成的离子OCN-与CO2互为等电子体,根据二氧化碳结构式知OCN-的结构简式为[N=C=O]-;
故答案为:[N=C=O]-;
(3)在元素C与S所形成的常见化合物CS2中,二硫化碳分子中中心原子价层电子对个数是2且不含孤电子对,所以C原子采用sp杂化;
故答案为:sp;
(4)①A.N2O与CO2是等电子体,二者结构相似,则N2O为直线型分子,故A正确;
B.同一周期元素的第一电离能随着原子序数的增大而呈增大趋势,由于氮原子2p轨道是半满稳定结构,第一电离能高于同周期相邻元素的,所以其第一电离能大小顺序是:N>O>C,故B错误;
C.CH2=CH-CHO分子中每个碳原子均形成三个σ键,没有孤对电子,杂化轨道数目为3,均采用sp2杂化,故C正确;
D.HCOOH分子间能形成氢键,CH3OCH3不能形成分子间氢键,所以相同压强下,HCOOH沸点比CH3OCH3高,故D错误.
故选:AC;
(5)根据均摊法可知,晶胞中P4分子数目为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 31 |
| N A |
| ||
| (acm)3 |
| 496 |
| a3N A |
故答案为:16;
| 496 |
| a3N A |
看了原子序数依次增大的A、B、C、...的网友还看了以下:
如图表示某种蛋白质中相关基团的数目,据图可知该蛋白质()A.由两条肽链组成B.共有126个肽键C. 2020-06-26 …
两个氨基酸脱水缩合形成二肽过程中失去的水中的氢来源于()A.氨基B.羧基C.氨基和羧基D.R基 2020-06-26 …
蛋白质水解时,水中的氢的去向是A.参与形成肽键B.参与形成氨基C.参与形成羧基D.参与形成氨基和羧基 2020-12-15 …
蛋白质水解时,水中的氢的去向是()A.参与形成肽键B.参与形成氨基C.参与形成羧基D.参与形成氨基和 2020-12-15 …
两个氨基酸分子脱水缩合形成二肽时生成一分子水,该分子水中的H来自于A.羧基B.羧基和氨基C.氨基D. 2020-12-28 …
肽键在下列哪两个基团之间形成的()A.磷酸基和羧酸B.羧基和氨基C.醇基和醛基D.醛基和氨基 2020-12-28 …
两个氨基酸分子生成二肽时脱去的水分子中的氧来自于()A.羧基B.氨基C.R基D.羧基和氨基 2020-12-28 …
肽键是在下列哪两个基团之间形成的A.磷酸基和羟基B.羧基和氨基C.醇基和醛基D.醛基和氨基 2020-12-28 …
两个氨基酸分子脱水缩合形成二肽,同时生成一分子水,该水分子中的氢来自()A.氨基B.羧基C.氨基和羧 2020-12-28 …
组成蛋白质的氨基酸的R基()A.与一个氢原子和一个C2H4O2N相连B.约有20种C.至少有一个氨基 2020-12-28 …