早教吧作业答案频道 -->化学-->
兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂.以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如图所示:(1)在
题目详情
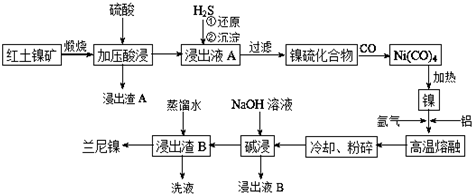
兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂.以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如图所示:
(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___;
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式___;
(3)向浸出液A中通入H2S气体,还原过程中发生反应的离子方程式是___;
(4)“高温熔融”时能否将通入氩气换为CO并说明原因___;
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程中发生反应的离子方程式为___.浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,请用化学反应原理加以解释:___;
(6)浸出液B可以回收,重新生成铝以便循环利用.请设计简单的回收流程:浸出液B→___.(示例:CuOCu2+Cu)

(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___;
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式___;
(3)向浸出液A中通入H2S气体,还原过程中发生反应的离子方程式是___;
(4)“高温熔融”时能否将通入氩气换为CO并说明原因___;
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程中发生反应的离子方程式为___.浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,请用化学反应原理加以解释:___;
(6)浸出液B可以回收,重新生成铝以便循环利用.请设计简单的回收流程:浸出液B→___.(示例:CuOCu2+Cu)
▼优质解答
答案和解析
红土镍矿(主要成分为NiS、FeS和SiO2等)煅烧发生氧化还原反应得到Ni2O3、Fe2O3(SiO2不反应),加入硫酸加压酸浸,Ni2O3、Fe2O3溶解,发生的反应有2Ni2O3+4H2SO4=4NiSO4+O2↑+4H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,SiO2不与硫酸反应,过滤得到浸出渣A(SiO2),浸出液A中含Ni2+、Fe3+,向浸出液A中通入H2S气体,发生还原反应的离子方程式是:H2S+2Fe3+=2Fe2++2H++S,另外生成沉淀NiS,过滤得到镍硫化合物NiS,再通入CO气体,形成Ni(CO)4,加热得到镍,高温熔融时通入氩气,加入铝,得到合金,将合金冷却、粉碎,再用浓氢氧化钠溶液碱浸,铝与氢氧化钠反应产生氢气使镍铝合金产生多孔的结构,浸出液B中含偏铝酸根,最后用蒸馏水洗浸出渣B,得到产品兰尼镍.
(1)通入CO气体,形成Ni(CO)4,在形成Ni(CO)4的过程中,碳元素的化合价没有变化,反应前后都是+2价,氧为-2价,根据化合价代数和为零可知Ni的化合价为0,
故答案为:0;
(2)已知红土镍矿煅烧后生成Ni2O3,加压酸浸后浸出液A中含有Ni2+,镍的化合价降低发生还原反应,只有氧的化合价能升高,所以产物有氧气,则发生的反应是2Ni2O3+4H2SO4=4NiSO4+O2↑+4H2O,
故答案为:2Ni2O3+4H2SO4=4NiSO4+O2↑+4H2O;
(3)浸出液A中含Ni2+、Fe3+,向浸出液A中通入H2S气体,三价铁具有较强氧化性,与硫化氢发生还原反应,离子方程式是:H2S+2Fe3+=2Fe2++2H++S↓,
故答案为:H2S+2Fe3+=2Fe2++2H++S↓;
(4)高温熔融时通入氩气,加入铝,得到合金,不能把氩气换为CO,因为冷却时,CO能与Ni反应生成Ni(CO)4,
故答案为:不能,因为冷却时,CO能与Ni反应生成Ni(CO)4;
(5)将合金冷却、粉碎,再用浓氢氧化钠溶液碱浸,铝与氢氧化钠反应产生氢气使镍铝合金产生多孔的结构,发生的反应为:2Al+2OH-+2H2O=2AlO2-+3H2↑;浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,因为Al溶于碱液生成AlO2-时在水中存在下列平衡:AlO2-+2H2O⇌Al(OH)3+OH-,OH-浓度过小,对AlO2-的水解的抑制作用小,所以,产生的Al(OH)3就会沉积下来进而阻止浸出反应持续进行,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;因为Al溶于碱液生成AlO2-时在水中存在下列平衡:AlO2-+2H2O⇌Al(OH)3+OH-,OH-浓度过小,对AlO2-的水解的抑制作用小,所以,产生的Al(OH)3就会沉积下来进而阻止浸出反应持续进行;
(6)浸出液B中含偏铝酸根,可通入过量二氧化碳得到氢氧化铝沉淀,再加热灼烧使其分解得到氧化铝,加入冰晶石,在熔融态下电解氧化铝得到铝,回收流程可表示为:浸出液B→Al(OH)3
Al2O3
Al,
故答案为:Al(OH)3
Al2O3
Al.
(1)通入CO气体,形成Ni(CO)4,在形成Ni(CO)4的过程中,碳元素的化合价没有变化,反应前后都是+2价,氧为-2价,根据化合价代数和为零可知Ni的化合价为0,
故答案为:0;
(2)已知红土镍矿煅烧后生成Ni2O3,加压酸浸后浸出液A中含有Ni2+,镍的化合价降低发生还原反应,只有氧的化合价能升高,所以产物有氧气,则发生的反应是2Ni2O3+4H2SO4=4NiSO4+O2↑+4H2O,
故答案为:2Ni2O3+4H2SO4=4NiSO4+O2↑+4H2O;
(3)浸出液A中含Ni2+、Fe3+,向浸出液A中通入H2S气体,三价铁具有较强氧化性,与硫化氢发生还原反应,离子方程式是:H2S+2Fe3+=2Fe2++2H++S↓,
故答案为:H2S+2Fe3+=2Fe2++2H++S↓;
(4)高温熔融时通入氩气,加入铝,得到合金,不能把氩气换为CO,因为冷却时,CO能与Ni反应生成Ni(CO)4,
故答案为:不能,因为冷却时,CO能与Ni反应生成Ni(CO)4;
(5)将合金冷却、粉碎,再用浓氢氧化钠溶液碱浸,铝与氢氧化钠反应产生氢气使镍铝合金产生多孔的结构,发生的反应为:2Al+2OH-+2H2O=2AlO2-+3H2↑;浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,因为Al溶于碱液生成AlO2-时在水中存在下列平衡:AlO2-+2H2O⇌Al(OH)3+OH-,OH-浓度过小,对AlO2-的水解的抑制作用小,所以,产生的Al(OH)3就会沉积下来进而阻止浸出反应持续进行,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;因为Al溶于碱液生成AlO2-时在水中存在下列平衡:AlO2-+2H2O⇌Al(OH)3+OH-,OH-浓度过小,对AlO2-的水解的抑制作用小,所以,产生的Al(OH)3就会沉积下来进而阻止浸出反应持续进行;
(6)浸出液B中含偏铝酸根,可通入过量二氧化碳得到氢氧化铝沉淀,再加热灼烧使其分解得到氧化铝,加入冰晶石,在熔融态下电解氧化铝得到铝,回收流程可表示为:浸出液B→Al(OH)3
| 灼烧 |
| 冰晶石、熔融 |
| 电解 |
故答案为:Al(OH)3
| 灼烧 |
| 冰晶石、熔融 |
| 电解 |
看了兰尼镍是一种带有多孔结构的细小...的网友还看了以下:
关于元素P的问题P的氧化物和热水反应的产物为什么(化学式)为什么要用6molNaOH才能完全中和为 2020-05-02 …
交流自己对祖国西部的感受急!明天就要用!( ⊙ o ⊙ )啊! 2020-05-17 …
实验室常用锌和稀硫酸反应制取氢气,同时生成硫酸锌.现在要制取氢气0.3g,需要锌的质量多少克?同时 2020-05-17 …
关于用氢氟酸做土壤消解的问题:玻璃的主要成分是二氧化硅,土壤消解要用到氢氟酸去除飞硅,用玻璃吸管去 2020-05-17 …
氢氧化钾要多少水可以完全解离做液体皂的时候要用水来溶解氢氧化钾,虽然可以用到氢氧化钾的3倍的水,但 2020-06-18 …
英语时刻表达,只有在整点时才有必要用O'clock吗? 2020-07-05 …
实验室用铝与氢氧化钠溶液反应也能制o氢气,反应b化学方程式为:b个1+bN个OH+bHbO=bN个 2020-07-09 …
关于H20与HF的沸点问题氢键的形成是因为有两个电负性很强的分子之间互相作用,而氢键能决定他们的溶点 2020-11-21 …
问一个英语问题看到练习册上翻译“军队正在向敌军营地前进”参考答案是:Thetroopsareadva 2020-11-21 …
氢化钙(CaH2)是一种重要的制氢剂,用它和水反应生成氢氧化钙和氢气,氢气供燃烧之需.请回答:(1) 2021-02-09 …