早教吧作业答案频道 -->化学-->
过碳酸钠(2Na2CO3•3H2O2)广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习:资料卡片:①过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解;
题目详情
过碳酸钠(2Na2CO3•3H2O2)广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习:
【资料卡片】:
①过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解;
②过碳酸钠分解的化学方程式为2(2Na2CO3•3H2O2)
4Na2CO3+6H2O+3O2↑
③H2O2分解放出热量,Na2CO3受热不分解;
I、制备研究:工业上采用“醇析法”将其转化成固态的过碳酸钠晶体(化学式为2Na2CO3•3H2O2),“醇析法”的生产工艺流程如下:
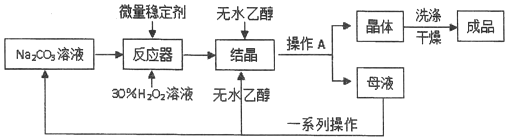
请回答问题:
(1)Na2CO3俗名:___;其水溶液能使酚酞变___;
(2)H2O2受热容易分解,写出该分解反应的方程式:___;
(3)生产过程中,反应及干澡均需在低温度下进行,原因是___;
(4)生产过程中,加入较多无水乙醇后,过碳酸钠晶体大量析出,此无水乙醇的作用可能是___;
(5)操作A的名称是___,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒和___;
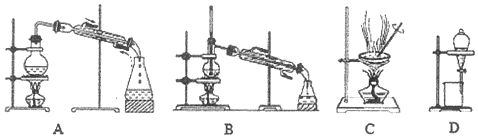
(6)母液可以循环使用,但须进行“一系列操作”分离,这些操作包括:加入少里___,不再有气泡产生后,过滤,将所得滤液再进行___(填操作名称),即可得Na2CO3溶液和95%的乙醇.为获取无水乙醇,还需进行的操作是:向95%的乙醇中加入足量CaO后,选___(填序号)装置进行实验.
II、纯度测定:兴趣小组同学设计了如图1所示实验装置(部分仪器略去),测定过碳酸钠样品中2Na2CO3•3H2O2的质量分数.步骤如下:
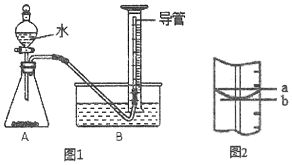
①连接仪器并检查好气密性
②将过碳酸钠样品(2.20g)和少许MnO2均匀混合后置于装置A中,在量筒中加满水;
③连接仪器,打开滴液漏斗活塞,缓缓滴入水;
④待装置A中___时,停止滴加水,并关闭活塞;
⑤冷却至室温后,平视读数;
⑥根据数据进行计算.
请回答下列问题:
(7)完善实验步骤的相关内容:④___;
(8)第⑤中,已“冷却至室温”的判断依据是:___;
(9)量筒中,加装的长导管的作用是:___;
(10)实验中,___,则开始收集气体;
A.刚开始出现气泡时
B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(11)量筒的局部示意见图2,平视读数时应沿___视线(选填“a”或“b”) 进行.图中___视线(选填“a”或“b”)对应的读数较大.
(12)若量筒中收集到气体的体积是224mL (己转化为标准状况下的数据),计算过碳酸钠样品中2Na2CO3•3H2O2的质量分数:___;[Mr(O2)=32、Mr(2Na2CO3•3H2O2)=314]
(13)经过讨论,小组同学一致认为测定结果偏大,理由是___(任写一种).
【资料卡片】:
①过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解;
②过碳酸钠分解的化学方程式为2(2Na2CO3•3H2O2)
| ||
③H2O2分解放出热量,Na2CO3受热不分解;
I、制备研究:工业上采用“醇析法”将其转化成固态的过碳酸钠晶体(化学式为2Na2CO3•3H2O2),“醇析法”的生产工艺流程如下:

请回答问题:
(1)Na2CO3俗名:___;其水溶液能使酚酞变___;
(2)H2O2受热容易分解,写出该分解反应的方程式:___;
(3)生产过程中,反应及干澡均需在低温度下进行,原因是___;
(4)生产过程中,加入较多无水乙醇后,过碳酸钠晶体大量析出,此无水乙醇的作用可能是___;
(5)操作A的名称是___,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒和___;
(6)母液可以循环使用,但须进行“一系列操作”分离,这些操作包括:加入少里___,不再有气泡产生后,过滤,将所得滤液再进行___(填操作名称),即可得Na2CO3溶液和95%的乙醇.为获取无水乙醇,还需进行的操作是:向95%的乙醇中加入足量CaO后,选___(填序号)装置进行实验.

II、纯度测定:兴趣小组同学设计了如图1所示实验装置(部分仪器略去),测定过碳酸钠样品中2Na2CO3•3H2O2的质量分数.步骤如下:

①连接仪器并检查好气密性
②将过碳酸钠样品(2.20g)和少许MnO2均匀混合后置于装置A中,在量筒中加满水;
③连接仪器,打开滴液漏斗活塞,缓缓滴入水;
④待装置A中___时,停止滴加水,并关闭活塞;
⑤冷却至室温后,平视读数;
⑥根据数据进行计算.
请回答下列问题:
(7)完善实验步骤的相关内容:④___;
(8)第⑤中,已“冷却至室温”的判断依据是:___;
(9)量筒中,加装的长导管的作用是:___;
(10)实验中,___,则开始收集气体;
A.刚开始出现气泡时
B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(11)量筒的局部示意见图2,平视读数时应沿___视线(选填“a”或“b”) 进行.图中___视线(选填“a”或“b”)对应的读数较大.
(12)若量筒中收集到气体的体积是224mL (己转化为标准状况下的数据),计算过碳酸钠样品中2Na2CO3•3H2O2的质量分数:___;[Mr(O2)=32、Mr(2Na2CO3•3H2O2)=314]
(13)经过讨论,小组同学一致认为测定结果偏大,理由是___(任写一种).
▼优质解答
答案和解析
(1)Na2CO3俗名为纯碱,其水溶液中碳酸根离子水解,能使溶液呈碱性,所以其水溶液能使酚酞变红,
故答案为:纯碱;红;
(2)H2O2受热容易分解,生成水和氧气,反应的化学方程式为2H2O2
2H2O+O2↑,
故答案为:2H2O2
2H2O+O2↑;
(3)H2O2和2Na2CO3•3H2O2不稳定,受热易分解,所以生产过程中,反应及干澡均需在低温度下进行,防止其分解,
故答案为:H2O2和2Na2CO3•3H2O2受热都容易分解;
(4)过碳酸钠在乙醇中的溶解度较小,所以实验过程中用无水乙醇能降低过碳酸钠溶解度,
故答案为:无水乙醇能降低过碳酸钠溶解度;
(5)操作A为分离不溶于液体的固体和液体,所以操作A为过滤,过滤时用到的玻璃仪器是烧杯、玻璃棒和漏斗,
故答案为:过滤;漏斗;
(6)母液里主要是过碳酸钠和乙醇,要使所含有的物质可以循环使用,要先将过碳酸钠分解得到碳酸钠,再进行蒸馏,可得Na2CO3溶液和95%的乙醇,要使过碳酸钠分解,要加MnO2做催化剂,然后再过滤将二氧化锰除去,将95%的乙醇变为无水乙醇,要向95%的乙醇中加入足量CaO后,再进行蒸馏,所以要选择A装置,
故答案为:MnO2;蒸馏;A;
(7)根据实验原理可知,要将过碳酸钠充分分解才能停止加水,过碳酸钠分解时有氧气产生,可以根据是否有气体产生判断过碳酸钠分解是否完全,所以步骤④为待装置A中无气泡冒出(或无明显现象)时,停止滴加水,并关闭活塞,
故答案为:无气泡冒出(或无明显现象);
(8)根据装置图可知,当气体热胀冷缩时,量筒中液面会发生变化,所以第⑤中,已“冷却至室温”的判断依据是量筒内液面不再变化,
故答案为:量筒内液面不再变化;
(9)如果使用短导管由于温度降低后会使水沿着导管倒吸入锥形瓶内,所以量筒中长导管的作用是起缓冲作用,防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量,
故答案为:防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量;
(10)开始锥形瓶中有空气,最后锥形瓶中留有制取的氧气,两者体积相同,所以一开始就应当收集,故选A;
(11)读取量筒中液体体积时应使液体的凹液面与刻度线水平,所以平视读数时应沿b视线 进行,量筒的小刻度在度部,而实验中量筒是倒置的,所以图中b视线对应的读数较大,
故答案为:b;b;
(12)根据题意可知量筒中收集到气体的体积是224mL,即氧气的物质的量为0.01mol,设样品中的过碳酸钠的质量为Y则:
2(2Na2CO3•3H2O2)═4Na2CO3+6H2O+3O2↑
628 3mol
Y 0.01mol
根据:
=
解得Y=2.09g,所以样品中2Na2CO3•3H2O2的质量分数为:
×100%=95.0%,
故答案为:95.0%;
(13)根据装置图可知,当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,使测量的气体体积偏大,会导致测得的氧气的体积偏大,所以会使测定结果偏大,
故答案为:当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,使测量的气体体积偏大.
故答案为:纯碱;红;
(2)H2O2受热容易分解,生成水和氧气,反应的化学方程式为2H2O2
| ||
故答案为:2H2O2
| ||
(3)H2O2和2Na2CO3•3H2O2不稳定,受热易分解,所以生产过程中,反应及干澡均需在低温度下进行,防止其分解,
故答案为:H2O2和2Na2CO3•3H2O2受热都容易分解;
(4)过碳酸钠在乙醇中的溶解度较小,所以实验过程中用无水乙醇能降低过碳酸钠溶解度,
故答案为:无水乙醇能降低过碳酸钠溶解度;
(5)操作A为分离不溶于液体的固体和液体,所以操作A为过滤,过滤时用到的玻璃仪器是烧杯、玻璃棒和漏斗,
故答案为:过滤;漏斗;
(6)母液里主要是过碳酸钠和乙醇,要使所含有的物质可以循环使用,要先将过碳酸钠分解得到碳酸钠,再进行蒸馏,可得Na2CO3溶液和95%的乙醇,要使过碳酸钠分解,要加MnO2做催化剂,然后再过滤将二氧化锰除去,将95%的乙醇变为无水乙醇,要向95%的乙醇中加入足量CaO后,再进行蒸馏,所以要选择A装置,
故答案为:MnO2;蒸馏;A;
(7)根据实验原理可知,要将过碳酸钠充分分解才能停止加水,过碳酸钠分解时有氧气产生,可以根据是否有气体产生判断过碳酸钠分解是否完全,所以步骤④为待装置A中无气泡冒出(或无明显现象)时,停止滴加水,并关闭活塞,
故答案为:无气泡冒出(或无明显现象);
(8)根据装置图可知,当气体热胀冷缩时,量筒中液面会发生变化,所以第⑤中,已“冷却至室温”的判断依据是量筒内液面不再变化,
故答案为:量筒内液面不再变化;
(9)如果使用短导管由于温度降低后会使水沿着导管倒吸入锥形瓶内,所以量筒中长导管的作用是起缓冲作用,防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量,
故答案为:防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量;
(10)开始锥形瓶中有空气,最后锥形瓶中留有制取的氧气,两者体积相同,所以一开始就应当收集,故选A;
(11)读取量筒中液体体积时应使液体的凹液面与刻度线水平,所以平视读数时应沿b视线 进行,量筒的小刻度在度部,而实验中量筒是倒置的,所以图中b视线对应的读数较大,
故答案为:b;b;
(12)根据题意可知量筒中收集到气体的体积是224mL,即氧气的物质的量为0.01mol,设样品中的过碳酸钠的质量为Y则:
2(2Na2CO3•3H2O2)═4Na2CO3+6H2O+3O2↑
628 3mol
Y 0.01mol
根据:
| 628 |
| Y |
| 3 |
| 0.01 |
| 2.09 |
| 2.20 |
故答案为:95.0%;
(13)根据装置图可知,当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,使测量的气体体积偏大,会导致测得的氧气的体积偏大,所以会使测定结果偏大,
故答案为:当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,使测量的气体体积偏大.
看了过碳酸钠(2Na2CO3•3H...的网友还看了以下:
有一在空气中暴露过的KOH固体,经分析知其内含水7.60%、K2CO32.38%、K0H90%,若 2020-05-13 …
病人已被告知要继续他的治疗用英文翻译 2020-06-02 …
有某未知浓度的盐酸25ML,能跟20ML某浓度的NaOH溶液完全反应,若先用0.1克CaCO3与2 2020-06-27 …
有未知浓度的盐酸25mL,能跟20mL某浓度的NaOH溶液完全反应,若先用0.1g CaCO3与2 2020-06-27 …
自制酸奶出现沉淀分离学的是生物技术,主要方向就是发酵类……是这样的,我用奶粉做的酸奶,用的菌种是泡 2020-07-24 …
半胱氨酸的料测浓度怎么测怎么计算!其实我对这个问题本生就很模糊!我是“半路出家”的化验员对浓度的概念 2020-11-13 …
有一在空气中暴露过的KOH固体,经分析知其中水7.60%,碳酸钾2.38%,KOH90%.若将此析知 2020-12-03 …
用C、H、O、Ca、Na、Cl等元素组成的化学式填写:用于急救病人的气体;用于灭火的气体;清洗铁锈用 2020-12-19 …
下列有关物质的用途说法正确的是()①熟石灰可用来改良土壤酸性②氦气可做保护气③干冰可作制冷剂④蒸馒头 2020-12-20 …
2005年10月以来,禽流感呈现出在全球蔓延的趋势.国际卫生组织推荐“达菲“作为治疗禽流感药品之一. 2021-01-02 …