早教吧作业答案频道 -->化学-->
工业上用软锰矿(主要成分MnO2,杂质金属元素Fe、Al等)制备MnSO4•H2O的一种工艺流程如图1已知:1.浸出过程中发生的主要反应化学方程式为:MnO2+SO2=MnSO42.浸出液中阳离子主要有Mn2+、Fe2+
题目详情
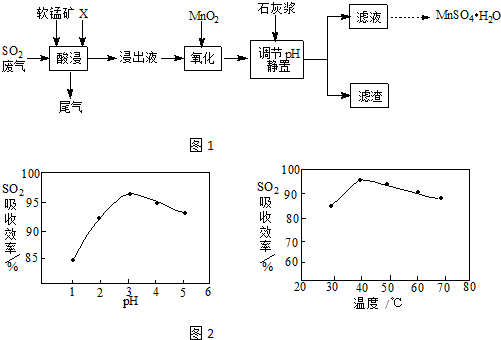
工业上用软锰矿(主要成分MnO2,杂质金属元素Fe、Al等) 制备MnSO4•H2O 的一种工艺流程如图1
已知:
1.浸出过程中发生的主要反应化学方程式为:MnO2+SO2=MnSO4
2.浸出液中阳离子主要有Mn2+、Fe2+、Al3+等
回答下列问题:
(1)物质X最好选用 ___
a.盐酸b.硫酸c.硝酸
(2)酸浸时SO2的吸收效率与pH、温度的关系如图2所示,为提高SO2的吸收效率,酸浸适宜的条件是___
(3)流程中“氧化”步骤主要反应的离子方程式是 ___
(4)加入石灰浆调节pH,可将氧化后的浸出液中Fe3+、Al3+形成氢氧化物除去.检验Fe3+是否除尽的最佳方法是 ___.
(5)用MnSO4可测定水中溶解氧,方法是:取100mL 水样,迅速加入足量MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用5.00×10-3mol•L-1Na2S2O3溶液和I2反应,当消耗Na2S2O3溶液 12.0mL时反应完全.有关化学反应方程式如下:
①2Mn2++O2+4OH-=2MnO(OH)2(反应很快);
②MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;
③I2+2S2O32-=S4O62-+2I-.
计算水样中溶解氧的浓度(以mg•L-1为单位)___mg.L-1.

已知:
1.浸出过程中发生的主要反应化学方程式为:MnO2+SO2=MnSO4
2.浸出液中阳离子主要有Mn2+、Fe2+、Al3+等
回答下列问题:
(1)物质X最好选用 ___
a.盐酸b.硫酸c.硝酸
(2)酸浸时SO2的吸收效率与pH、温度的关系如图2所示,为提高SO2的吸收效率,酸浸适宜的条件是___
(3)流程中“氧化”步骤主要反应的离子方程式是 ___
(4)加入石灰浆调节pH,可将氧化后的浸出液中Fe3+、Al3+形成氢氧化物除去.检验Fe3+是否除尽的最佳方法是 ___.
(5)用MnSO4可测定水中溶解氧,方法是:取100mL 水样,迅速加入足量MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用5.00×10-3mol•L-1Na2S2O3溶液和I2反应,当消耗Na2S2O3溶液 12.0mL时反应完全.有关化学反应方程式如下:
①2Mn2++O2+4OH-=2MnO(OH)2(反应很快);
②MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;
③I2+2S2O32-=S4O62-+2I-.
计算水样中溶解氧的浓度(以mg•L-1为单位)___mg.L-1.
▼优质解答
答案和解析
(1)物质X最好选用硫酸,不引入杂质,故答案为:b;
(2)由图可知,提高SO2的吸收效率,酸浸适宜的条件为pH控制在3左右、温度控制在40℃左右,
故答案为:pH控制在3左右、温度控制在40℃左右;
(3)流程中“氧化”步骤主要反应的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(4)检验Fe3+是否除尽的最佳方法是取上层清液少许,向其中滴加少许KSCN溶液,若溶液未出现血红色,则Fe3+除尽,
故答案为:取上层清液少许,向其中滴加少许KSCN溶液,若溶液未出现血红色,则Fe3+除尽;
(5)n(S2O32-)=5.00×10-3mol•L-1×12.0 mL=6.00×10-5 mol,
O2~4 S2O32-
1 4
n(O2) 6.00×10-5 mol
n(O2)=
=1.50×10-5 mol,
水样中溶解氧的浓度为
=4.80 mg•L-1,
故答案为:4.80.
(2)由图可知,提高SO2的吸收效率,酸浸适宜的条件为pH控制在3左右、温度控制在40℃左右,
故答案为:pH控制在3左右、温度控制在40℃左右;
(3)流程中“氧化”步骤主要反应的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(4)检验Fe3+是否除尽的最佳方法是取上层清液少许,向其中滴加少许KSCN溶液,若溶液未出现血红色,则Fe3+除尽,
故答案为:取上层清液少许,向其中滴加少许KSCN溶液,若溶液未出现血红色,则Fe3+除尽;
(5)n(S2O32-)=5.00×10-3mol•L-1×12.0 mL=6.00×10-5 mol,
O2~4 S2O32-
1 4
n(O2) 6.00×10-5 mol
n(O2)=
| 1×6.00×10-5mol |
| 4 |
水样中溶解氧的浓度为
| 1.5×10-5mol×32g/mol×1000mg/g |
| 0.1L |
故答案为:4.80.
看了工业上用软锰矿(主要成分MnO...的网友还看了以下:
中国矿产资源的优势是()A.矿产种类比较齐全B.主要矿产资源贫矿少,富矿多C.矿产资源分布较均匀D 2020-04-06 …
读黄土高原各类矿产潜在价值所占比例表,完成问题。矿产种类各类矿产潜在价值占总价值的百分(%)能源矿 2020-04-06 …
有两种矿,一种是53度,一种是62度.我想把两种矿配在一起,最终成为60度.两种矿的比例分别是多少 2020-06-04 …
某同学准备参加暑期勤工俭学体验活动,制作A,B,C三种手工艺品共10件,且应满足C种手工艺品数量是 2020-06-20 …
南瓜的种子如何处理?南瓜播种前种子处理,一般用50至55摄氏度温汤浸种,后用清水浸种8至12小时, 2020-06-21 …
四年级科学题填空题我国已发现各种矿产种,这些矿产资源属于,任何和个人不得私四年级科学题填空题我国已 2020-06-30 …
(2014•徐州)小明家有一个镶嵌玉石的铜制工艺品,在实验室中用测出工艺品的质量为141g,已知其 2020-07-01 …
小明的妈妈到某工艺品商店买了一件用铝制成的工艺品,如图,小明通过实验测出工艺品的质量为243g,测 2020-07-19 …
有故事书、科技书、文艺书三种书,其中故事书是总数的2/5,科技书是故事书的7/8,其余是文艺书,故事 2020-12-12 …
关于西南区发展有利条件的正确叙述是……………………………………………()A.矿产种类多,但储量不大B 2021-01-13 …