早教吧作业答案频道 -->化学-->
工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-.为除去杂质离子,部分操作流程如下图:请回答问题:(1)用稀硫酸浸泡某矿石后的溶液中
题目详情
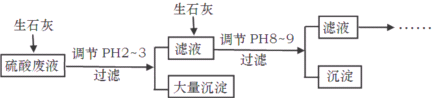
工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-.为除去杂质离子,部分操作流程如下图:
请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9g•L-1,则该溶液的pH约为___
(2)NH4+在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在.现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH4+)恰好是NH4Cl溶液中c(NH4+)的2倍,则c[(NH4)2SO4]___c(NH4Cl)(填:<、=或>)
(3)向废液中投入生石灰(忽略溶液温度的变化),溶液中c(NH3•H2O)与c(OH-)的比值(填“增大”、“减小”或“不变”)___
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],提纯CaSO4•2H2O的主要操作步骤:向沉淀中加入过量___充分反应后,过滤、洗涤、
(5)25℃,H3AsO4电离常数为K1=5.6×10-3 ,K2=1.7×10-7,K3=4.0×10-12.当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2
①Na3AsO4第一步水解的平衡常数数值为:___
②已知:AsO43-+2I-+2H+═AsO33-+I2+H2O,SO2+I2+2H2O═SO42-+2I-+4H+.上述两个反应中还原性最强的微粒是___.

请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9g•L-1,则该溶液的pH约为___
(2)NH4+在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在.现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH4+)恰好是NH4Cl溶液中c(NH4+)的2倍,则c[(NH4)2SO4]___c(NH4Cl)(填:<、=或>)
(3)向废液中投入生石灰(忽略溶液温度的变化),溶液中c(NH3•H2O)与c(OH-)的比值(填“增大”、“减小”或“不变”)___
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],提纯CaSO4•2H2O的主要操作步骤:向沉淀中加入过量___充分反应后,过滤、洗涤、
(5)25℃,H3AsO4电离常数为K1=5.6×10-3 ,K2=1.7×10-7,K3=4.0×10-12.当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2
①Na3AsO4第一步水解的平衡常数数值为:___
②已知:AsO43-+2I-+2H+═AsO33-+I2+H2O,SO2+I2+2H2O═SO42-+2I-+4H+.上述两个反应中还原性最强的微粒是___.
▼优质解答
答案和解析
硫酸废液中含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-,加入生石灰,调节pH2~3,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],滤液加入生石灰调节pH8~9,生成Ca3(AsO4)2沉淀,滤液主要含有(NH4)2SO4和NH4Cl,
(1)硫酸的浓度为4.9g•L-1,c(H2SO4)=
=0.05mol/L,c(H+)=0.1mol/L,pH=-lg0.1=1,故答案为:1;
(2)如c[(NH4)2SO4]=c(NH4Cl),则(NH4)2SO4溶液中c(NH4+)较大,因c(NH4+)越大,NH4+水解程度越小,则(NH4)2SO4溶液中c(NH4+)小于是NH4Cl溶液中c(NH4+)的2倍,如等于2倍,则c(NH4Cl)应较大,
故答案为:<;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小,则溶液中
减小,故答案为:减小;
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,且防止CaSO4•2H2O的溶解,过滤后洗涤、干燥,
故答案为:稀硫酸;晾干或干燥;
(5)①Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O⇌HAsO42-+OH-,该步水解的平衡常数Kh=
=
=
=
=2.5×10-3,
故答案为:2.5×10-3;
②已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.还原剂还原性大于还原产物的还原性,则还原性SO2>I->AsO33-,两个反应中还原性最强的微粒是SO2,
故答案为:SO2.
(1)硫酸的浓度为4.9g•L-1,c(H2SO4)=
| ||
| 1L |
(2)如c[(NH4)2SO4]=c(NH4Cl),则(NH4)2SO4溶液中c(NH4+)较大,因c(NH4+)越大,NH4+水解程度越小,则(NH4)2SO4溶液中c(NH4+)小于是NH4Cl溶液中c(NH4+)的2倍,如等于2倍,则c(NH4Cl)应较大,
故答案为:<;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小,则溶液中
| [NH3•H2O] |
| [OH-] |
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,且防止CaSO4•2H2O的溶解,过滤后洗涤、干燥,
故答案为:稀硫酸;晾干或干燥;
(5)①Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O⇌HAsO42-+OH-,该步水解的平衡常数Kh=
| c(HAsO42-)•c(OH -) |
| c(AsO 4 3-) |
| c(HAsO4 2-)•c(OH-)•c(H +) |
| c(AsO4 3-)•c(H +) |
| Kw |
| K3 |
| 10 -14 |
| 4.0×10 -12 |
故答案为:2.5×10-3;
②已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.还原剂还原性大于还原产物的还原性,则还原性SO2>I->AsO33-,两个反应中还原性最强的微粒是SO2,
故答案为:SO2.
看了工厂中用稀硫酸浸泡某矿石后的溶...的网友还看了以下:
石块A自塔顶自由落下h时,石块B自离塔顶H处自由落下,两石块同时落地,则塔高为多少? 2020-05-20 …
变限积分求道问题对函数f(t+h)-f(t-h)在[-h,h]上的积分对h求导.F(h)=∫[-h 2020-05-23 …
已知A是生产生活中用量最大的金属,B为淡黄色粉末.在常温下C为无色液体,E、G、H、I、J为气体, 2020-07-08 …
如图所示,2013年2月15日,一颗数十吨的陨石被地球俘获,在加速下落的过程中,陨石与大气剧烈摩擦 2020-07-12 …
下列有关试验的现象描述中不正确的是()A.在碳酸钠溶液中滴加石蕊,石蕊呈现蓝色B.在硬水中加入肥皂 2020-07-15 …
zn和c是不是永远都是zn做负极?其中有个对比是这个样子的.原电池构成部分对比:0.53mol/L 2020-07-29 …
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进 2020-12-04 …
小明注意到家中灯泡比平时亮,猜测可能电压不稳.于是做了如下探究:关闭家中其他电器,只开一只“220V 2020-12-20 …
今天(6月26日)为世界禁毒日,一百多年前虎门销烟的壮举是中国禁毒史上的辉煌篇章.在虎门销烟中,人们 2021-01-08 …
(2005•长沙)长沙市的主要矿产资源有()A.石油、金刚石B.煤炭、黄金C.金刚石、菊花石D.菊花 2021-01-22 …