早教吧作业答案频道 -->化学-->
“低碳经济”备受关注,CO2的有效开发利用成为科学家研究的重要课题.(1)已知:CO2(g)+2H2(g)⇌C(s)+2H2O(g)△H=-90.0kJ•mol-1H2O(1)═H2O(g)△H=+44.0kJ•mol-1C(s)的燃烧热△H=-394.0
题目详情
“低碳经济”备受关注,CO2的有效开发利用成为科学家研究的重要课题.
(1)已知:
CO2(g)+2H2(g)⇌C(s)+2H2O(g)△H=-90.0kJ•mol-1
H2O(1)═H2O(g)△H=+44.0kJ•mol-1
C(s)的燃烧热△H=-394.0kJ•mol-1
则表示H2燃烧热的热化学方程式为___.
(2)在0.1MPa、Ru/TiO2催化下,将H2和CO2按投料比
=4:1置于恒压密闭容器中发生反应:
反应I CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)△H1
反应II CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2
测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示.
(选择性:转化的CO2中生成CH4或CO的百分比)
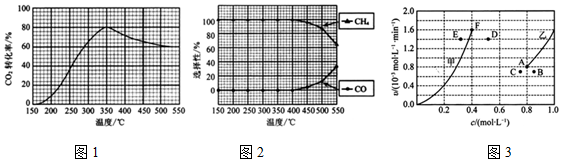
①反应I的△H1___ (填“>”、“<“或“=”)0;理由是___.
②温度过高或过低均不利于反应I的进行,原因是___.
③350℃时,反应I的平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
④为减少CO在产物中的比率,可采取的措施有___(列举一条).
(3)为探究反应I的反应速率与浓度的关系,向恒容密闭容器中通入浓度均为1.0mol•L-1的H2与CO2.根据相关数据绘制出反应速率与浓度关系曲线:v正~c(CO2)和v逆~c(H2O).则与曲线v正~c(CO2)相对应的是图3曲线___(填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线甲对应的平衡点可能为___(填字母,下同),曲线乙对应的平衡点可能为___.
(1)已知:
CO2(g)+2H2(g)⇌C(s)+2H2O(g)△H=-90.0kJ•mol-1
H2O(1)═H2O(g)△H=+44.0kJ•mol-1
C(s)的燃烧热△H=-394.0kJ•mol-1
则表示H2燃烧热的热化学方程式为___.
(2)在0.1MPa、Ru/TiO2催化下,将H2和CO2按投料比
| n(H2) |
| n(CO2) |
反应I CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)△H1
反应II CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2
测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示.
(选择性:转化的CO2中生成CH4或CO的百分比)

①反应I的△H1___ (填“>”、“<“或“=”)0;理由是___.
②温度过高或过低均不利于反应I的进行,原因是___.
③350℃时,反应I的平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
④为减少CO在产物中的比率,可采取的措施有___(列举一条).
(3)为探究反应I的反应速率与浓度的关系,向恒容密闭容器中通入浓度均为1.0mol•L-1的H2与CO2.根据相关数据绘制出反应速率与浓度关系曲线:v正~c(CO2)和v逆~c(H2O).则与曲线v正~c(CO2)相对应的是图3曲线___(填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线甲对应的平衡点可能为___(填字母,下同),曲线乙对应的平衡点可能为___.
▼优质解答
答案和解析
(1)①CO2(g)+2H2(g)⇌C(s)+2H2O(g)△H=-90.0kJ/mol
②H2O(1)═H2O(g)△H=+44.0kJ/mol
C(s)的燃烧热△H=-394.0kJ•mol-1,故热化学方程式为③C(s)+O2(g)=CO2(g)△H=-394.0kJ/mol
×①+
×③-②得,H2(g)+
O2(g)=H2O(l)△H=-286KJ/mol,
故答案为:H2(g)+
O2(g)=H2O(l)△H=-286KJ/mol;
(2)①反应Ⅰ达到平衡状态后,随温度升高二氧化碳平衡转化率减小,说明正反应为放热反应,故<0;原因是反应Ⅰ达到平衡状态后,随温度升高二氧化碳平衡转化率减小,说明正反应为放热反应,
故答案为:<;反应Ⅰ达到平衡状态后,随温度升高二氧化碳平衡转化率减小,说明正反应为放热反应;
②温度过高或过低均不利于反应I的进行,原因是:温度过低,化学反应速率慢,温度过高反应Ⅰ向逆反应方向进行且CH4的选择性减小,
故答案为:温度过低,化学反应速率慢,温度过高反应Ⅰ向逆反应方向进行且CH4的选择性减小;
③CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
开始(n) 1 4 0 0
变化 0.8 3.2 0.8 1.6
平衡 0.2 0.8 0.8 1.6,则p(CO2)=
×0.1MPa=
MPa,p(H2)=
×0.1MPa=
MPa,p(CH4)=
×0.1MPa=
MPa,p(H2O)=
×0.1MPa=
MPa,则Kp=
=
=2.89×104(MPa)-2,
故答案为:2.89×104(MPa)-2;
④由图象得,为减少CO在产物中的比率,可采取的措施有降低温度或增加压强,
故答案为:降低温度或增加压强;
(3)CH4与CO2其起始的物质的量浓度均为1.0 mol•L-1,且随着反应的进行,甲烷的浓度会越来越小,正反应速率也会越来越小,所以曲线v正-c(CH4)相对应的是如图3中曲线是乙线;根据图可知,反应平衡时图中对应的点应为A和F点,降温后,反应速率减小,平衡逆向移动,甲烷的浓度会增大,所以此时曲线甲对应的平衡点可能为应为D点;降温后,反应速率减小,平衡逆向移动,CO浓度减小,曲线乙对应的平衡点可能为C点,
故答案为:乙;D;C.
②H2O(1)═H2O(g)△H=+44.0kJ/mol
C(s)的燃烧热△H=-394.0kJ•mol-1,故热化学方程式为③C(s)+O2(g)=CO2(g)△H=-394.0kJ/mol
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:H2(g)+
| 1 |
| 2 |
(2)①反应Ⅰ达到平衡状态后,随温度升高二氧化碳平衡转化率减小,说明正反应为放热反应,故<0;原因是反应Ⅰ达到平衡状态后,随温度升高二氧化碳平衡转化率减小,说明正反应为放热反应,
故答案为:<;反应Ⅰ达到平衡状态后,随温度升高二氧化碳平衡转化率减小,说明正反应为放热反应;
②温度过高或过低均不利于反应I的进行,原因是:温度过低,化学反应速率慢,温度过高反应Ⅰ向逆反应方向进行且CH4的选择性减小,
故答案为:温度过低,化学反应速率慢,温度过高反应Ⅰ向逆反应方向进行且CH4的选择性减小;
③CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
开始(n) 1 4 0 0
变化 0.8 3.2 0.8 1.6
平衡 0.2 0.8 0.8 1.6,则p(CO2)=
| 0.2 |
| 0.2+0.8+0.8+1.6 |
| 1 |
| 170 |
| 0.8 |
| 0.2+0.8+0.8+1.6 |
| 4 |
| 170 |
| 0.8 |
| 0.2+0.8+0.8+1.6 |
| 4 |
| 170 |
| 1.6 |
| 0.2+0.8+0.8+1.6 |
| 8 |
| 170 |
| p(CH4)p2(H2O) |
| p(CO2)p4(H2) |
| ||||
|
故答案为:2.89×104(MPa)-2;
④由图象得,为减少CO在产物中的比率,可采取的措施有降低温度或增加压强,
故答案为:降低温度或增加压强;
(3)CH4与CO2其起始的物质的量浓度均为1.0 mol•L-1,且随着反应的进行,甲烷的浓度会越来越小,正反应速率也会越来越小,所以曲线v正-c(CH4)相对应的是如图3中曲线是乙线;根据图可知,反应平衡时图中对应的点应为A和F点,降温后,反应速率减小,平衡逆向移动,甲烷的浓度会增大,所以此时曲线甲对应的平衡点可能为应为D点;降温后,反应速率减小,平衡逆向移动,CO浓度减小,曲线乙对应的平衡点可能为C点,
故答案为:乙;D;C.
看了“低碳经济”备受关注,CO2的...的网友还看了以下:
一道物理题,关于功和滑轮组的,快,最好解释一下,10分钟内做出再加5分.一滑轮组,两动滑轮,两定滑 2020-04-25 …
在光电效应实验中,某金属的截止频率相应的波长为λ0,该金属的逸出功为hcλ0hcλ0.若用波长为λ 2020-05-13 …
matlab 条件判断语句不生效想用cos(w*t+y)的值的正负来决定函数的表达式,可是发现条件 2020-05-16 …
世上最难——初一一元一次方程!为有效利用电力资源,某市电力局采取“峰谷”用电政策,每天8:00至2 2020-06-04 …
我国科学家正在研制航母舰载机使用的电磁弹射器,舰载机总质量为3.0×104kg,设起飞过程中发动机 2020-07-17 …
测量滑轮组机械效率的装置如图所示.用5N拉力F将重为8N的物体匀速提升0.5m,用时4s,拉力做得总 2020-11-10 …
某市为更有效利用电力资源,制定了用电标准.如果一户三口之家每月用电量不超过a度,按每度0.50元收费 2020-11-30 …
今年1月,国务院发布了《关于实行最严格水资源管理制度的意见》,其中用水效率控制上规定,到2030年万 2020-12-06 …
在光电效应现象中,若某金属的截止波长为λ0,已知真空中的光速和普朗克常量分别为c和h,该金属的逸出功 2020-12-15 …
下列说法中,正确的是()A.用科学记数法表示的数3.05×104,其原数一定是30500B.将数90 2021-02-02 …