早教吧作业答案频道 -->化学-->
二氧化碳是一种宝贵的碳氧资源.以CO2和NH3为原料合成尿素是固定和利用CO2的成功范例.在尿素合成塔中的主要反应(均自发进行)可表示如下:反应Ⅰ:2NH3(g)+CO2(g)═NH2CO2NH4(s);
题目详情
二氧化碳是一种宝贵的碳氧资源.以CO2和NH3为原料合成尿素是固定和利用CO2的成功范例.在尿素合成塔中的主要反应(均自发进行)可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)═NH2CO2NH4(s);△H1
反应Ⅱ:NH2CO2NH4(s)═CO(NH2)2(s)+H2O(l);△H2
反应Ⅲ:2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(g);△H3
已知:H2O(g)═H2O(l);△H4
请回答下列问题:
(1)反应Ⅰ的△H1=___(用其他△H表示).
(2)反应Ⅱ的△S___0 (填“>”、“=”或“<”).
(3)某研究小组为探究反应Ⅲ影响CO2转化率的因素,在其它条件一定时,图1为CO2转化率受温度变化影响的曲线,图2是按不同氨碳比[n(NH3)/n(CO2)]投料时CO2平衡转化率的变化曲线.
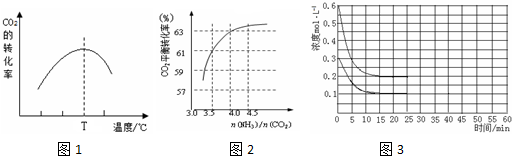
①当温度高于T℃后,CO2转化率变化趋势如图1所示,其原因是___.
②生产中氨碳比宜控制在4.0左右,而不是4.5的原因可能是___.
(4)在某恒定温度下,将NH3和CO2物质的量之比按2:1充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计且只发生反应Ⅰ),经15min达到平衡,各物质浓度的变化曲线如图2所示.
①在上述条件下,从反应开始至15min时,NH3的平均反应速率为___.则反应Ⅰ的平衡常数的值为___.
②若保持平衡的温度和体积不变,25min时再向该容器中充入2mol NH3和1mol CO2,在40min时重新达到平衡,请在图3中画出25~50min内CO2的浓度变化趋势曲线.
反应Ⅰ:2NH3(g)+CO2(g)═NH2CO2NH4(s);△H1
反应Ⅱ:NH2CO2NH4(s)═CO(NH2)2(s)+H2O(l);△H2
反应Ⅲ:2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(g);△H3
已知:H2O(g)═H2O(l);△H4
请回答下列问题:
(1)反应Ⅰ的△H1=___(用其他△H表示).
(2)反应Ⅱ的△S___0 (填“>”、“=”或“<”).
(3)某研究小组为探究反应Ⅲ影响CO2转化率的因素,在其它条件一定时,图1为CO2转化率受温度变化影响的曲线,图2是按不同氨碳比[n(NH3)/n(CO2)]投料时CO2平衡转化率的变化曲线.

①当温度高于T℃后,CO2转化率变化趋势如图1所示,其原因是___.
②生产中氨碳比宜控制在4.0左右,而不是4.5的原因可能是___.
(4)在某恒定温度下,将NH3和CO2物质的量之比按2:1充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计且只发生反应Ⅰ),经15min达到平衡,各物质浓度的变化曲线如图2所示.
①在上述条件下,从反应开始至15min时,NH3的平均反应速率为___.则反应Ⅰ的平衡常数的值为___.
②若保持平衡的温度和体积不变,25min时再向该容器中充入2mol NH3和1mol CO2,在40min时重新达到平衡,请在图3中画出25~50min内CO2的浓度变化趋势曲线.
▼优质解答
答案和解析
(1)①2NH3(g)+CO2(g)⇌NH2CO2NH4(s);△H1
②NH2CO2NH4(s)⇌CO(NH2)2(s)+H2O(l);△H2
③2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g);△H3
④H2O(g)⇌H2O(l);△H4
由盖斯定律可知①=③+④-②,则△H1=△H3+△H4-△H2;
故答案为:△H3+△H4-△H2;
(2)反应Ⅱ:NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g)是气体体积增大的反应,熵变△S>0;
故答案为:>;
(3)①温度高于T℃时,因为反应Ⅲ为自发反应,△S<0,则反应△H3<0,是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低;
故答案为:温度高于T℃时,因为反应Ⅲ为自发反应,△S<0,则反应△H3<0,是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低;
②氨碳比在4.5时,需要氨气较多,但依据图象分析二氧化碳转化率增大不多,工业合成氨生成工艺较复杂,提高生产成本;
故答案为:氨碳比在4.5时,NH3的量增大较多,而CO2的转化率增加不大,提高了生产成本;
(4)①由图可知,15min时达平衡,NH3的浓度变化量为0.6mol/L-0.2mol/L=0.4mol/L,故v(NH3)=
=
=0.027mol•L-1•min-1,
反应2NH3(g)+CO2(g)⇌NH2CO2NH4(s),由图象可知NH3和CO2的起始浓度分别为0.6mol/L、0.3mol/L,平衡时NH3和CO2的浓度分别为0.2mol/L、0.1mol/L,固体浓度视为不变,K=
=
=250;
故答案为:0.027mol•L-1•min-1;250;
②25min时再向容器中充入2mol氨气和1mol二氧化碳,在40min时重新达到平衡,则建立的是等效平衡,二氧化碳的平衡浓度保持不变,曲线如下: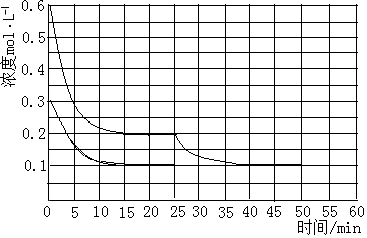 ;
;
故答案为: .
.
②NH2CO2NH4(s)⇌CO(NH2)2(s)+H2O(l);△H2
③2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g);△H3
④H2O(g)⇌H2O(l);△H4
由盖斯定律可知①=③+④-②,则△H1=△H3+△H4-△H2;
故答案为:△H3+△H4-△H2;
(2)反应Ⅱ:NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g)是气体体积增大的反应,熵变△S>0;
故答案为:>;
(3)①温度高于T℃时,因为反应Ⅲ为自发反应,△S<0,则反应△H3<0,是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低;
故答案为:温度高于T℃时,因为反应Ⅲ为自发反应,△S<0,则反应△H3<0,是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低;
②氨碳比在4.5时,需要氨气较多,但依据图象分析二氧化碳转化率增大不多,工业合成氨生成工艺较复杂,提高生产成本;
故答案为:氨碳比在4.5时,NH3的量增大较多,而CO2的转化率增加不大,提高了生产成本;
(4)①由图可知,15min时达平衡,NH3的浓度变化量为0.6mol/L-0.2mol/L=0.4mol/L,故v(NH3)=
| △c |
| △t |
| 0.4mol/L |
| 15min |
反应2NH3(g)+CO2(g)⇌NH2CO2NH4(s),由图象可知NH3和CO2的起始浓度分别为0.6mol/L、0.3mol/L,平衡时NH3和CO2的浓度分别为0.2mol/L、0.1mol/L,固体浓度视为不变,K=
| 1 |
| c 2(NH 3)•c(CO 2) |
| 1 |
| 0.2 2×0.1 |
故答案为:0.027mol•L-1•min-1;250;
②25min时再向容器中充入2mol氨气和1mol二氧化碳,在40min时重新达到平衡,则建立的是等效平衡,二氧化碳的平衡浓度保持不变,曲线如下:
 ;
;故答案为:
 .
.
看了二氧化碳是一种宝贵的碳氧资源....的网友还看了以下:
英语翻译戴进字文进,钱塘人也.为人物花鸟,肖状精奇,直倍常工.进亦自得,以为人且宝贵传之.一日于市, 2020-03-30 …
某增值税一般纳税人销售从农业生产者处购进的自产谷物,其缴纳增值税时适用零税率。( ) 2020-05-17 …
汉译英;最初的自行车是木制的,只有2个木轮子.1,最初的自行车是木制的,只有2个木轮子.2,改进的 2020-06-07 …
易语言动画框自动前进和自动旋转问题!如何在易语言的动画框中完成以下动作:动画物体1从56,136的 2020-07-12 …
某体育用品商场分别用10000元购进A种品牌,用7500元购进B种品牌的自行车进行销售,已知B种品 2020-07-16 …
下列关于惯性的说法正确的是()A.急速前进的自行车紧急刹车,车上的人向前倾,是由于受自行车向前冲力的 2020-11-02 …
以下能正确描述三者之间关系的是哪一个()A.自然选择→生物多样性→生物进化B.自然选择→生物进化→生 2020-11-04 …
关于自力更生与发展对外经济的关系,正确的认识有①自力更生是发展对外经济关系的前提和基础②发展对外经济 2020-11-22 …
自行车队出发20分钟后,通信员骑摩托车去追他们,在距出发地点12千米的地方追上了自行车队,然后通信员 2020-12-05 …
喷泉是一种常见的自然现象,其产生的原因是存在压强差.制取氨气并完成喷泉实验(图中夹持装置均已略去). 2020-12-19 …