早教吧作业答案频道 -->化学-->
自从1985年发现了富勒烯以来,由于其具有独特的物理和化学性质,越来越受到人们的关注.(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图.①Fe3+基态时M能层电子排布式为
题目详情
自从1985年发现了富勒烯以来,由于其具有独特的物理和化学性质,越来越受到人们的关注.
(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图.
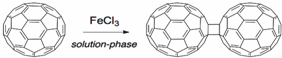
①Fe3+基态时M能层电子排布式为___.
②富勒烯二聚体中碳原子杂化轨道类型有___.
(2)下列有关说法正确的是___.
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、NH3都是非极性分子
C.每个N2中,含有2个π键
(3)CO的一种等电子体为NO+,NO+的电子式为___
(4)ClO2-的立体构型是___,该离子中两种元素的电负性由小到大的顺序为___.
(5)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是___.
(6)关于化合物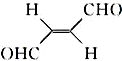 ,下列叙述正确的有___.
,下列叙述正确的有___.
A.该分子在水中的溶解度大于2-丁烯
B.分子中只有极性键
C.分子中有7个σ键和1个π键
D.该化合物既能发生还原反应又能发生氧化反应
E.分子间可形成氢键.
(1)富勒烯(C60)在液相中用FeCl3催化可生成二聚体,过程见图.

①Fe3+基态时M能层电子排布式为___.
②富勒烯二聚体中碳原子杂化轨道类型有___.
(2)下列有关说法正确的是___.
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、NH3都是非极性分子
C.每个N2中,含有2个π键
(3)CO的一种等电子体为NO+,NO+的电子式为___
(4)ClO2-的立体构型是___,该离子中两种元素的电负性由小到大的顺序为___.
(5)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是___.
(6)关于化合物
 ,下列叙述正确的有___.
,下列叙述正确的有___.A.该分子在水中的溶解度大于2-丁烯
B.分子中只有极性键
C.分子中有7个σ键和1个π键
D.该化合物既能发生还原反应又能发生氧化反应
E.分子间可形成氢键.
▼优质解答
答案和解析
(1)①铁是26号元素,铁原子核外有26个电子,铁原子失去3个电子变成铁离子,根据构造原理可知铁离子核外电子排布式为1s22s22p63s23p63d5 或[Ar]3d5;
故答案为:3s23p63d5;
②从富勒烯二聚体中可以看出大多数碳原子每个C原子和其它三个C原子成键,为三个δ键和一个π键,故杂化类型为sp2杂化,有4个碳原子每个C原子和其它四个C原子成键,为四个δ键,故杂化类型为sp3杂化;
故答案为:sp2、sp3;
(2)A.C3H8分子中每个C原子含有4个σ键,所以每个C原子价层电子对个数是4,则C原子采用sp3杂化,故A正确;
B.O2是以非极性键结合的双原子一定为非极性分子,CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子,NH3的立体构型为三角锥型,结构不对称,分子中正负电荷重心不重叠,为极性分子,故B错误;
C.1个氮氮三键中含有2个π键,故C正确;
故答案为:AC;
(3)CO的一种等电子体为NO+,CO的结构为C≡O,则NO+的电子式为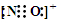 ,
,
故答案为: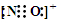 ;
;
(4)ClO2-中价层电子对个数=2+
(7+1-2×2)=2,且含有2个孤电子对,所以是V型;元素的非金属性越强,其电负性越强,则电负性:Cl<O;
故答案为:Cl<O;
(5)Zr原子序数为40,价电子排布式为4d25s2,含有5个电子层,在第五周期,价电子数为4,为第IVB族;
故答案为:第5周期第ⅣB族;
(6)A.2-丁烯不溶于水,而该物质属于烯醛类物质,可溶于水,则该分子在水中的溶解度大于2-丁烯,故A正确;
B.C、H与C、O之间形成极性键,而C、C之间形成非极性键,则分子中既有极性键又有非极性键,故B错误;
C.双键中含1个σ键和1个π键,单键均为σ键,则分子中有9个σ键和3个π键,故C错误;
D.-CHO能被氧化成羧基、被还原成羟基,碳碳双键,既能被酸性高锰酸钾等氧化剂氧化,又能加氢被还原,故D正确;
E.含-CHO,没有O-H键,则不能形成氢键,故E错误;
故答案为:AD.
故答案为:3s23p63d5;
②从富勒烯二聚体中可以看出大多数碳原子每个C原子和其它三个C原子成键,为三个δ键和一个π键,故杂化类型为sp2杂化,有4个碳原子每个C原子和其它四个C原子成键,为四个δ键,故杂化类型为sp3杂化;
故答案为:sp2、sp3;
(2)A.C3H8分子中每个C原子含有4个σ键,所以每个C原子价层电子对个数是4,则C原子采用sp3杂化,故A正确;
B.O2是以非极性键结合的双原子一定为非极性分子,CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子,NH3的立体构型为三角锥型,结构不对称,分子中正负电荷重心不重叠,为极性分子,故B错误;
C.1个氮氮三键中含有2个π键,故C正确;
故答案为:AC;
(3)CO的一种等电子体为NO+,CO的结构为C≡O,则NO+的电子式为
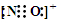 ,
,故答案为:
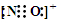 ;
;(4)ClO2-中价层电子对个数=2+
| 1 |
| 2 |
故答案为:Cl<O;
(5)Zr原子序数为40,价电子排布式为4d25s2,含有5个电子层,在第五周期,价电子数为4,为第IVB族;
故答案为:第5周期第ⅣB族;
(6)A.2-丁烯不溶于水,而该物质属于烯醛类物质,可溶于水,则该分子在水中的溶解度大于2-丁烯,故A正确;
B.C、H与C、O之间形成极性键,而C、C之间形成非极性键,则分子中既有极性键又有非极性键,故B错误;
C.双键中含1个σ键和1个π键,单键均为σ键,则分子中有9个σ键和3个π键,故C错误;
D.-CHO能被氧化成羧基、被还原成羟基,碳碳双键,既能被酸性高锰酸钾等氧化剂氧化,又能加氢被还原,故D正确;
E.含-CHO,没有O-H键,则不能形成氢键,故E错误;
故答案为:AD.
看了自从1985年发现了富勒烯以来...的网友还看了以下:
如图,某储藏室入口的截面是一个半径为1.2m的 半圆形,一个长,宽,高分别是1.2m,1m,0.8 2020-04-05 …
在下列数据后填上合适的单位和单位换算:(1)小民的身高为17.2.(2)教室的长度850.(3)8 2020-05-12 …
2^2m×8^m(m>0)=2×2×.×2(2m个2相乘)×8×8×.×8(m个8相乘)=2×8× 2020-05-21 …
小明用电学方法测量电线的长度.首先,小明测得电线铜芯的直径为1.00mm,估计其长度不超过50m( 2020-06-12 …
已知全集U={1,2,3,4,5,6,7,8},M={3,4,5},P={1,3,6},则{2,7 2020-07-13 …
把8米长的钢管平均分成5段,每段是全长的,每段长米,每段是8米的. 2020-07-15 …
已知集合M={x|sinx>cosx,0<x<π}和N={x|sin2x>cos2x,0<x<π} 2020-07-30 …
已知α,β表示两个不同的平面,m为平面α内的一条直线,则“α⊥β”是“m⊥β”的.①充分不必要条件 2020-07-30 …
已知α,β表示两个不同的平面,m为平面α内的一条直线,则“α⊥β”是“m⊥β”的.①充分不必要条件 2020-08-02 …
GreenTreesGym(体育馆)SwimmingMon.~Sun.8:00a.m.~8:00p. 2020-10-30 …