早教吧作业答案频道 -->化学-->
某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验过程如下:i.打开弹簧夹,缓慢通入N2,并保持后续反应均在N2氛围中进
题目详情
某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验过程如下:
i.打开弹簧夹,缓慢通入N2,并保持后续反应均在N2氛围中进行;
ii.加入pH 已调至2.5 的 0.01mol•L-1KNO3酸性溶液100mL,一段时间后铁粉部分溶解,
溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物
质附着;
iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在NO3-、NH4+和Fe2+.
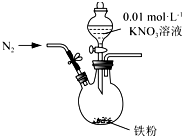
(1)通入N2并保持后续反应均在N2 氛围中进行的实验目的是___.
(2)白色物质是___,用化学方程式解释其变为红褐色的原因:___.
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是___.
(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色.溶液变成红色的原因是___.
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳.他用上述KNO3溶液继续设计如下实验,探究碳粉的作用
③关于碳粉的作用,还可以提出的假设是___.
i.打开弹簧夹,缓慢通入N2,并保持后续反应均在N2氛围中进行;
ii.加入pH 已调至2.5 的 0.01mol•L-1KNO3酸性溶液100mL,一段时间后铁粉部分溶解,
溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物
质附着;
iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在NO3-、NH4+和Fe2+.

(1)通入N2并保持后续反应均在N2 氛围中进行的实验目的是___.
(2)白色物质是___,用化学方程式解释其变为红褐色的原因:___.
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是___.
(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色.溶液变成红色的原因是___.
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳.他用上述KNO3溶液继续设计如下实验,探究碳粉的作用
| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原剂,脱除硝酸盐 | 向烧杯中加入 ___一段时间后,测定烧杯中NO3-的浓度 | NO3-浓度无明显变化,说明假设不成立 |
| 假设2:碳粉、铁粉形成无数个微小的原电池,促进了硝酸盐的脱除 | 按下图所示组装实验装置,一段时间后,测定NO3-浓度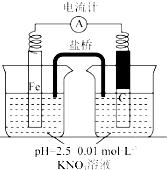 | ___,说明假设2成立 |
▼优质解答
答案和解析
(1)用氮气排尽装置中空气,避免空气中氧气对Fe与NO3-离子反应的干扰,
故答案为:避免空气中氧气对Fe与NO3-离子反应的干扰;
(2)铁粉部分溶解,溶液逐渐变为浅绿色,说明有Fe2+生成,待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物,酸性减弱Fe2+水解得到Fe(OH)2,白色物质为氢氧化亚铁,被氧化为氢氧化铁,颜色变为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是:取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,证明滤液中存Fe2+,
故答案为:取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,证明滤液中存Fe2+;
(4)溶液中存在Fe2+、NO3-离子,加入硫酸,发生反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,生成的Fe3+和SCN-反应使溶液呈红色,
故答案为:溶液中存在Fe2+、NO3-离子,加入硫酸,发生反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,生成的Fe3+和SCN-反应使溶液呈红色;
(5)假设1:探究的是碳粉直接与NO3-反应效果,加入碳粉即可,作对照试验,溶液选取与原题中相同;
假设2:构成原电池,负极电极反应式:Fe-2e-=Fe2+,正极NO3-被还原,Fe电极部分溶解,电流计指针偏转等,说明假设2成立,
③碳粉作为催化剂,提高脱除硝酸盐反应速率,
故答案为:碳粉;Fe电极部分溶解,电流计指针偏转;碳粉作为催化剂,提高脱除硝酸盐反应速率.
故答案为:避免空气中氧气对Fe与NO3-离子反应的干扰;
(2)铁粉部分溶解,溶液逐渐变为浅绿色,说明有Fe2+生成,待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物,酸性减弱Fe2+水解得到Fe(OH)2,白色物质为氢氧化亚铁,被氧化为氢氧化铁,颜色变为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是:取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,证明滤液中存Fe2+,
故答案为:取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,证明滤液中存Fe2+;
(4)溶液中存在Fe2+、NO3-离子,加入硫酸,发生反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,生成的Fe3+和SCN-反应使溶液呈红色,
故答案为:溶液中存在Fe2+、NO3-离子,加入硫酸,发生反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,生成的Fe3+和SCN-反应使溶液呈红色;
(5)假设1:探究的是碳粉直接与NO3-反应效果,加入碳粉即可,作对照试验,溶液选取与原题中相同;
假设2:构成原电池,负极电极反应式:Fe-2e-=Fe2+,正极NO3-被还原,Fe电极部分溶解,电流计指针偏转等,说明假设2成立,
③碳粉作为催化剂,提高脱除硝酸盐反应速率,
故答案为:碳粉;Fe电极部分溶解,电流计指针偏转;碳粉作为催化剂,提高脱除硝酸盐反应速率.
看了某同学看到“利用零价铁还原NO...的网友还看了以下:
FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:I.实验需 2020-07-01 …
小邦同学利用U型管压强计和装有水的大烧杯探究液体内部压强的特点.(1)为了顺利完成实验,除了图甲中 2020-07-02 …
晓轩同学在“探究冰和蜡的熔化规律”时,使用的实验装置如图甲所示.(1)本实验所用的温度计是根据液体 2020-07-06 …
下列化学反应不能达到实验目的是()A.用Al(OH)3治疗胃酸过多症B.用稀盐酸除去炭粉中的CuO 2020-07-12 …
(1)我在练习册看到一段话:在进行物质检验时,注意排除杂质的干扰,如含氯离子的溶液中若含有硫酸根离子 2020-11-10 …
(17分)FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:I 2020-12-04 …
FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:I.实验需要 2020-12-04 …
检验CO2用NaOH溶液还是石灰水?原因吸收CO2用NaOH溶液还是石灰水?鉴别石灰水和NaOH溶液 2021-02-01 …
下列实验能达到目的是()A.用饱和Na2CO3溶液除去混在CO2中的HCl气体B.用Cl2除去Fe2 2021-02-09 …
下列实验能达到预期目的是()①用溴水验证汽油中含有不饱和烃②用NaOH溶液除去苯中混有的少量苯酚③用 2021-02-16 …