(8分)提出查理定律的查理很幸运,碰巧开始时没有以N2O4来研究气体行为,否则他或许会得出一种相当特殊的温度效应。对于平衡N2O4(g)2NO2(g),在298K时,其Kp=0.1pθ
(8分)提出查理定律的查理很幸运,碰巧开始时没有以N 2 O 4 来研究气体行为,否则他或许会得出一种相当特殊的温度效应。
对于平衡N 2 O 4 (g)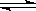 2NO 2 (g),在298K时,其K p =0.1pθ,而K p =4α 2 p/(1-α 2 ),α为N 2 O 4 的解离度,p为平衡体系的总压。假设,298 K时,查理把0.015 mol的N 2 O 4 放于一只2.44×10 -3m3 的烧杯中,当解离达到平衡后,他将看到平衡压力等于0.205pθ。其对应的α=0.33。
2NO 2 (g),在298K时,其K p =0.1pθ,而K p =4α 2 p/(1-α 2 ),α为N 2 O 4 的解离度,p为平衡体系的总压。假设,298 K时,查理把0.015 mol的N 2 O 4 放于一只2.44×10 -3m3 的烧杯中,当解离达到平衡后,他将看到平衡压力等于0.205pθ。其对应的α=0.33。
1.在保持体积不变的前提下,查理做把温度升高10%的实验,即把温度升高至328K。根据理想气体定律,其压力也应只增大10%,即等于0.226 pθ,但查理发现这时的压力为0.240 pθ。自然,问题是出在N 2 O 4 的解离度增加上了。试求此时的α和K p 。
2.若NO 2 在298K下的标准摩尔生成自由能为51.463kJ/mol,试计算N 2 O 4 在298K下标准摩尔生成自由能。
团长:做湿度场模拟时,可以查看质量分数的情况,如何转换成相对湿度.质量分数与相对湿度之间转换公式有 2020-04-08 …
以下是我在自学物理时遇到的两个问题:(一)惯性离心力是什么?离心力大小如何计算?(二)一个小球P绕 2020-05-16 …
实验测得某有机物元素质量组成为C:69%,H:4.6%,N:8%,其余为O,相对分子质量是300 2020-05-16 …
求独立坐标系原点在大地坐标系中的坐标大坝有一点O,相对坐标为纵0+000.00,坝0+000.00 2020-06-21 …
一个铅质的圆柱体,测得其直径为d=(2.040+—0.001)cm,高度h=(4.120+—0.0 2020-06-30 …
P的相对原子质量分数 2020-07-20 …
如图表示生长素浓度与植物生长的关系.下列部位的生长素浓度与生长关系,与P点相对应的是()A.胚芽鞘 2020-07-26 …
如图,长方形ABCO对角线BO与AC的交点P到相对两边距离相等.若C点(2,0),P(1,2),请 2020-08-01 …
一半径为3m的水轮如图所示,水轮圆心O距离水面2m,已知水轮每分钟转动4圈,如果当水轮上P点从水中浮 2020-11-26 …
一半径为4m的水轮,如图所示水轮圆心O距离水面2m,己知水轮每分钟转动4圈,如果当水轮上P点从水中浮 2021-01-12 …