25℃时,H2CO3的Kal=4.2×10-7,Ka2=5.6×10-11.室温下向10mL0.1mo1•L-1Na2CO3溶液中逐滴加入0.1mo1•L-1HCl溶液.如图是溶液中含碳元素微粒物质的量分数随pH降低而变化的图象(CO2因有逸出未画出).
25℃时,H2CO3的Kal=4.2×10-7,Ka2=5.6×10-11.室温下向10mL 0.1mo1•L-1Na2CO3溶液中逐滴加入0.1mo1•L-1HCl溶液.如图是溶液中含碳元素微粒物质的量分数随pH降低而变化的图象(CO2因有逸出未画出).下列说法错误的是( )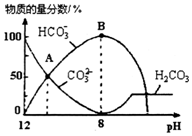
A. A点所示溶液的pH<11
B. B点所示溶液:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. A点→B点发生反应的离子方程式为CO32-+H+═HCO3-
D. 分步加入酚酞和甲基橙,用滴定法可测定Na2CO3与NaHCO3混合物的组成
| c(CO32-)×c(H+) |
| c(HCO3-) |
B.室温下向10mL 0.1mo1•L-1Na2CO3溶液中逐滴加入0.1mo1•L-1HCl溶液,B点溶液中钠离子的物质的量浓度是含碳离子的浓度的2倍,即c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3),故B错误;
C.A点→B:CO32-逐渐减少,HCO3-逐渐增加,所以发生反应的离子方程式为CO32-+H+═HCO3-,故C正确;
D.1Na2CO3溶液中逐滴加入HCl,用酚酞作指示剂,滴定产物是NaHCO3,用甲基橙作指示剂滴定时NaHCO3与HCl反应产物是H2CO3,所以分步加入酚酞和甲基橙,用滴定法可测定Na2CO3与NaHCO3混合物的组成,故D正确.
故选B.
GA=50N,F=150N.M=0.2N(就是动摩擦因数)1)若将A从下面拉出需多大的力?2)若将 2020-04-09 …
两份体积相同的某植物营养液,其配方分别如下:KClK2SO4ZnSO4①0.3mol•L-10.2 2020-05-13 …
质量分数为a%,物质的量浓度为cmol·L-1的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变 2020-05-14 …
法律上的处分是指依照所有人的意志,通过某种法律行为对物进行处置,它意味着( )A.物的消耗B.所有 2020-05-27 …
已知抛物线C:y1=a(x-h)2-1,直线l:y2=kx-kh-1.(1)求证:直线l恒过抛物线 2020-06-27 …
L-多巴是一种药物,它可用于帕金森综合症的治疗.对该药物的研究,使科学家们分别获得诺贝尔医学奖和诺贝 2020-10-31 …
(1/2)设抛物线C:x^2=2py的焦点为F,准线为l,A为C上一点,已知F为圆心,FA为半径的圆 2020-11-27 …
用L,l,m表示k某种弹簧秤原来的长度为l,悬挂重物后的长度L可用公式L=l+k分之m表示某种弹簧秤 2020-12-05 …
在恒温、恒容的密闭容器中反应.若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓 2020-12-22 …
如图所示,A、B两个同样的物体,A与B用弹簧连接,当悬挂A物的细线突然剪断,在剪断的瞬间,A、B的加 2021-01-23 …