早教吧作业答案频道 -->化学-->
若往20mL0.01mol/L的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是(填标号)①该烧碱溶液的浓度为0.02mol/L②该烧碱溶液的浓度为0
题目详情
若往20mL0.01mol/L的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是___(填标号)
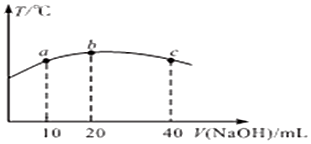
①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)

①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
▼优质解答
答案和解析
①HNO2是弱酸,次氯酸电离是吸热反应,酸碱中和反应是放热反应,当恰好完全中和时放出热量最多,c(NaOH)=
=0.01mol/L;
故①错误,②正确;
③电离吸热,温度越高电离平衡常数越大,所以HNO2的电离平衡常数:b点>a点,故③正确;
④从b点到c点,当C(NaOH)较大时,可能出现:c(Na+)>c(OH-)>c(NO2-)>c(H+),故④错误;
故答案为:②③.
| 0.020L×0.01mol/L |
| 0.020L |
故①错误,②正确;
③电离吸热,温度越高电离平衡常数越大,所以HNO2的电离平衡常数:b点>a点,故③正确;
④从b点到c点,当C(NaOH)较大时,可能出现:c(Na+)>c(OH-)>c(NO2-)>c(H+),故④错误;
故答案为:②③.
看了若往20mL0.01mol/L...的网友还看了以下:
Ⅰ、A物质的化学式为M(OH)2,将其溶于水制成稀溶液,该溶液呈中性,在溶液中存在:M2++2OH 2020-04-12 …
常温下,某溶液M中存在的离子有:Na+、A2-、HA-、H+、OH一,存在的分子有H2A、H2O. 2020-05-23 …
关于x的方程(m的平方-4)x平方+(m+2)x+(m+1)y=m+5关于x的方程(m的平方—4) 2020-06-12 …
MOH强碱溶液和等体积、等浓度的HA弱酸溶液混合后,溶液中有关离子的浓度应满足的关系是()A.c( 2020-07-16 …
用一个玻璃瓶装满水后称得总质量是500g.用它盛某种液体,测得液体体积V和液体与玻璃瓶总质量m的关 2020-07-22 …
常温下,某水溶液M中存在的离子有:Na+、A-、H+、OH-.若该溶液M由pH=3的HA溶液V1m 2020-07-25 …
用量筒盛某种液体,测得“液体体积V”和“液体与量筒的总质量m”的关系如图所示,请观察图象,并根据图 2020-07-25 …
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后 2020-11-04 …
小明利用天平和量杯测量某种液体的密度,得到“液体体积V”和“液体与量筒的总质量m”的关系如图所示,求 2021-02-20 …
小明利用天平和量杯测量某种液体的密度,得到“液体体积V”和“液体与量筒的总质量m”的关系如图所示,求 2021-02-20 …