早教吧作业答案频道 -->化学-->
现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.请回答:(1)写出反应中发生的化学方程式;(2)
题目详情
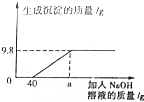
现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.
请回答:
(1)写出反应中发生的化学方程式___;
(2)列出求解溶液中含有的氯化氢的质量(x)的比例式___;
(3)混合溶液中CuCl2的质量分数为___;
(4)求恰好完全反应时,消耗NaOH溶液的总质量为___;
(5)若恰好完全反应时过滤,并向滤液中加入15.3g水,则所得溶液的溶质质量分数为___;
(6)若题中所用的NaOH溶液是用25%的NaOH溶液稀释而成,则需加水的质量为___.
请回答:

(1)写出反应中发生的化学方程式___;
(2)列出求解溶液中含有的氯化氢的质量(x)的比例式___;
(3)混合溶液中CuCl2的质量分数为___;
(4)求恰好完全反应时,消耗NaOH溶液的总质量为___;
(5)若恰好完全反应时过滤,并向滤液中加入15.3g水,则所得溶液的溶质质量分数为___;
(6)若题中所用的NaOH溶液是用25%的NaOH溶液稀释而成,则需加水的质量为___.
▼优质解答
答案和解析
(1)氢氧化钠和盐酸反应生成氯化钠和水,氢氧化钠和氯化铜反应生成氢氧化铜沉淀和氯化钠,化学方程式为:HCl+NaOH=NaCl+H2O、CuCl2+2NaOH═Cu(OH)2↓+2NaCl;
(2)设与氢氧化钠反应的氯化氢的质量为x,生成氯化钠质量为y,
HCl+NaOH=NaCl+H2O
36.5 40 58.5
x 40g×10% y
=
=
x=3.65g
y=5.85g
(3)设参加反应的氯化铜的质量为z,参加反应的氢氧化钠质量为m,生成氯化钠的质量为n,
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
135 80 98 117
z m 9.8g n
=
=
=
z=13.5g
m=8g
n=11.7g
所以混合溶液中CuCl2的质量分数为:
×100%=27%;
(4)恰好完全反应时,消耗NaOH溶液的总质量为:40g+
=120g;
(5)恰好完全反应时过滤,并向滤液中加入15.3g水,则所得溶液的溶质质量分数为:
×100%=10%;
(6)需要氢氧化钠溶质的质量为:120g×10%=12g,
需加水的质量为:120g-
=72g.
故答案为:(1)HCl+NaOH=NaCl+H2O、CuCl2+2NaOH═Cu(OH)2↓+2NaCl;
(2)
=
(3)27%;
(4)120g;
(5)10%;
(6)72g.
(2)设与氢氧化钠反应的氯化氢的质量为x,生成氯化钠质量为y,
HCl+NaOH=NaCl+H2O
36.5 40 58.5
x 40g×10% y
| 36.5 |
| x |
| 40 |
| 40g×10% |
| 58.5 |
| y |
x=3.65g
y=5.85g
(3)设参加反应的氯化铜的质量为z,参加反应的氢氧化钠质量为m,生成氯化钠的质量为n,
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
135 80 98 117
z m 9.8g n
| 135 |
| z |
| 80 |
| m |
| 98 |
| 9.8g |
| 117 |
| n |
z=13.5g
m=8g
n=11.7g
所以混合溶液中CuCl2的质量分数为:
| 13.5g |
| 50g |
(4)恰好完全反应时,消耗NaOH溶液的总质量为:40g+
| 8g |
| 10% |
(5)恰好完全反应时过滤,并向滤液中加入15.3g水,则所得溶液的溶质质量分数为:
| 5.85g+11.7g |
| 120g+50g+15.3g-9.8g |
(6)需要氢氧化钠溶质的质量为:120g×10%=12g,
需加水的质量为:120g-
| 12g |
| 25% |
故答案为:(1)HCl+NaOH=NaCl+H2O、CuCl2+2NaOH═Cu(OH)2↓+2NaCl;
(2)
| 36.5 |
| x |
| 40 |
| 40g×10% |
(3)27%;
(4)120g;
(5)10%;
(6)72g.
看了现有含HCl和CuCl2的混合...的网友还看了以下:
配制一定体积、一定物质的量浓度的溶液,下列操作使配得的溶液浓度偏小的是()A.容量瓶中原有少量蒸馏 2020-04-12 …
一位同学先在试管中加入约2ml的氢氧化钠溶液,有滴入几滴酚酞溶液,溶液变红,然后慢慢滴入稀盐酸,边 2020-05-17 …
在一烧杯中盛有一定质量的金属镁,向其中加入足量的稀硫酸在一定温度下得到30gA溶液.再向所得的A溶 2020-05-23 …
向一含有盐酸的氯化铁溶液边震荡边逐滴滴入氢氧化钠溶液,直至过量,某同学画了如图,要表明反应过程中, 2020-06-15 …
某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液,锥形 2020-07-03 …
烧杯中盛有BaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO 2020-07-20 …
已知:①在淀粉KI溶液中滴入少量NaClO溶液,并加入少量硫酸,溶液立即变蓝;②在上述蓝色溶液中, 2020-07-26 …
在滴有酚酞的氢氧化钠溶液中逐滴滴入盐酸,测定逐滴滴加盐酸后相应溶液的pH,并在坐标图中将这些点用光滑 2020-11-03 …
向一含有盐酸的氯化铁溶液中边振荡边逐滴滴入氢氧化钠溶液,直至过量,某同学画了如图,要表明反应过程中, 2020-11-11 …
(2013•柳州)向一含有盐酸的氯化铁溶液边震荡边逐滴滴入氢氧化钠溶液,直至过量,某同学画了如图,要 2020-11-13 …