早教吧作业答案频道 -->化学-->
废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如下:(1)①写出铜帽溶解过程中发生反应
题目详情
废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如下:
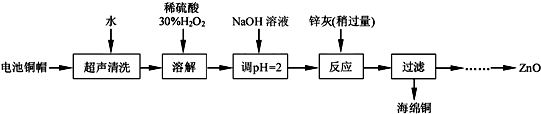
(1)①写出铜帽溶解过程中发生反应的化学方程式___.
②铜帽溶解后需将溶液中过量H2O2除去.除去H2O2的简便方法是___.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2 I2+2
═2I-+
①滴定选用的指示剂为___,滴定终点观察到的现象为___.
②若滴定前溶液中H2O2没有除尽,所测得的Cu2+的含量将会___(填“偏高”、“偏低”、“不变”).
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
由回收铜后的滤液制备ZnO的实验步骤依次为:
①___;
②___;
③过滤;
④___;
⑤过滤、洗涤、干燥
⑥900℃煅烧.

(1)①写出铜帽溶解过程中发生反应的化学方程式___.
②铜帽溶解后需将溶液中过量H2O2除去.除去H2O2的简便方法是___.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2 I2+2
| S | 2 |
| O | 2- 3 |
| S | 4 |
| O | 2- 6 |
①滴定选用的指示剂为___,滴定终点观察到的现象为___.
②若滴定前溶液中H2O2没有除尽,所测得的Cu2+的含量将会___(填“偏高”、“偏低”、“不变”).
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀的pH | 3.2 | 8.8 | 8.9 |
由回收铜后的滤液制备ZnO的实验步骤依次为:
①___;
②___;
③过滤;
④___;
⑤过滤、洗涤、干燥
⑥900℃煅烧.
▼优质解答
答案和解析
利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收 Cu并制备ZnO,电池铜帽加入水过滤后除去溶于水的杂质,在固体中加入过氧化氢溶解,铜生成硫酸铜溶液,加热煮沸将溶液中过量的H2O2除去,加入氢氧化钠溶液调节溶液PH=2沉淀铁离子,加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物),反应过滤得到海绵铜,沉淀锌离子得到氢氧化锌,分解得到氧化锌,
(1)①因为双氧水在酸性溶液中先把铜氧化成氧化铜,当然这是一个微弱的反应,形成一个平衡,但是形成的氧化铜马上就会被稀硫酸溶解,平衡被打破,反应朝正方向进行,故而逐渐溶解,反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;
②过氧化氢性质比较稳定,若加热到153℃便猛烈的分解为水和氧气,将溶液中过量的H2O2 除去可加热至沸,
故答案为:加热至沸;
(2)①淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,
故答案为:淀粉溶液;蓝色褪去并半分钟内不恢复;
②若留有H2O2,加入KI后,会有以下反应:H2O2+2I-+2H+=I2+2H2O,误当成2Cu2++4I-=2CuI(白色)↓+I2 生成的碘,使测定结果偏高,
故答案为:偏高;
(3)根据表中阳离子沉淀的PH可知,由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入30%H2O2,使其充分反应,目的使Fe2+转化完全为Fe3+,②加氢氧化钠溶液,控制PH在4左右,使Fe3+沉淀完全,③过滤,向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全,⑤过滤、洗涤、干燥;
⑥900℃煅烧,制得氧化锌,
故答案为:①向滤液中加入略过量30%的H2O2,使其充分反应;②向反应后的溶液中滴加1.0 moL•L-1的NaOH溶液,调节溶液的pH约为5(或3.2≤pH<5.9);④向滤液中滴加1.0 moL•L-1的氢氧化钠,调节pH约为10(或8.9≤pH≤11).
(1)①因为双氧水在酸性溶液中先把铜氧化成氧化铜,当然这是一个微弱的反应,形成一个平衡,但是形成的氧化铜马上就会被稀硫酸溶解,平衡被打破,反应朝正方向进行,故而逐渐溶解,反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;
②过氧化氢性质比较稳定,若加热到153℃便猛烈的分解为水和氧气,将溶液中过量的H2O2 除去可加热至沸,
故答案为:加热至沸;
(2)①淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,
故答案为:淀粉溶液;蓝色褪去并半分钟内不恢复;
②若留有H2O2,加入KI后,会有以下反应:H2O2+2I-+2H+=I2+2H2O,误当成2Cu2++4I-=2CuI(白色)↓+I2 生成的碘,使测定结果偏高,
故答案为:偏高;
(3)根据表中阳离子沉淀的PH可知,由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入30%H2O2,使其充分反应,目的使Fe2+转化完全为Fe3+,②加氢氧化钠溶液,控制PH在4左右,使Fe3+沉淀完全,③过滤,向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全,⑤过滤、洗涤、干燥;
⑥900℃煅烧,制得氧化锌,
故答案为:①向滤液中加入略过量30%的H2O2,使其充分反应;②向反应后的溶液中滴加1.0 moL•L-1的NaOH溶液,调节溶液的pH约为5(或3.2≤pH<5.9);④向滤液中滴加1.0 moL•L-1的氢氧化钠,调节pH约为10(或8.9≤pH≤11).
看了废弃物的综合利用既有利于节约资...的网友还看了以下:
生活在豆科植物根部的根瘤菌,可以吸收并利用空气中的氮气,制造含氮化合物供植物利用,而植物也可以供给 2020-05-17 …
物理的并联电路怎样画(要点是什么)要典型例题 2020-05-21 …
初三物理的并联电路图,开关的符号必须是那个小圆圈一端是正极吗?如果电路图中一个元件(如灯泡、开关) 2020-05-23 …
地球上植物产生的纤维素中有40%~60%被土壤中的某些微生物利用,从土壤中分离并研究这些微生物有利 2020-06-20 …
某商场投入了一笔资金采购了一批物品紧销商品,经过市场调查发现,如果月初出售,可获利15%,并可用本 2020-06-26 …
2011年5月23日中国医学科学院药物研究所研究人员发现了一种新物质,并向中国专利技术局申请了专利, 2020-11-14 …
下列各种生理活动中,属于动物特有的是A利用水和二氧化碳能合成自身所需要的某些有机物B利用消化分解食物 2020-11-22 …
阅读下列材料:所有权是无限地利用并支配物品的权利,但利用以不受法律的禁止为限。除非供公用并有公正的赔 2020-12-07 …
地球上植物产生的纤维素中有40%~60%被土壤中的某些微生物利用,从土壤中分离并研究这些微生物有利于 2020-12-12 …
关于物理的并联的用电器越多,电路中的总功率越,家庭电路中电压是,根据公式可知干路中电流.并联的用电器 2021-01-05 …