早教吧作业答案频道 -->化学-->
(1)用作橡胶工业的硫化剂S2Cl2的分子结构中每个原子均满足8电子稳定结构,①试写出S2Cl2的电子式.②S2Cl2易发生水解反应,产生无色刺激性气味气体,同时生成淡黄色沉淀,其反应的
题目详情
(1)用作橡胶工业的硫化剂S2Cl2的分子结构中每个原子均满足8电子稳定结构,①试写出S2Cl2的电子式___.
②S2Cl2易发生水解反应,产生无色刺激性气味气体,同时生成淡黄色沉淀,其反应的化学方程式为___.
(2)用作氧化剂的过二硫酸铵[(NH4)2S2O8]属于离子化合物,易溶于水,其可由(NH4)2SO4为原料制备.
①若硫酸铵溶液的浓度为250g/L,其物质的量浓度是___moI/L.
②(NH4)2S2O8在Ag+的催化作用下能将Mn2+氧化成MnO4-,其反应的离子方程式为 ___.
(3)Na2S2O4在空气分析中常用来吸收氧气,当吸收氧气、水蒸气后发生反应时,若还原剂和氧化剂的物质的量之比为1:1,则产物为___(填化学式).
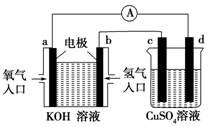
(4)氢气是一种绿色能源,具有广阔的发展前景.现用氢氧燃料电池进行如图所示实验(其中a、b均为碳棒,c、d均为铜电极).
d电极的电极反应式是①___
a电极的电极反应式是②___.
②S2Cl2易发生水解反应,产生无色刺激性气味气体,同时生成淡黄色沉淀,其反应的化学方程式为___.
(2)用作氧化剂的过二硫酸铵[(NH4)2S2O8]属于离子化合物,易溶于水,其可由(NH4)2SO4为原料制备.
①若硫酸铵溶液的浓度为250g/L,其物质的量浓度是___moI/L.
②(NH4)2S2O8在Ag+的催化作用下能将Mn2+氧化成MnO4-,其反应的离子方程式为 ___.
(3)Na2S2O4在空气分析中常用来吸收氧气,当吸收氧气、水蒸气后发生反应时,若还原剂和氧化剂的物质的量之比为1:1,则产物为___(填化学式).
(4)氢气是一种绿色能源,具有广阔的发展前景.现用氢氧燃料电池进行如图所示实验(其中a、b均为碳棒,c、d均为铜电极).
d电极的电极反应式是①___
a电极的电极反应式是②___.

▼优质解答
答案和解析
(1)①S2Cl2分子结构与H2O2相似,S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对,S2Cl2电子式为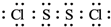 ,
,
故答案为: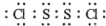 ;
;
②S2Cl2与水反应,有无色刺激性气味气体产生,并有黄色沉淀生成,无色刺激性气味气体除氯化氢外,依据氧化还原反应的元素化合价变化守恒推断,化合价降低的生成黄色沉淀为单质硫,化合价升高的生成二氧化硫气体,依据原子守恒、电子守恒写出化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑,
故答案为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.
(2)①若硫酸铵溶液的浓度为250g/L=
=1.89 mol/L,
故答案为:1.89;
②在Ag+的作用下,过二硫酸盐将Mn2+氧化为MnO4-,同时自身被还原为硫酸根离子,离子方程式为:2Mn2++5S2O82-+8H2O
2MnO4-+10SO42-+10H+,
故答案为:2Mn2++5S2O82-+8H2O
2MnO4-+10SO42-+10H+;
(3)Na2S2O4暴露于空气中易被氧气氧化,则氧化剂为氧气,还原剂为Na2S2O4,又氧化剂和还原剂的物质的量之比为l:1,设Na2S2O4被氧化后硫的化合价为+x价,则根据得失电子守恒,1×4=1×2×(x-3),解得x=5,又有水蒸气参与反应,所以产物为NaHSO4 和NaHSO3,
故答案为:NaHSO4 和NaHSO3;
(4)左边装置是燃料电池,通入氢气的电极是负极、通入氧气的电极是正极,右边装置在电解池,左边Cu是阴极、右边Cu是阳极,阳极上Cu失电子发生氧化反应,电极反应式为Cu-2e-=Cu2+,通入氧气的电极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:Cu-2e-=Cu2+;O2+2H2O+4e-=4OH-.
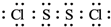 ,
,故答案为:
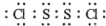 ;
;②S2Cl2与水反应,有无色刺激性气味气体产生,并有黄色沉淀生成,无色刺激性气味气体除氯化氢外,依据氧化还原反应的元素化合价变化守恒推断,化合价降低的生成黄色沉淀为单质硫,化合价升高的生成二氧化硫气体,依据原子守恒、电子守恒写出化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑,
故答案为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.
(2)①若硫酸铵溶液的浓度为250g/L=
| ||
| 1L |
故答案为:1.89;
②在Ag+的作用下,过二硫酸盐将Mn2+氧化为MnO4-,同时自身被还原为硫酸根离子,离子方程式为:2Mn2++5S2O82-+8H2O
| ||
故答案为:2Mn2++5S2O82-+8H2O
| ||
(3)Na2S2O4暴露于空气中易被氧气氧化,则氧化剂为氧气,还原剂为Na2S2O4,又氧化剂和还原剂的物质的量之比为l:1,设Na2S2O4被氧化后硫的化合价为+x价,则根据得失电子守恒,1×4=1×2×(x-3),解得x=5,又有水蒸气参与反应,所以产物为NaHSO4 和NaHSO3,
故答案为:NaHSO4 和NaHSO3;
(4)左边装置是燃料电池,通入氢气的电极是负极、通入氧气的电极是正极,右边装置在电解池,左边Cu是阴极、右边Cu是阳极,阳极上Cu失电子发生氧化反应,电极反应式为Cu-2e-=Cu2+,通入氧气的电极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:Cu-2e-=Cu2+;O2+2H2O+4e-=4OH-.
看了(1)用作橡胶工业的硫化剂S2...的网友还看了以下:
在恒容绝热的条件下进行2A(g)+B(g)→2C(g)+D(s)反应,加入2molA1molB2m 2020-05-17 …
在恒温恒容下发生A(s)=3C(g)+2D(s)反应,某时刻平均相对分子质量保持不变能否判断达到平 2020-05-22 …
静止在匀强磁场中的锂核63Li俘获一个速度为7.7×104m/s的中子而发生核反应,反应中放出α粒 2020-06-20 …
1.一辆火车一20m/s的速度沿平直轨道行驶,在进入隧道前某处鸣笛,经过10s,司机听到从隧道口山 2020-06-27 …
一初中物理题地震时震源的震动一横波和纵波两种方式向外传播,两种波在地壳中的传播速度并不一样,分别约为 2020-12-15 …
某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知 2020-12-25 …
Ⅰ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已 2020-12-25 …
I.某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。 2020-12-25 …
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反 2020-12-25 …
某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知 2020-12-25 …