早教吧作业答案频道 -->化学-->
苯胺是一种良好的黑色燃料,俗称苯胺黑,可以通过如下方式合成(1)基态铁原子价电子排布式为.(2)Fe2+的未成对电子数.(3)组成硝基苯的C、N、O三种元素的电负性由大到小顺序
题目详情
苯胺是一种良好的黑色燃料,俗称苯胺黑,可以通过如下方式合成
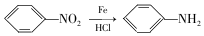
(1)基态铁原子价电子排布式为___.
(2)Fe2+的未成对电子数___.
(3)组成硝基苯的C、N、O三种元素的电负性由大到小顺序是___
(4)CH4、NH3、H2O的键角由小到大的顺序是___
(5)苯胺中的C、N两元素的杂化方式分别是___、___
(6)苯胺在水中的溶解度远大于硝基苯的在水中的溶解度的原因是___
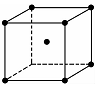
(7)某种单质铁的晶胞结构如图所示,假设铁原子的半径为a nm,则该种铁的密度为___g/cm3.(列出计算表达式)

(1)基态铁原子价电子排布式为___.
(2)Fe2+的未成对电子数___.
(3)组成硝基苯的C、N、O三种元素的电负性由大到小顺序是___
(4)CH4、NH3、H2O的键角由小到大的顺序是___
(5)苯胺中的C、N两元素的杂化方式分别是___、___
(6)苯胺在水中的溶解度远大于硝基苯的在水中的溶解度的原因是___
(7)某种单质铁的晶胞结构如图所示,假设铁原子的半径为a nm,则该种铁的密度为___g/cm3.(列出计算表达式)

▼优质解答
答案和解析
(1)铁是26号元素,其原子核外有26个电子,Fe原子的3d、4s电子为其价电子,根据构造原理书写Fe核外价电子排布式为3d64s2,
故答案为:3d64s2;
(2)Fe2+核外电子排布式为1s22s22p63s23p63d6,在3d上存在4个未成对电子,
故答案为:4;
(3)元素原子的得电子能力越强,则电负性越大,同周期从左到右元素的电负性逐渐增强,所以电负性:O>N>C,
故答案为:O>N>C;
(4)CH4分子中每个碳原子杂化轨道数为4,所以采取sp3杂化,为正四面体,键角为109°28′;
NH3分子中每个氮原子杂化轨道数为4,所以采取sp3杂化,三角锥形,键角为107°18′;
H2O分子中每个氧原子杂化轨道数为4,所以采取sp3杂化,为V形,键角为104.5°;
所以CH4、NH3、H2O的键角由小到大的顺序是:H2O34,
故答案为:H2O34;
(5)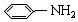 中碳原子杂化轨道数为3,所以采取sp2杂化,N元素全部形成单键,属于sp3杂化,
中碳原子杂化轨道数为3,所以采取sp2杂化,N元素全部形成单键,属于sp3杂化,
故答案为:sp2杂化;sp3杂化;
(6)氢键比范德华力强,是一种介于化学键与分子间作用力之间的作用力,含F、O、N元素的物质中分子内或分子之间能形成氢键,苯胺在水中与水形成氢键,而硝基苯与水不能形成氢键,所以苯胺在水中的溶解度远大于硝基苯的在水中的溶解度,
故答案为:苯胺与水形成氢键,而硝基苯与水不能形成氢键;
(7)Fe晶胞图为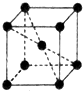 ,单质晶体为体心立方密堆积,晶体中Fe原子的配位数为8,其Fe的原子半径为apm=10-10acm,设晶胞棱长为xcm,则3x2=(4×10-10a)2,故x=
,单质晶体为体心立方密堆积,晶体中Fe原子的配位数为8,其Fe的原子半径为apm=10-10acm,设晶胞棱长为xcm,则3x2=(4×10-10a)2,故x=
a×10-10cm,晶胞中Fe原子数目为1+8×
=2,晶胞质量为
g,
则晶体密度为:
g÷(
a×10-10cm)3=
g/cm3,
故答案为:
.
故答案为:3d64s2;
(2)Fe2+核外电子排布式为1s22s22p63s23p63d6,在3d上存在4个未成对电子,
故答案为:4;
(3)元素原子的得电子能力越强,则电负性越大,同周期从左到右元素的电负性逐渐增强,所以电负性:O>N>C,
故答案为:O>N>C;
(4)CH4分子中每个碳原子杂化轨道数为4,所以采取sp3杂化,为正四面体,键角为109°28′;
NH3分子中每个氮原子杂化轨道数为4,所以采取sp3杂化,三角锥形,键角为107°18′;
H2O分子中每个氧原子杂化轨道数为4,所以采取sp3杂化,为V形,键角为104.5°;
所以CH4、NH3、H2O的键角由小到大的顺序是:H2O
故答案为:H2O
(5)
 中碳原子杂化轨道数为3,所以采取sp2杂化,N元素全部形成单键,属于sp3杂化,
中碳原子杂化轨道数为3,所以采取sp2杂化,N元素全部形成单键,属于sp3杂化,故答案为:sp2杂化;sp3杂化;
(6)氢键比范德华力强,是一种介于化学键与分子间作用力之间的作用力,含F、O、N元素的物质中分子内或分子之间能形成氢键,苯胺在水中与水形成氢键,而硝基苯与水不能形成氢键,所以苯胺在水中的溶解度远大于硝基苯的在水中的溶解度,
故答案为:苯胺与水形成氢键,而硝基苯与水不能形成氢键;
(7)Fe晶胞图为
 ,单质晶体为体心立方密堆积,晶体中Fe原子的配位数为8,其Fe的原子半径为apm=10-10acm,设晶胞棱长为xcm,则3x2=(4×10-10a)2,故x=
,单质晶体为体心立方密堆积,晶体中Fe原子的配位数为8,其Fe的原子半径为apm=10-10acm,设晶胞棱长为xcm,则3x2=(4×10-10a)2,故x=4
| ||
| 3 |
| 1 |
| 8 |
| 2×56 |
| NA |
则晶体密度为:
| 2×56 |
| NA |
4
| ||
| 3 |
21
| ||
| 4a3NA×10-21 |
故答案为:
21
| ||
| 4a3NA×10-21 |
看了苯胺是一种良好的黑色燃料,俗称...的网友还看了以下:
下列有关氢原子电子云图的说法正确的是()A.黑点密度大,电子数目大B.黑点密度大,单位体积内电子出 2020-05-14 …
下列关于电子云的说法中,正确的是A.电子云表示电子在原子核外运动的轨迹B.电子云表示电子在核外单位 2020-05-14 …
关于电子云的下列说法不正确的是()A.s电子绕核旋转,其轨道为一圆圈,而p电子是走∞字形B.s轨道 2020-05-14 …
下列关于电子云的说法中,正确的是()A.电子云表示电子在原子核外运动的轨迹B.电子云表示电子在核外 2020-05-14 …
下列关于电子云的说法中,正确的是()A.电子云图中的小黑点密表示该核外空间的电子多B.电子云可表示 2020-05-14 …
下列关于电子云的描述中,正确的是()A.电子云是一团带负电荷的云雾B.每个小黑点表示一个核外电子C 2020-05-14 …
下列说法中正确的是()A.所有的电子在同一区域里运动B.同一原子中,1s、2s、3s所能容纳的电子 2020-05-14 …
一电子仅受电场力作用,从高电势处移动到低电势处,则()A.电场力对电子做正功B.电子的电势能减少C 2020-05-15 …
电离H+的关系,不是化学精英可跳过1.乙醇中性因为停机的推电子,苯酚弱酸性因为苯基的吸电子,乙酸显 2020-05-22 …
我国政府规定在2006年7月1日后将含有铜、铬、镉、汞、多溴联苯等材料的电子产品禁止投放市场.下列有 2020-12-31 …