早教吧作业答案频道 -->化学-->
A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,其相关信息如下:相关信息A所处的周期数、族序数分别与其原子序数相等B原子核外电子有4种不同的运动
题目详情
A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,其相关信息如下:
请回答下列问题:
(1)F位于元素周期表第___族,其简化电子排布式为___.
(2)D元素基态原子中能量最高的电子,其电子云在空间有___个方向,原子轨道呈___形.
(3)某同学根据上述信息,推断E基态原子的核外电子排布图为: ,该同学所画的电子排布图违背了___.
,该同学所画的电子排布图违背了___.
(4)A与D形成的D2A4分子中D原子的杂化类型为___杂化,A与D形成的最简单分子易溶于水的原因___.
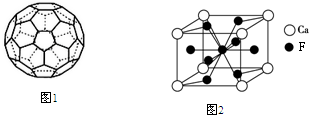
(5)C的一种单质相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环(如图1).则1个这种单质分子中所含π键的数目为___.
(6)已知在元素周期表中存在“对角线规则”,即周期表中左上方与右下方元素它们的单质及其化合物的性质相似,如Li和Mg,试写出向BeCl2溶液中加入过量的NaOH溶液反应的化学方程式:___.
(7)图2是金属Ca和F所形成的某种合金的晶胞结构示意图,已知镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力.已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=___(填数值);氢在合金中的密度为___.
| 相关信息 | |
| A | 所处的周期数、族序数分别与其原子序数相等 |
| B | 原子核外电子有4种不同的运动状态 |
| C | 元素原子的核外成对电子数是未成对电子数的2倍且有3个能级 |
| D | 元素原子的核外p电子数比s电子数少1 |
| E | E原子的第一至第四电离能如下:I1=738 kJ•mol-1 I2=1451 kJ•mol-1 I3=7733 kJ•mol-1 I4=10540 kJ•mol-1 |
| F | 第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满 |
(1)F位于元素周期表第___族,其简化电子排布式为___.
(2)D元素基态原子中能量最高的电子,其电子云在空间有___个方向,原子轨道呈___形.
(3)某同学根据上述信息,推断E基态原子的核外电子排布图为:
 ,该同学所画的电子排布图违背了___.
,该同学所画的电子排布图违背了___.(4)A与D形成的D2A4分子中D原子的杂化类型为___杂化,A与D形成的最简单分子易溶于水的原因___.
(5)C的一种单质相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环(如图1).则1个这种单质分子中所含π键的数目为___.

(6)已知在元素周期表中存在“对角线规则”,即周期表中左上方与右下方元素它们的单质及其化合物的性质相似,如Li和Mg,试写出向BeCl2溶液中加入过量的NaOH溶液反应的化学方程式:___.
(7)图2是金属Ca和F所形成的某种合金的晶胞结构示意图,已知镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力.已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=___(填数值);氢在合金中的密度为___.
▼优质解答
答案和解析
A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,A所处的周期数、族序数分别与其原子序数相等,则A为H元素;
B原子核外电子有4种不同的运动状态,则B为Be元素;
C元素原子的核外成对电子数是未成对电子数的2倍且有3个能级,为C元素;
D元素原子的核外p电子数比s电子数少1,则D为N元素;
E原子的第一至第四电离能如下:I1=738 kJ•mol-1、I2=1451 kJ•mol-1、I3=7733 kJ•mol-1、I4=10540 kJ•mol-1,为第IIIA族元素,为Al元素;
F为第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,为Cu元素;
(1)F是Cu元素,原子核外有29个电子,位于第四周期第IB族,根据构造原理书写其核外电子排布式为[Ar]3d104s1 ,
故答案为:IB;[Ar]3d104s1 ;
(2)D是N元素,D元素基态原子中能量最高的电子是2p电子,p电子电子云有3种,原子轨道为哑铃形,
故答案为:3;哑铃;
(3)泡利原理为同一轨道中不能有自旋方向相同的两个电子,根据图知,该原子核外电子排布违反泡利原理,故答案为:泡利原理;
(4)H与N形成的N2H4分子中每个N原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断N原子的杂化类型为sp3,氨气和水分子之间形成氢键而促进氨气溶解,所以氨气易溶于水;
故答案为:sp3;氨气分子能与水分子形成氢键;
(5)碳元素的一种单质相对分子质量为720,则该分子为C60,分子构型为一个32面体,其中有12个五元环,20个六元环,每个碳周围有一个碳碳双键和两个碳碳单键,均为两个碳共用,所以每个碳实际占有的碳碳双键数为0.5,而每个双键中有一个π键,所以C60中π键的数目为60×0.5=30,
故答案为:30;
(6)根据对角线规则知,Be元素和Al元素性质相似,根据氯化铝与NaOH的反应写出BeCl2与NaOH的反应方程式为BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O,
故答案为:BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O;
(7)该晶胞中白色球个数=8×
=1、黑色球个数=1+8×
=5,根据化学式知,n=5;密度=
=
g•cm-3=0.083 g•cm-3,
故答案为:5;0.083 g•cm-3.
B原子核外电子有4种不同的运动状态,则B为Be元素;
C元素原子的核外成对电子数是未成对电子数的2倍且有3个能级,为C元素;
D元素原子的核外p电子数比s电子数少1,则D为N元素;
E原子的第一至第四电离能如下:I1=738 kJ•mol-1、I2=1451 kJ•mol-1、I3=7733 kJ•mol-1、I4=10540 kJ•mol-1,为第IIIA族元素,为Al元素;
F为第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,为Cu元素;
(1)F是Cu元素,原子核外有29个电子,位于第四周期第IB族,根据构造原理书写其核外电子排布式为[Ar]3d104s1 ,
故答案为:IB;[Ar]3d104s1 ;
(2)D是N元素,D元素基态原子中能量最高的电子是2p电子,p电子电子云有3种,原子轨道为哑铃形,
故答案为:3;哑铃;
(3)泡利原理为同一轨道中不能有自旋方向相同的两个电子,根据图知,该原子核外电子排布违反泡利原理,故答案为:泡利原理;
(4)H与N形成的N2H4分子中每个N原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断N原子的杂化类型为sp3,氨气和水分子之间形成氢键而促进氨气溶解,所以氨气易溶于水;
故答案为:sp3;氨气分子能与水分子形成氢键;
(5)碳元素的一种单质相对分子质量为720,则该分子为C60,分子构型为一个32面体,其中有12个五元环,20个六元环,每个碳周围有一个碳碳双键和两个碳碳单键,均为两个碳共用,所以每个碳实际占有的碳碳双键数为0.5,而每个双键中有一个π键,所以C60中π键的数目为60×0.5=30,
故答案为:30;
(6)根据对角线规则知,Be元素和Al元素性质相似,根据氯化铝与NaOH的反应写出BeCl2与NaOH的反应方程式为BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O,
故答案为:BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O;
(7)该晶胞中白色球个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
| ||
| V |
| ||
| 9.0×10-23 |
故答案为:5;0.083 g•cm-3.
看了A、B、C、D、E、F为前四周...的网友还看了以下:
X、Y、Z、W是元素周期表短周期中的四种常见元素,其相关信息如下表:元素相关信息XX的原子核外3个 2020-04-08 …
阅读下表中短周期主族元素的相关信息.元素代号相关信息AA单质能与冷水剧烈反应,得到强碱性溶液BB原 2020-05-14 …
A、B、C、D、E是元素周期表前四周期中的五种常见元素,其相关信息如下表:元素相关信息AA原子的1 2020-06-09 …
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表: 2020-06-09 …
四种短周期元素的相关信息如表所示:元素相关信息X它存在多种同素异形体,可用于制作钻头、电极和纳米材 2020-06-25 …
现有甲、乙、丙三种元素,其原子序数都不超过20.有关信息如下:元素代号相关信息甲n为电子层数,甲原 2020-07-07 …
X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:元素相关信息XX原子的L层电子数是 2020-11-01 …
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如表:元素相关信息XX最外层电子数是次 2020-11-01 …
X、Y、W、M、N五种元素分别位于周期表中三个紧邻的周期,且原子序数依次增大,其相关信息如下表:元素 2020-11-17 …
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:元 2020-12-05 …