早教吧作业答案频道 -->化学-->
为测定碱式碳酸钴[COx(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究.已知:碱式碳酸钴受热时可分解生成三种氧化物.(1)按如图所示装置组装好
题目详情
为测定碱式碳酸钴[COx(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究.已知:碱式碳酸钴受热时可分解生成三种氧化物.
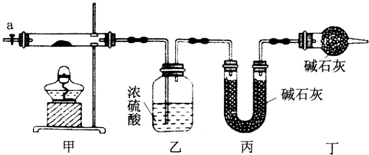
(1)按如图所示装置组装好仪器,并___;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中___(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是___.
(2)某同学认为上述实验中存在一个缺陷,该缺陷是___.
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为___.
(4)CoCl2•6H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取COCl2•6H2O的一种工艺如下:
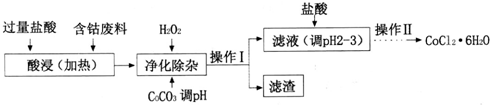
已知;25℃时
①净化除杂时,加入H2O2发生反应的离子方程式为___;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为___;
③加盐酸调整pH为2~3的目的为___;
④操作Ⅱ过程为蒸发浓缩、冷却结晶、过滤.

(1)按如图所示装置组装好仪器,并___;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中___(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是___.
(2)某同学认为上述实验中存在一个缺陷,该缺陷是___.
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为___.
(4)CoCl2•6H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取COCl2•6H2O的一种工艺如下:

已知;25℃时
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为___;
③加盐酸调整pH为2~3的目的为___;
④操作Ⅱ过程为蒸发浓缩、冷却结晶、过滤.
▼优质解答
答案和解析
(1)按如图所示装置组装好仪器,应首先检验装置的气密性,加热甲中玻璃管,当乙装置中不再有气泡产生,即碱式碳酸钴分解完毕,步骤中缓缓通入空气数分钟,将装置中生成的CO2和H2O全部排入乙、丙装置中,以免影响测量结果,
故答案为:检验装置的气密性,不再有气泡产生,将装置中生成的CO2和H2O全部排入乙、丙装置中;
(2)空气中的水蒸气和二氧化碳被乙丙装置吸收产生误差,在活塞a前,加装装置干燥管,装置中盛放的碱石灰用来吸收空气中的水蒸气和二氧化碳;
故答案为:未考虑空气中的水蒸气和二氧化碳对实验的影响;
(3)碱式碳酸钴样品3.65g,故生成水的质量为0.36g,物质的量为
=0.02mol,生成二氧化碳的质量为0.88g,物质的量为
=0.02mol,故氧化钴的质量为3.65g-0.36g-0.88g=2.41g,物质的量为
=0.03mol,根据Co、H、C元素守恒可知,x:y:z=0.03mol:0.02mol×2:0.02mol=3:4:2,故碱式碳酸钴的化学式为Co3(OH)4(CO3)2,故答案为:Co3(OH)4(CO3)2;
(4)①三价铁离子易转化为沉淀,所以要加入氧化剂过氧化氢把二价铁离子氧化为三价铁离子,而不会引入新的杂质,反应的离子方程式为;2Fe2++H2O2+2H+=2Fe3++2H2O;
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②废料加入盐酸后生成氯化物,然后加入双氧水,二价铁离子被双氧水氧化生成三价铁离子,根据沉淀的pH值表格知,当溶液的pH值为5.2时,铁离子和铝离子被完全沉淀,当溶液的pH值为7.6时,钴离子才开始产生沉淀,所以要想将铁离子、铝离子和钴离子分离,溶液的pH值应该不小于5.2不大于7.6,则操作I获得的滤渣成分为Fe(OH)3和Al(OH)3;
故答案为:Fe(OH)3和Al(OH)3;
③加盐酸调整pH为2~3的目的为抑制CoCl2的水解,故答案为:抑制CoCl2的水解.
故答案为:检验装置的气密性,不再有气泡产生,将装置中生成的CO2和H2O全部排入乙、丙装置中;
(2)空气中的水蒸气和二氧化碳被乙丙装置吸收产生误差,在活塞a前,加装装置干燥管,装置中盛放的碱石灰用来吸收空气中的水蒸气和二氧化碳;
故答案为:未考虑空气中的水蒸气和二氧化碳对实验的影响;
(3)碱式碳酸钴样品3.65g,故生成水的质量为0.36g,物质的量为
| 0.36g |
| 18g/mol |
| 0.88g |
| 44g/mol |
| 2.41g |
| 75g/mol |
(4)①三价铁离子易转化为沉淀,所以要加入氧化剂过氧化氢把二价铁离子氧化为三价铁离子,而不会引入新的杂质,反应的离子方程式为;2Fe2++H2O2+2H+=2Fe3++2H2O;
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②废料加入盐酸后生成氯化物,然后加入双氧水,二价铁离子被双氧水氧化生成三价铁离子,根据沉淀的pH值表格知,当溶液的pH值为5.2时,铁离子和铝离子被完全沉淀,当溶液的pH值为7.6时,钴离子才开始产生沉淀,所以要想将铁离子、铝离子和钴离子分离,溶液的pH值应该不小于5.2不大于7.6,则操作I获得的滤渣成分为Fe(OH)3和Al(OH)3;
故答案为:Fe(OH)3和Al(OH)3;
③加盐酸调整pH为2~3的目的为抑制CoCl2的水解,故答案为:抑制CoCl2的水解.
看了为测定碱式碳酸钴[COx(OH...的网友还看了以下:
(2013•崇明县二模)龙胆酸甲酯是制取抗心律失常药物--氟卡尼的中间体.已知:I、龙胆酸甲酯结构 2020-05-17 …
已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱.可以将转变为的方法是()①与足量的NaOH溶液共热, 2020-06-25 …
(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为.PbO2可由PbO与次氯酸钠溶液反应 2020-07-21 …
已知甲酸(HCOOH)与浓硫酸共热到60~80℃可发生脱水型的分解反应,并由此而制得CO气体.实验 2020-07-24 …
已知甲酸(HCOOH)与浓硫酸共热到60~80℃可发生脱水型的分解反应,并由此而制得CO气体.实验 2020-07-24 …
已知甲酸(HCOOH)与浓硫酸共热到60~80℃可发生脱水型的分解反应,并由此而制得CO气体.实验 2020-07-24 …
高一化学题目将26.1克二氧化锰与160克36.5%盐酸共热,如不考虑氯化氢损失,在反应后的溶液中 2020-07-29 …
醋酸钠过饱和溶液吸热的放热的温度?我在网上查到醋酸钠的熔点是58.2度,属于中低温储热材料.我想知道 2020-11-05 …
氯酸钾热分解是实验室制取氧气的一种方法,某探究小组查阅资料得知,氯酸钾在不同条件下分解结果如下:实验 2020-12-25 …
氯酸钾热分解是实验室制取氧气的一种方法,某探究小组查阅资料得知,氯酸钾在不同条件下分解结果如下:实验 2020-12-25 …