早教吧作业答案频道 -->化学-->
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄As2S3和雄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药.(1).砷元素有+2、+3两种常见价态.
题目详情
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄As2S3和雄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药.
(1).砷元素有+2、+3两种常见价态.一定条件下,雌黄和雄黄的转化关系如图1所示.
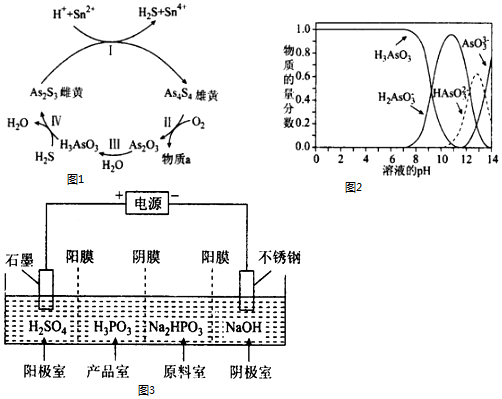
①Ⅰ中,氧化剂是___.
②Ⅱ中,若1mol As4S4反应,转移28mol e-,写出Ⅱ的化学方程式:___.
(2)Ⅲ中产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分
数与溶液的pH 关系如图2所示.
①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是___.
②下列说法不正确的是___(填字母序号).
a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中:c(H2AsO3-)+2c(HAsO32-)+3c(AsO3-)+c(OH-)=c(OH+)
c.在K3AsO3溶液中,c((AsO3-)>c(HAsO32-)>c(H2AsO3-)
③将KOH溶液滴人亚砷酸溶液,当pH调至11时发生反应的离子方程式是___.
(3)P和As屈于同主族元素,存在亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3.
①Na2HPO3为___(填“正盐”或“酸式盐”),推测Na2HPO3溶液PH___7(填“>”“<”或“=”).
②工业电解Na2HPO3溶液可得到亚磷酸,装置示意图如图3:
阴极的电极反应式为,产品室中反应的离子方程式为___.
(1).砷元素有+2、+3两种常见价态.一定条件下,雌黄和雄黄的转化关系如图1所示.

①Ⅰ中,氧化剂是___.
②Ⅱ中,若1mol As4S4反应,转移28mol e-,写出Ⅱ的化学方程式:___.
(2)Ⅲ中产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分
数与溶液的pH 关系如图2所示.
①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是___.
②下列说法不正确的是___(填字母序号).
a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中:c(H2AsO3-)+2c(HAsO32-)+3c(AsO3-)+c(OH-)=c(OH+)
c.在K3AsO3溶液中,c((AsO3-)>c(HAsO32-)>c(H2AsO3-)
③将KOH溶液滴人亚砷酸溶液,当pH调至11时发生反应的离子方程式是___.
(3)P和As屈于同主族元素,存在亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3.
①Na2HPO3为___(填“正盐”或“酸式盐”),推测Na2HPO3溶液PH___7(填“>”“<”或“=”).
②工业电解Na2HPO3溶液可得到亚磷酸,装置示意图如图3:
阴极的电极反应式为,产品室中反应的离子方程式为___.
▼优质解答
答案和解析
(1)①Ⅰ中Sn的化合价升高,As的化合价降低,所以As2S3在反应中得电子作氧化剂;
故答案为:As2S3;
②Ⅱ中,若1molAs4S4反应转移28mole-,则反应消耗7mol氧气,则反应的方程式为:As4S4+7O2
2As2O3+4SO2;
故答案为:As4S4+7O2
2As2O3+4SO2;
(2)①由图象可知,pH在7.35-7.45之间,溶液中含砷元素的主要微粒是H3AsO3;
故答案为:H3AsO3;
②a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液的pH=9,所以溶液显碱性,故a正确;
b.pH=12时,溶液显碱性,则c(OH-)>c(H+),所以c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)>c(H+),故b错误;
c.在K3AsO3溶液中,存在三步水解,以第一步水解为主,第一步水解生成HAsO32-,第二步水解生成H2AsO3-,则c(AsO33-)>c(HAsO32-)>c(H2AsO3-),故c正确;
故答案为:b;
③将KOH 溶液滴入亚砷酸溶液,当pH 调至11时,亚砷酸与氢氧根离子反应生成H2AsO3-,其反应的离子方程为:H3AsO3+OH-=H2AsO3-+H2O;
故答案为:H3AsO3+OH-=H2AsO3-+H2O;
(3)①亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3,说明盐为正盐,亚磷酸为弱酸,则 Na2HPO3为强碱弱酸盐,溶液显碱性,溶液PH>7,
故答案为:正盐;>;
②阴极上得电子发生还原反应,电极反应式为2H++2e-=H2↑;产品室中HPO32-和氢离子结合生成亚磷酸,反应离子方程式为:HPO32-+2H+=H3PO3,
故答案为:2H++2e-=H2↑;HPO32-+2H+=H3PO3.
故答案为:As2S3;
②Ⅱ中,若1molAs4S4反应转移28mole-,则反应消耗7mol氧气,则反应的方程式为:As4S4+7O2
| ||
故答案为:As4S4+7O2
| ||
(2)①由图象可知,pH在7.35-7.45之间,溶液中含砷元素的主要微粒是H3AsO3;
故答案为:H3AsO3;
②a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液的pH=9,所以溶液显碱性,故a正确;
b.pH=12时,溶液显碱性,则c(OH-)>c(H+),所以c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)>c(H+),故b错误;
c.在K3AsO3溶液中,存在三步水解,以第一步水解为主,第一步水解生成HAsO32-,第二步水解生成H2AsO3-,则c(AsO33-)>c(HAsO32-)>c(H2AsO3-),故c正确;
故答案为:b;
③将KOH 溶液滴入亚砷酸溶液,当pH 调至11时,亚砷酸与氢氧根离子反应生成H2AsO3-,其反应的离子方程为:H3AsO3+OH-=H2AsO3-+H2O;
故答案为:H3AsO3+OH-=H2AsO3-+H2O;
(3)①亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3,说明盐为正盐,亚磷酸为弱酸,则 Na2HPO3为强碱弱酸盐,溶液显碱性,溶液PH>7,
故答案为:正盐;>;
②阴极上得电子发生还原反应,电极反应式为2H++2e-=H2↑;产品室中HPO32-和氢离子结合生成亚磷酸,反应离子方程式为:HPO32-+2H+=H3PO3,
故答案为:2H++2e-=H2↑;HPO32-+2H+=H3PO3.
看了中国自古有“信口雌黄”、“雄黄...的网友还看了以下:
画油画时95%的酒精可以代替松节油吗?酒精对油画颜料有没有溶解作用,可以洗笔和稀释颜料吗?我说的是 2020-05-15 …
我用丙烯颜料(并未兑水)在玻璃杯上画了些图案,已干,但问题是遇水会整片脱落.我想问画过的XDJM怎 2020-06-28 …
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄As2S3和雄黄As4S4都是自然界中常见的砷化物, 2020-07-10 …
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄(As2S3)和雄黄(As4S4)都是自然界中常见的 2020-07-10 …
中国自古有“信口雌黄”、“雄黄入药”之说。雌黄和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料 2020-07-10 …
砷(As)及其化合物在生产、医疗、科技等方面有许多应用(1)中国自古“信口雌黄”、“雄黄入药”之说. 2020-11-01 …
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄As2S3和雄As4S4都是自然界中常见的砷化物,早期 2020-11-01 …
关于国画画家及其艺术风格的英语作文简称“国画”,在本世界美术领域内自成都市独特体系.它用毛笔、墨,和 2020-12-01 …
小兔在给蛋涂颜色:红色、黄色、蓝色.它在一个窝里放3个彩蛋,有哪几种放法,把它们都画出来.1、3个红 2020-12-08 …
小兔在给蛋涂颜色:红色、黄色、蓝色.它在一个窝里放3个彩蛋,有哪几种放法,把它们都画出来.1、3个红 2020-12-08 …