卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子.若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁.若要求产品尽量不含杂质,而且生产成本较
卤块的主要成分是MgCl 2 ,此外还含Fe 3+ 、Fe 2+ 和Mn 2+ 等离子.若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁.
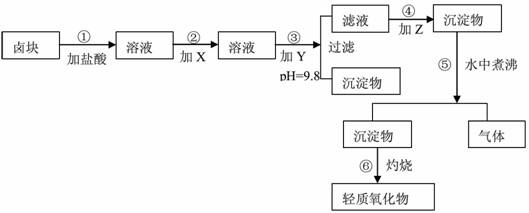
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
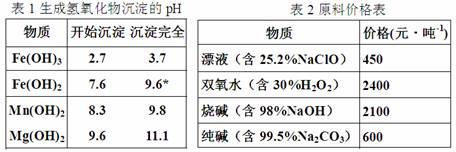
Fe 2+ 氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe 3+ ,生成Fe(OH) 3 沉淀除去.(1)在步骤②中加入的试剂X,最佳的选择是 ,漂液
其作用是
(2)在步骤③中加入的试剂应是 NaOH
;之所以要控制pH=9.8,其目的是
。
(3)在步骤④中加入的试剂Z应是 纯碱
;
(4)在步骤⑤中发生的反应是 。 MgCO 3 +H 2 O=Mg(OH) 2 +CO 2
(5)在实验室中,为了除去MgCl 2 酸性溶液中的Fe 3+ 而得到较纯净的MgCl 2 溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是 。
A.NH 3 ·H 2 O B.NaOH C.Na 2 CO 3 D.MgCO 3
(6)已知MgCl 2 ·6H 2 O受热时发生水解:MgCl 2 ·6H 2 O=Mg(OH)Cl+HCl↑+5H 2 O而MgSO 4 ·7H 2 O受热不易发生水解。试解释原因
。
(7)过滤后的沉淀往往需要洗涤,而选择洗涤沉淀的试剂需要考虑沉淀的损失,例如:分别用等体积的蒸馏水和0.010mol/L硫酸洗涤BaSO 4 沉淀, 用水洗涤造成BaSO 4 的损失量大于用稀硫酸洗涤的损失量。试利用平衡移动原理进行解释
。
(1)漂液/NaClO [1分] 将Fe 2+ 氧化为Fe 3+ ; [2分]
(2)烧碱/NaOH [1分] 使Mg 2+ 以外的杂质转化为氢氧化物沉淀除去 [2分]
(3)纯碱/Na 2 CO 3 [1分]
(4)MgCO 3 +H 2 O Mg(OH) 2 +CO 2 ↑ [2分]
Mg(OH) 2 +CO 2 ↑ [2分]
(5)D [1分]
(6)受热时,MgCl 2 •6H 2 O水解反应的生成物HCl逸出反应体系,相当于不断减少可逆反应的生成物,从而使平衡不断向水解反应方向移动;MgSO 4 •7H 2 O没有类似的可促进水解反应进行的情况。 [2分]
(7)硫酸溶液的SO 4 2- 对BaSO 4 的沉淀溶解平衡有促进平衡向生成沉淀的方向移动的作用。 [2分]
艺术品的艺术价值是艺术品的生命吗?想买好的艺术品来收藏,目前哪些艺术品最有潜力?当一件优秀的艺术作 2020-05-17 …
2011年3月,胡润研究院发布“2010胡润艺术榜”,艺术榜是依据2010年度公开拍卖市场作品的总 2020-06-12 …
温州龙港礼品城某店经销一种工艺品,已投资3000元进行店面装修.已知这种工艺品单个成本50元.据调 2020-06-12 …
求各位高手帮解答一道税务筹划的题目题目是这样的,某日用化妆品厂,将生产的化妆品、护肤护发品、小工艺 2020-07-15 …
中国古代文学艺术璀璨夺目,出现了很多珍品.下列说法正确的是[]A,东汉末中国古代文学艺术璀璨夺目, 2020-07-28 …
阅读下面的作品,完成下列各题。从脸谱说起叶秀山脸谱在京剧艺术中不可或缺,实在是我国艺术家对世界艺术作 2020-11-06 …
顾客请一位工艺师把、两件玉石原料各制成一件工艺品,工艺师带一位徒弟完成这项任务,每件原料先由徒弟完成 2020-11-06 …
/小红买了一件甲乙合金的工艺品.小组成员测出:质量为360g体积为24cm3密度为(应该是15*10 2020-12-02 …
阅读下面的作品,完成1—4题。墨点无多泪点多裴志强①有人把中国书画艺术分为三大类:一类为“洗眼”的艺 2020-12-04 …
阅读下面的作品,完成下列各题。文艺作品要超越“戾气”张颐武一些文艺作品中存在“戾气”横行的情况,这样 2021-01-14 …