早教吧作业答案频道 -->化学-->
素有“铜都”之称的安徽铜陵有许多黄铜矿(主要成分为CuFeS2).黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4.某同学通过废铁屑与溶液甲反应,制取补血剂原料碳
题目详情
素有“铜都”之称的安徽铜陵有许多黄铜矿(主要成分为CuFeS2).黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4.某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜.主要步骤如图所示:
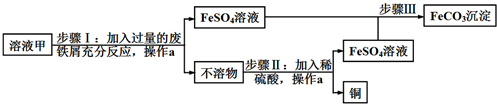
(1)Fe2(SO4)3与铁反应的化学方程式如下,请配平:xFe2(SO4)3+yFe═zFeSO4,其中x、y、z为化学计量数,z的值为___.
(2)步骤Ⅰ中,生成铜的化学方程式:___. 废铁屑含有少量铁锈,对产物的成分没有影响,原因是___.
(3)操作a名称为___.实验室中操作a要用到玻璃棒、烧杯和___等玻璃仪器.
(4)不溶物的成分为___(填化学式).

(1)Fe2(SO4)3与铁反应的化学方程式如下,请配平:xFe2(SO4)3+yFe═zFeSO4,其中x、y、z为化学计量数,z的值为___.
(2)步骤Ⅰ中,生成铜的化学方程式:___. 废铁屑含有少量铁锈,对产物的成分没有影响,原因是___.
(3)操作a名称为___.实验室中操作a要用到玻璃棒、烧杯和___等玻璃仪器.
(4)不溶物的成分为___(填化学式).
▼优质解答
答案和解析
(1)通过分析xFe2(SO4)3+yFe=zFeSO4可知,依据化合价的升降,将方程式配平,所以Fe2(SO4)3+2Fe=3FeSO4,z的值为3;
(2)溶液甲中含有硫酸铜,硫酸铜和加入的铁屑反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁;
(3)由流程图可知,操作a是将固体与液体分离,名称是过滤,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(4)所得“不溶物”中含两种金属,其成分是剩余的铁和置换出的铜.
故答案为:(1)3;
(2)Fe+CuSO4═FeSO4+Cu,铁锈可与硫酸反应生成硫酸铁,硫酸铁再和铁反应生成硫酸亚铁;
(3)过滤,漏斗;
(4)Cu、Fe.
(2)溶液甲中含有硫酸铜,硫酸铜和加入的铁屑反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁;
(3)由流程图可知,操作a是将固体与液体分离,名称是过滤,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(4)所得“不溶物”中含两种金属,其成分是剩余的铁和置换出的铜.
故答案为:(1)3;
(2)Fe+CuSO4═FeSO4+Cu,铁锈可与硫酸反应生成硫酸铁,硫酸铁再和铁反应生成硫酸亚铁;
(3)过滤,漏斗;
(4)Cu、Fe.
看了素有“铜都”之称的安徽铜陵有许...的网友还看了以下:
已知集合s是满足下列条件的函数f(4)的全体:在定义域内存在实数40,使口f(40+1)=f(40 2020-05-13 …
有一段带塑料绝缘皮的铜导线,其质量为m,长度为L,已知其绝缘皮的密度为ρ塑,截面积为S塑,铜的密度 2020-06-21 …
80℃时,将饱和硫酸铜溶液310g加热蒸发掉100g水,再冷却至30℃,可析出g胆矾晶体.(80℃ 2020-06-25 …
初一科学在一充满水的直自来水管的一端敲击一下,要在另一端听到三声,则此水管的长度至少为多长?(已知 2020-07-06 …
80℃时,将饱和硫酸铜溶液310g加热蒸发掉100g水,再冷却至30℃,可析出g胆矾晶体.(80℃ 2020-07-09 …
Fe2(SO4)3+h2o+na2co3=na2fe6(so4)4(oh)12+na2so4+co 2020-07-21 …
黄铜矿(CuFeS2)是炼钢的最主要矿物.(1)S位于周期表中族,该族元素氢化物中,H2Te比H2 2020-07-29 …
离子反应:BaSO4(s)+CO3^2-==BaCO3(s)+SO4^2-,计算该反应的平衡常数答案 2020-11-03 …
20、有一个字符串变量s,要得到该字符串变量从第3个字符开始的共4个字符的函数是()。A.Right 2020-11-07 …
一个由1个定滑轮和1个动滑轮组成的滑轮组,n=3测出的4组值G都为3N,F都为1.2N,s和h是变量 2020-11-20 …