早教吧作业答案频道 -->化学-->
某实验小组同学模拟工业制碘的方法,探究ClO3-和I-的反应规律.实验操作及现象如表:实验及试剂编号无色NaClO3溶液用量试管中溶液颜色淀粉KI试纸颜色10.05mL浅黄
题目详情
某实验小组同学模拟工业制碘的方法,探究ClO3-和I-的反应规律.实验操作及现象如表:
(1)取实验2后的溶液,进行如图实验:
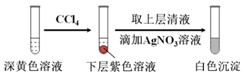
经检验,上述白色沉淀是AgCl.写出加入0.20mL NaClO3后,溶液中ClO3-和I-发生反应的离子方程式:___.
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-.
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)
中的反应产物继续反应,同时生成Cl2.
进行实验:
①取少量实验4中的无色溶液进行如图实验,进一步佐证其中含有IO3-.
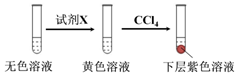
其中试剂X可以是___(填字母序号).
a.碘水b.KMnO4溶液c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL 1.33mol•L-1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化.进行以上对比实验的目的是___,进一步佐证实验4中生成了Cl2.获得结论:NaClO3溶液用量增加导致溶液褪色的原因是___(用离子方程式表示).
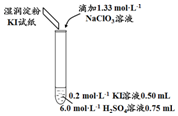
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
①对比实验4和5,可以获得的结论是___.
②用离子方程式解释实验6的现象:___.
| 实验及试剂 | 编号 | 无色NaClO3 溶液用量 | 试管中 溶液颜色 | 淀粉KI 试纸颜色 |
 | 1 | 0.05 mL | 浅黄色 | 无色 |
| 2 | 0.20 mL | 深黄色 | 无色 | |
| 3 | 0.25 mL | 浅黄色 | 蓝色 | |
| 4 | 0.30 mL | 无色 | 蓝色 |

经检验,上述白色沉淀是AgCl.写出加入0.20mL NaClO3后,溶液中ClO3-和I-发生反应的离子方程式:___.
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-.
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)
中的反应产物继续反应,同时生成Cl2.
进行实验:
①取少量实验4中的无色溶液进行如图实验,进一步佐证其中含有IO3-.

其中试剂X可以是___(填字母序号).
a.碘水b.KMnO4溶液c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL 1.33mol•L-1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化.进行以上对比实验的目的是___,进一步佐证实验4中生成了Cl2.获得结论:NaClO3溶液用量增加导致溶液褪色的原因是___(用离子方程式表示).
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
| 编号 | 6.0 mol•L-1 H2SO4溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
| 5 | 0.25 mL | 浅黄色 | 无色 |
| 6 | 0.85 mL | 无色 | 蓝色 |
②用离子方程式解释实验6的现象:___.
▼优质解答
答案和解析
(1)加入0.20mL NaClO3后,溶液颜色变为深黄色,淀粉KI试纸颜色变蓝色,说明氯酸根离子具有氧化性能氧化碘离子为单质碘,反应的离子方程式为:ClO3-+6I-+6H+═Cl-+3I2+3H2O,
故答案为:ClO3-+6I-+6H+═Cl-+3I2+3H2O;
(2)①取少量实验4中的无色溶液进行如图实验,无色溶液中加入试剂X变为黄色,加入四氯化碳萃取得到下层紫红色,说明生成了碘单质,加入的试剂具有还原性,能和碘酸根离子发生氧化还原反应生成碘单质,选择c选项的NaHSO3溶液,a选项含碘单质不能验证,b为高锰酸钾溶液具有氧化性,不符合要求,进一步佐证其中含有IO3-,所选试剂为c,
故答案为:c;
②将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL 1.33mol•L-1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化,说明无碘单质生成,排除易升华的I2对湿润淀粉KI试纸检验Cl2的干扰,NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2;说明是氯气的氧化性以后碘离子生成了碘单质;NaClO3溶液用量增加导致溶液褪色的原因是氯酸根离子以后碘单质为碘酸根离子,反应的离子方程式为:2ClO3-+I2═Cl2↑+2IO3-,
故答案为:排除易升华的I2对湿润淀粉KI试纸检验Cl2的干扰;2ClO3-+I2═Cl2↑+2IO3-;
(3)①对比实验5和6,硫酸用量不同试管中溶液颜色不同说明氢离子浓度不同氯酸根离子以后碘离子产物不同,获得的结论是ClO3-和I-的反应规律与H+(或H2SO4)的用量有关,
故答案为:ClO3-和I-的反应规律与H+(或H2SO4)的用量有关;
②实验6的现象是氯酸根离子以后碘离子生成碘酸根,通式生成氯气能使湿润的淀粉KI试纸变蓝色,反应的离子方程式为:6ClO3-+5I-+6H+═3Cl2↑+5IO3-+3H2O,
故答案为:6ClO3-+5I-+6H+═3Cl2↑+5IO3-+3H2O.
故答案为:ClO3-+6I-+6H+═Cl-+3I2+3H2O;
(2)①取少量实验4中的无色溶液进行如图实验,无色溶液中加入试剂X变为黄色,加入四氯化碳萃取得到下层紫红色,说明生成了碘单质,加入的试剂具有还原性,能和碘酸根离子发生氧化还原反应生成碘单质,选择c选项的NaHSO3溶液,a选项含碘单质不能验证,b为高锰酸钾溶液具有氧化性,不符合要求,进一步佐证其中含有IO3-,所选试剂为c,
故答案为:c;
②将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL 1.33mol•L-1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化,说明无碘单质生成,排除易升华的I2对湿润淀粉KI试纸检验Cl2的干扰,NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2;说明是氯气的氧化性以后碘离子生成了碘单质;NaClO3溶液用量增加导致溶液褪色的原因是氯酸根离子以后碘单质为碘酸根离子,反应的离子方程式为:2ClO3-+I2═Cl2↑+2IO3-,
故答案为:排除易升华的I2对湿润淀粉KI试纸检验Cl2的干扰;2ClO3-+I2═Cl2↑+2IO3-;
(3)①对比实验5和6,硫酸用量不同试管中溶液颜色不同说明氢离子浓度不同氯酸根离子以后碘离子产物不同,获得的结论是ClO3-和I-的反应规律与H+(或H2SO4)的用量有关,
故答案为:ClO3-和I-的反应规律与H+(或H2SO4)的用量有关;
②实验6的现象是氯酸根离子以后碘离子生成碘酸根,通式生成氯气能使湿润的淀粉KI试纸变蓝色,反应的离子方程式为:6ClO3-+5I-+6H+═3Cl2↑+5IO3-+3H2O,
故答案为:6ClO3-+5I-+6H+═3Cl2↑+5IO3-+3H2O.
看了某实验小组同学模拟工业制碘的方...的网友还看了以下:
1.臭氧的化学式2.二氧化碳的颜色3.一氧化碳的颜色4.二氧化硫的颜色5.二氧化氮的颜色6.一氧化 2020-05-14 …
金属指示剂是利用()和()颜色的不同,通过在化学计量点时其颜色的变化指示终点的. 2020-06-02 …
数学题一道,有一定的难度.有10个同学站成一排,学校要给每个同学戴上不同颜色红、蓝、黄的帽子(一人 2020-06-03 …
形容颜色的词比如说什么样的颜色,带给人视觉享受或者可以说什么色彩我不是要组成颜色的词语啊,我是想要 2020-07-06 …
已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.化学 2020-07-18 …
已知一些银盐的颜色及溶解度数值如下:化学式AgClAgBrAgIAg2SAg2CrO4颜色白色浅黄 2020-07-18 …
已知一些银盐的颜色及溶解度数值如下:化学式AgClAgBrAgIAg2SAg2CrO4颜色白色浅黄色 2020-11-24 …
近现代科学研究告诉我们:颜色本身并不真正存在。或者不妨这样说,如果颜色确实存在的话,也只是因为人类在 2020-11-28 …
某同学将量程为200μA、内阻为500Ω的表头μA改装成量程为1mA和10mA的双量程电流表.电路如 2020-11-28 …
阅读文言文,完成下题。以学自损,不如无学文/颜之推①夫学者,所以求益耳①。见人读数十卷书,便自高大, 2020-12-14 …