如图所示,下列说法正确的是()A.甲池通入O2的电极反应为O2+4e-+4H+=2H2OB.乙池Ag电极增重6.4g,溶液中将转移0.2mol电子C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4
如图所示,下列说法正确的是( )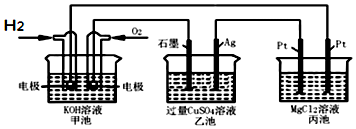
A. 甲池通入O2的电极反应为O2+4e-+4H+=2H2O
B. 乙池 Ag电极增重6.4g,溶液中将转移0.2mol电子
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D. 甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
B、电解质溶液中没有电子转移,是离子定向移动,故B错误;
C、电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,故C错误;
D、甲池中根据电极反应:O2+2H2O+4e-=4OH-,所以消耗280mL(标准状况下0.0125mol)O2,则转移电子0.05mol,根据丙装置中,在阴极上是氢离子放电,转移电子0.05mol,减小的氢离子是0.05mol,氢氧根离子是0.05mol,镁离子和氢氧根离子之间反应生成氢氧化镁,理论上最多产生氢氧化镁质量应该是0.05mol×
| 1 |
| 2 |
故选D.
电梯里放有一个弹簧体重计,质量为60kg的人站在体重计上,求下列四种情况中体重计的读数1.电梯不动或 2020-03-30 …
—寻找还原剂已知:As元素的电势图如下AsO43-(-0.71V)AsO33-(-0.68V)As( 2020-03-30 …
、3Fe3O4+28HNO3===9Fe(NO3)3+NO+14H20Fe升(3*1/3)*3N降 2020-05-13 …
氢氧化铝的碱式水解:Al(OH)3+4H2O=[Al(OH)2(H2O)4]2-+OH-中电荷不守 2020-05-13 …
AL的转化的方程式AL→ALCL3→AL(OH)3→ALCL3AL→AL2O3→ALAL→NA{A 2020-06-13 …
在25℃时,用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大 2020-07-20 …
!!!急~~~四羟基合铝酸根和二氧化碳反应老师写了2个方程式:CO2+[Al(OH)4]-==== 2020-07-29 …
电池重量是多少小明第一天捡了4节一号电池,5节5号电池.重是460.第二天捡了2节一号电池,3节五号 2020-11-25 …
电动起重机常用于工程建设,如图所示是某工地用电动机起吊重物示意图,该电动机铭牌上标有:额定电压380 2020-12-01 …
1.为什么最外层电子排满的铁比较活泼,而容易失去3个电子的铜不活泼,而且一般铜显+2价(应该是+3价 2020-12-12 …