早教吧作业答案频道 -->化学-->
将水分解制得氢气的一种工业方法是“硫-碘循环法”,依次涉及下列三步反应:I.SO2+2H2O+I2→H2SO4+2HIII.2HI(g)⇌H2(g)+I2(g)III.2H2SO4→2SO2+O2+2H2O(1)一定温度下,向5L恒容密闭容器
题目详情
将水分解制得氢气的一种工业方法是“硫-碘循环法”,依次涉及下列三步反应:
I.SO2+2H2O+I2→H2SO4+2HI
II.2HI(g)⇌H2(g)+I2(g)
III.2H2SO4→2SO2+O2+2H2O
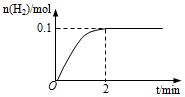
(1)一定温度下,向5L恒容密闭容器中加入1molHI,发生反应II,H2物质的量随时间的变化如图所示.0~2min内的平均反应速率v(HI)=___.相同温度下,若起始加入的HI改为2mol,反应达平衡时H2的量为___mol.
(2)分析上述反应,下列判断错误的是___(填写选项编号,只有一个正确选项).
a.三步反应均为氧化还原反应
b.循环过程中产生1molH2,同时产生1molO2
c.在整个分解水的过程中SO2和I2相当于催化剂.
I.SO2+2H2O+I2→H2SO4+2HI
II.2HI(g)⇌H2(g)+I2(g)
III.2H2SO4→2SO2+O2+2H2O
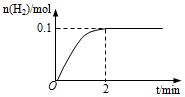
(1)一定温度下,向5L恒容密闭容器中加入1molHI,发生反应II,H2物质的量随时间的变化如图所示.0~2min内的平均反应速率v(HI)=___.相同温度下,若起始加入的HI改为2mol,反应达平衡时H2的量为___mol.
(2)分析上述反应,下列判断错误的是___(填写选项编号,只有一个正确选项).
a.三步反应均为氧化还原反应
b.循环过程中产生1molH2,同时产生1molO2
c.在整个分解水的过程中SO2和I2相当于催化剂.
▼优质解答
答案和解析
(1)方程式为2HI(g)⇌H2(g)+I2(g),平衡时氢气的物质的量为0.1mol,则消耗0.2molHI,0~2min内的平均反应速率v(HI)=
=0.02moL/(L•min),
相同温度下,若起始加入的HI改为2mol,相当于增大压强,平衡不移动,反应达平衡时H2的量为原平衡的2倍,应为0.2mol,
故答案为:0.02moL/(L•min);0.2;
(2)a.三步反应都涉及到单质,存在元素化合价的变化,均为氧化还原反应,故a正确;
b.总反应为2H2O
2H2+O2,循环过程中产生1molH2,同时产生0.5molO2,故b错误;
c.将Ⅰ+Ⅱ+Ⅲ×
可得H2O
H2+
O2,在整个分解水的过程中SO2和I2相当于催化剂,故c正确.
故答案为:b.
| ||
| 2min |
相同温度下,若起始加入的HI改为2mol,相当于增大压强,平衡不移动,反应达平衡时H2的量为原平衡的2倍,应为0.2mol,
故答案为:0.02moL/(L•min);0.2;
(2)a.三步反应都涉及到单质,存在元素化合价的变化,均为氧化还原反应,故a正确;
b.总反应为2H2O
| ||
c.将Ⅰ+Ⅱ+Ⅲ×
| 1 |
| 2 |
| ||
| 1 |
| 2 |
故答案为:b.
看了将水分解制得氢气的一种工业方法...的网友还看了以下:
单词辨音,判断每组单词划线部分的读音是(S)否(D)相同1.milk(划线部分为i)this(划线 2020-05-24 …
Performanceevaluation...o(1),O(n),O(n?2),O(logn)? 2020-06-03 …
有一电容器C=31.8uF,按u=220√2(根号2)sin(314t-45°).求1,电容器电路 2020-07-19 …
上面10,下面1∑(i*2^i)=过程O(∩∩)O谢谢 2020-07-21 …
O,I分别是锐角三角形ABC的外心,内心.O',I'分别是O,I关于BC的对称点.已知A、B、O' 2020-07-30 …
已知椭圆x^2/a^2+y^2/b^2=1(a>b>0)和圆O:x^2+y^2=b^2,过椭圆上一 2020-07-31 …
单词拼写。①brcc1A.o;o;iB.o;i;oC.o;o;y②cartA.roB.orC.re③ 2020-10-31 …
数据结构试题一、单项选择题(10)1、若长度为n的线性表采用顺序存储结构,在其第i个位置插入一个新元 2021-01-14 …
fori=1tonforj=1toifork=1tojx=x+1;这个的时间复杂度是多少呀!怎么算的 2021-01-14 …
设集合S={Ao,A1,A2,A3,),在S上定义运算@,Ai@Aj=Ak,其中Ak为i+j被4除的 2021-02-05 …