早教吧作业答案频道 -->化学-->
甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)⇌CH3OH(g).化学键H-HH-OO=O键能kJ/mol436x496已知:①图为反应的能量变
题目详情
甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)⇌CH3OH(g).
已知:
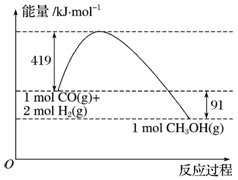
①图为反应的能量变化和物质键能
②CO(g)+
O2(g)═CO2(g)△H=-280kJ/mol
H2(g)+
O2(g)═H2O(l)△H=-284kJ/mol
H2O(l)═H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式___.
(2)H-O键的键能x为___kJ/mol.
(3)甲醇气体分解为CO和H2两种气体的反应的活化能为___kJ/mol.
| 化学键 | H-H | H-O | O=O |
| 键能kJ/mol | 436 | x | 496 |
①图为反应的能量变化和物质键能
②CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
H2O(l)═H2O(g)△H=+44kJ/mol
请回答下列问题:

(1)请写出表示气态甲醇燃烧热的热化学方程式___.
(2)H-O键的键能x为___kJ/mol.
(3)甲醇气体分解为CO和H2两种气体的反应的活化能为___kJ/mol.
▼优质解答
答案和解析
(1)由图可得热化学方程式:①CO(g)+2H2(g)=CH3OH(g)△H=-91kJ/mol,
又已知:②CO(g)+
O2(g)═CO2(g)△H=-280kJ/mol
③H2(g)+
O2(g)═H2O(l)△H=-284 kJ/mol
根据盖斯定律,③×2+②-①可得:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-757kJ•mol-1,
故答案为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-757kJ•mol-1;
(2)已知:H2(g)+
O2(g)═H2O(l)△H=-284 kJ/mol,
H2O(l)═H2O(g)△H=+44kJ/mol
二者相加可得:H2(g)+
O2(g)═H2O(g)△H=-240 kJ/mol,
反应热=反应物总键能-生成物总键能,则436kJ/mol+
×496kJ/mol-2×x kJ/mol=-240kJ/mol,解得x=462,
故答案为:462;
(3)由图形可知甲醇气体分解为CO和H2两种气体的反应的活化能为(419+91)kJ/mol=510kJ/mol,
故答案为:510.
又已知:②CO(g)+
| 1 |
| 2 |
③H2(g)+
| 1 |
| 2 |
根据盖斯定律,③×2+②-①可得:CH3OH(g)+
| 3 |
| 2 |
故答案为:CH3OH(g)+
| 3 |
| 2 |
(2)已知:H2(g)+
| 1 |
| 2 |
H2O(l)═H2O(g)△H=+44kJ/mol
二者相加可得:H2(g)+
| 1 |
| 2 |
反应热=反应物总键能-生成物总键能,则436kJ/mol+
| 1 |
| 2 |
故答案为:462;
(3)由图形可知甲醇气体分解为CO和H2两种气体的反应的活化能为(419+91)kJ/mol=510kJ/mol,
故答案为:510.
看了 甲醇是重要的工业原料.煤化工...的网友还看了以下:
已知函数f(x)=1/2x^2-3x-3/4已知f(7/2)=-41/8,不用带入值计算,...已 2020-04-26 …
数学题目,一定要有过程!方括号代表根号(1)[x+2][2x+3]-x=2(2)(x/x+1)平方 2020-04-27 …
1.甲数与乙数的比值是2/5,甲、乙俩数的和是21,甲数是多少?比乙数少百分之几?2.同学们采集树 2020-05-13 …
求下列数学题的解.已知ΔABC中<A=30°,b=4c=7求abc2.已知偶函数f(x)在单调增加 2020-06-14 …
已知矩阵B,求B^2,B^3,B^4.已知矩阵B0a00000a00000a00000a00000 2020-07-09 …
六一班同学分三组采集树种,第一组,第二组,第三组采集的树种质量比是5比3比4,已知第一组比第二组多 2020-07-17 …
已知空间三个点P(-2,0,2),Q(-1,1,2)和R(-3,0,4)已知空间三个点P(-2,0 2020-07-20 …
有关分式的数学题1.已知多项式A能被X-1整除,则方程式A=0一定有一个跟是2.A^2+2AB+B 2020-07-30 …
六1班同学分三组采集树种.第一组、第二组、第三组采集的树种的质量比是5:3:4.已知第一组比第二组多 2020-11-24 …
六(1)班同学分三组采集树种.第一组、第二组、第三组采集的树种的质量比是5比3比4.已知第一组比第二 2020-11-24 …